Clear Sky Science · de
Die Fluorchinolin-Verbindung wirkt anti-erythroleukämisch durch Doppelwirkung auf GLUT1 und den PI3K/AKT-Signalweg
Ein neuer Blick auf eine gefährliche Blutkrebserkrankung
Erythroleukämie ist eine seltene, aber hoch aggressive Form von Blutkrebs mit wenigen Behandlungsoptionen jenseits der Stammzelltransplantation. Für viele, meist ältere Patientinnen und Patienten bedeutet das harte Therapien, hohe Kosten und schlechte Aussichten. Diese Studie untersucht eine im Labor entwickelte Verbindung namens FKL-137, die Erythroleukämiezellen auf unerwartete Weise angreift: indem sie deren bevorzugten Brennstoff, Zucker, abschneidet und so den Zelltod auslöst. Die Arbeit deutet auf eine mögliche neue Klasse gezielter Wirkstoffe hin, die die Abhängigkeit von Krebszellen von verändertem Energiestoffwechsel ausnutzen, während sie gesunde Gewebe weitgehend schonen.
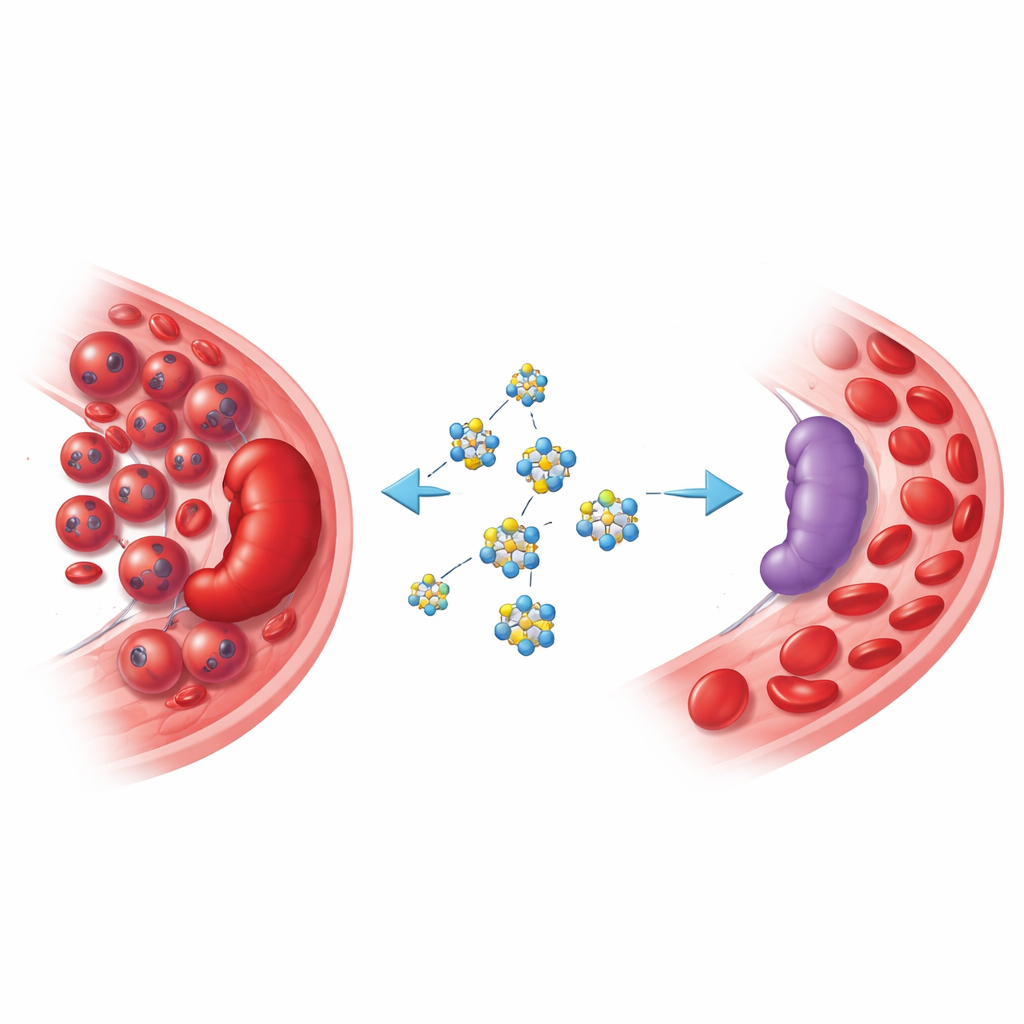
Wenn Blutzellen außer Kontrolle geraten
Bei der Erythroleukämie vermehren sich unreife Vorläufer roter Blutkörperchen im Knochenmark und in der Milz unkontrolliert. Patientinnen und Patienten können schwere Anämie, vergrößerte Milz mit Rupturgefahr und einen raschen Gesundheitsverfall entwickeln. Die verfügbaren Therapien sind begrenzt, und viele Betroffene sind für aggressive Behandlungen zu gebrechlich. Zugleich haben Forschende erkannt, dass viele Bluttumoren auf umprogrammierten Zuckerverbrauch angewiesen sind: Sie nehmen Glukose in hohem Tempo auf und wandeln sie rasch in Energie und Bausteine um, was ihre Teilung fördert und dem Immunsystem das Erkennen erschwert. Diese metabolische „Sucht“ zu adressieren, ist zu einer attraktiven Strategie für neue Medikamente geworden.
Krebszellen vom Zucker abschneiden
Die Forschenden konzentrierten sich auf ein kleines synthetisches Molekül, FKL-137, das aus einer chemischen Familie stammt, die bereits für antitumorale Aktivität bekannt ist. In Laborversuchen setzten sie zwei menschliche Erythroleukämie-Zelllinien steigenden Dosen von FKL-137 aus. Die Verbindung verlangsamte das Zellwachstum deutlich über die Zeit und trieb die Zellen in den programmierten Zelltod, erkennbar an klassischen Veränderungen der Zellgestalt und der Aktivierung intrazellulärer Todesmechanismen. Wichtig ist, dass FKL-137 gegen Leukämiezellen deutlich wirkstärker war als gegen normale Leberzellen, und Sicherheitsmessungen deuteten bei wirksamen Dosen auf vergleichsweise geringe Toxizität hin.
Die Zucker-Tore des Krebses treffen
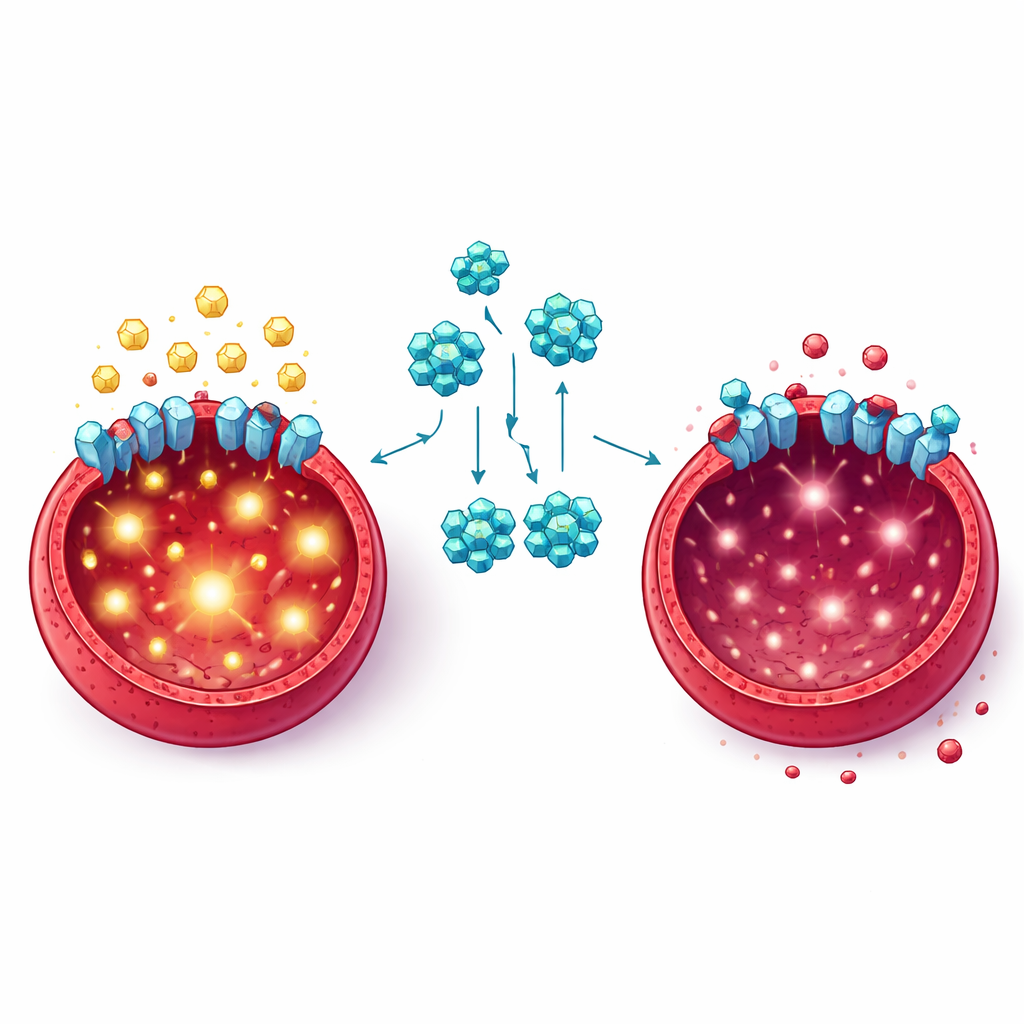
Um tiefer zu verstehen, wie FKL-137 den Krebsstoffwechsel stört, untersuchte das Team die Glukoseaufnahme und Metabolite. Behandelte Leukämiezellen nahmen weniger Glukose auf und setzten weniger Laktat frei, ein Nebenprodukt intensiver Zuckerverbrennung. Schlüsseleiweiße, die normalerweise bei der Umwandlung von Glukose in Energie und Bausteine helfen, waren herunterreguliert. Mithilfe von computergestützter Modellierung, thermischen Stabilitätstests und Bildgebung zeigten die Forschenden, dass FKL-137 an GLUT1 bindet, ein zentrales „Tor“ an der Zelloberfläche, das Glukose ins Zellinnere aufnimmt. Wurden die GLUT1-Spiegel genetisch reduziert, wuchsen die Leukämiezellen langsamer, nutzten weniger Zucker und wurden noch empfindlicher gegenüber FKL-137. Das bestätigte, dass GLUT1 sowohl das Wachstum von Erythroleukämiezellen fördert als auch ein wichtiges Ziel des Wirkstoffs ist.
Störung einer wachstumsfördernden Signalachse
Die Studie förderte zudem Effekte zutage, die über das Zucker-Tor hinausgehen. Erythroleukämiezellen nutzen normalerweise den Signalweg PI3K/AKT, um Überleben, Wachstum und hohen Zuckerverbrauch zu unterstützen, teilweise durch Unterstützung von GLUT1. Die Behandlung mit FKL-137 verringerte die aktiven Formen zentraler Proteine dieses Weges und unterbrach so eine Verstärkungsschleife zwischen Zuckertransport und Wachstumssignalen. In Mäusen, die mit einem Virus infiziert waren, das zuverlässig Erythroleukämie auslöst, verbesserte FKL-137 die roten Blutbildwerte, verkleinerte vergrößerte Milzen, verringerte das Eindringen von Krebszellen in Organe und normalisierte den gestörten Zuckerstoffwechsel im Milzgewebe — und das ohne erkennbare Schäden an Herz, Leber, Lunge oder Niere.
Verheißung, Grenzen und nächste Schritte
In der Summe präsentieren die Autorinnen und Autoren FKL-137 als Kandidaten mit Doppelwirkung: Es blockiert das wichtigste Zucker-Tor von Erythroleukämiezellen und dämpft gleichzeitig einen kraftvollen Wachstumsweg, der von diesem Brennstoff abhängt. Indem der Wirkstoff die Krebszellen zunächst aushungert und sie dann in Richtung Zelltod treibt, bietet er einen konzeptionell eleganten Weg, eine Schwäche auszunutzen, die normale Zellen nicht im gleichen Maße teilen. Die Forschenden mahnen jedoch zur Vorsicht: FKL-137 hat ein relativ schmales Dosierungsfenster, Krebszellen könnten Wege finden, ihren Stoffwechsel umzuleiten, und Befunde aus Zelllinien und Mausmodellen müssen in menschlichen Geweben bestätigt werden. Dennoch stärkt die Studie die Idee, dass eine präzise Angriffnahme auf das Ernährungsverhalten und Wachstum von Krebszellen eine neue Front in der Behandlung dieser sonst schwer zu beherrschenden Blutkrebserkrankung eröffnen könnte.
Zitation: Cheng, S., Zhao, W., Yu, J. et al. The fluoroquinoline compound exerts anti-erythroleukemic effects by dual-targeting GLUT1 and the PI3K/AKT signaling pathway. Sci Rep 16, 10916 (2026). https://doi.org/10.1038/s41598-026-45597-9
Schlüsselwörter: Erythroleukämie, Krebsstoffwechsel, GLUT1-Inhibitor, PI3K AKT-Signalweg, gezielte Therapie