Clear Sky Science · de
Früherkennung des metastatischen Risikos bei primärem kutanem Melanom mittels schwach überwachtem Lernen
Warum das für Patienten und Ärztinnen wichtig ist
Hauta Melanom kann tödlich sein, nicht wegen des Flecks auf der Haut selbst, sondern weil einige Tumoren still in andere Organe streuen. Heute verlassen sich Ärztinnen und Ärzte vor allem auf die Tumordicke und darauf, ob die Oberfläche durchbrochen ist, um einzuschätzen, welche Patientinnen und Patienten das größte Risiko haben. Diese Studie fragt, ob moderne künstliche Intelligenz (KI) deutlich mehr aus routinemäßigen Mikroskopbildern des ursprünglichen Hauttumors ablesen kann und gefährliche Krebsarten früher erkennt — insbesondere bei Patientinnen und Patienten, deren Tumoren noch vergleichsweise klein erscheinen.
Suche nach stillen Warnzeichen in Gewebsbildern
Die Forschenden sammelten digitale Versionen standardmäßiger Objektträger von 426 primären Hautmelanomen sowie grundlegende Informationen wie Tumordicke, Ulzeration, Mitoserate und Tumorgröße. Etwa drei von fünf dieser Tumoren führten später zu Befall von Lymphknoten oder Fernmetastasen, während der Rest über mindestens drei Jahre Nachbeobachtung nicht metastasierte. Anstatt Pathologinnen und Pathologen zu bitten, bestimmte Bereiche per Hand zu markieren, ließen die Forschenden den Computer jeden Teil jedes Objektträgers untersuchen und schnitten jedes riesige Bild in viele kleine Ausschnitte. Die Frage war einfach: Kann ein Computer, der nur darauf trainiert wurde, ob jede Patientin/jeder Patient schließlich Metastasen entwickelte oder nicht, visuelle Muster lernen, die Hochrisiko- von Niedrigrisiko-Tumoren trennen?
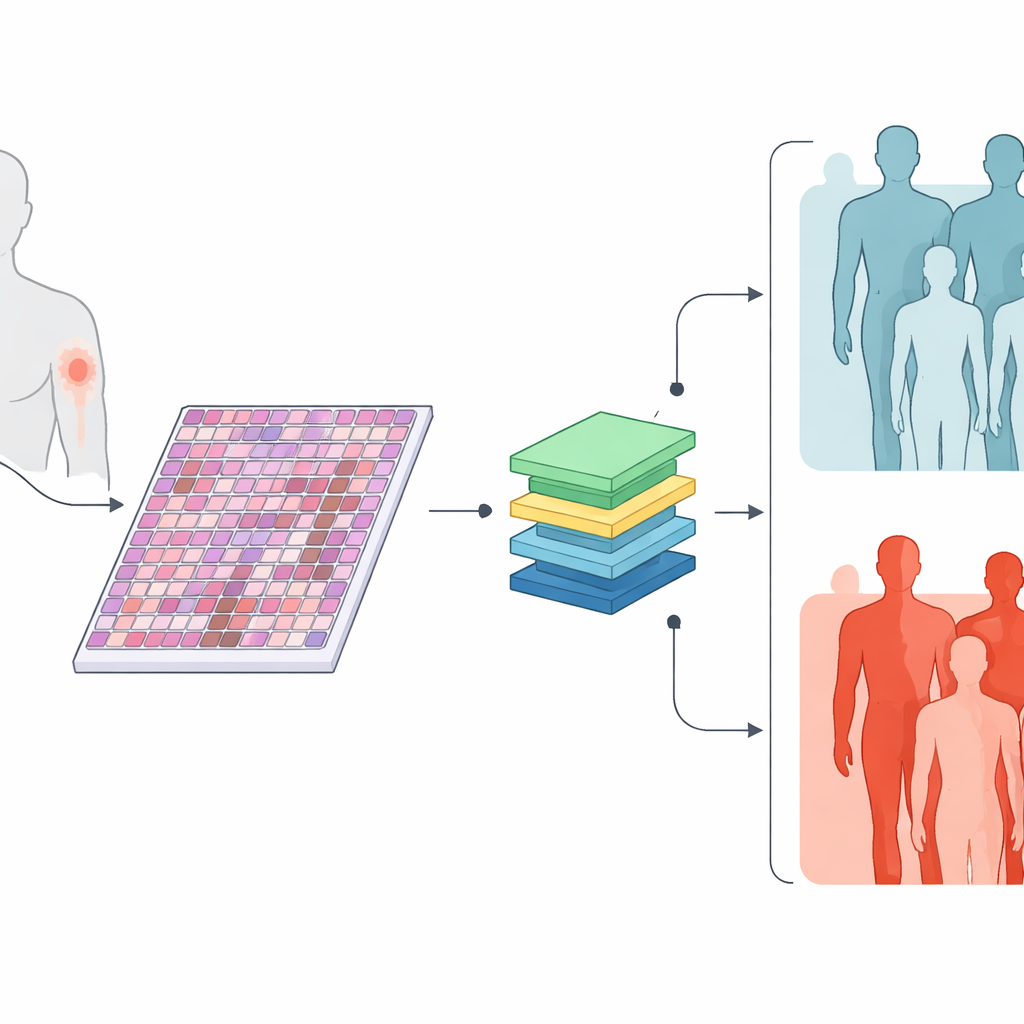
Maschinen beibringen, Gewebe wie eine Karte zu lesen
Das Team nutzte neuere KI-Methoden, die zuerst an riesigen Sammlungen medizinischer Bilder und Texte vortrainiert und dann auf Melanom angepasst wurden. Ein Modell namens TransMIL betrachtete nur die Gewebebilder. Ein anderes, MultiTrans, verband die Bildinformation mit einer kompakten Textbeschreibung der klinischen Tumormerkmale. Ein drittes, einfacheres Modell, BertMLP, verwendete nur diese klinischen Merkmale und ignorierte die Bilder. Getestet an einer separaten Gruppe von Objektträgern, die das System zuvor nicht gesehen hatte, trennten beide bildbasierten Modelle metastatische von nicht-metastatischen Tumoren in etwa 85 % der Fälle korrekt und zeigten insgesamt eine höhere Genauigkeit als das nur auf klinischen Daten basierende Modell. Dies legt nahe, dass die Mikroskopbilder reichhaltige Hinweise auf das zukünftige Verhalten enthalten, die die aktuellen Routinemessungen nicht vollständig erfassen.
Stärkere Unterstützung dort, wo Entscheidungen am schwierigsten sind
Der Vorteil der bildbasierten KI war am deutlichsten bei Tumoren mittlerer Dicke, einer Gruppe, bei der Ärztinnen und Ärzte am meisten damit ringen, zu entscheiden, wer eine aggressive Behandlung braucht. Bei diesen T2-Melanomen übertrafen die Bildmodelle das nur klinische Modell klar, das dazu neigte, zu viele Tumoren als Niedrigrisiko einzustufen. Die bildbasierten Systeme lieferten auch bei dickerer Tumoren gute Ergebnisse, doch diese Fälle gelten nach Standardmaßen ohnehin bereits als gefährlich. In mehreren Patientinnen und Patienten, die zunächst als nicht-metastatisch klassifiziert wurden, später aber Metastasen entwickelten, stuften die KI-Modelle die Primärtumoren Jahre früher korrekt als hochriskant ein, was andeutet, wie solche Werkzeuge eines Tages eine frühere, gezieltere Therapie unterstützen könnten.
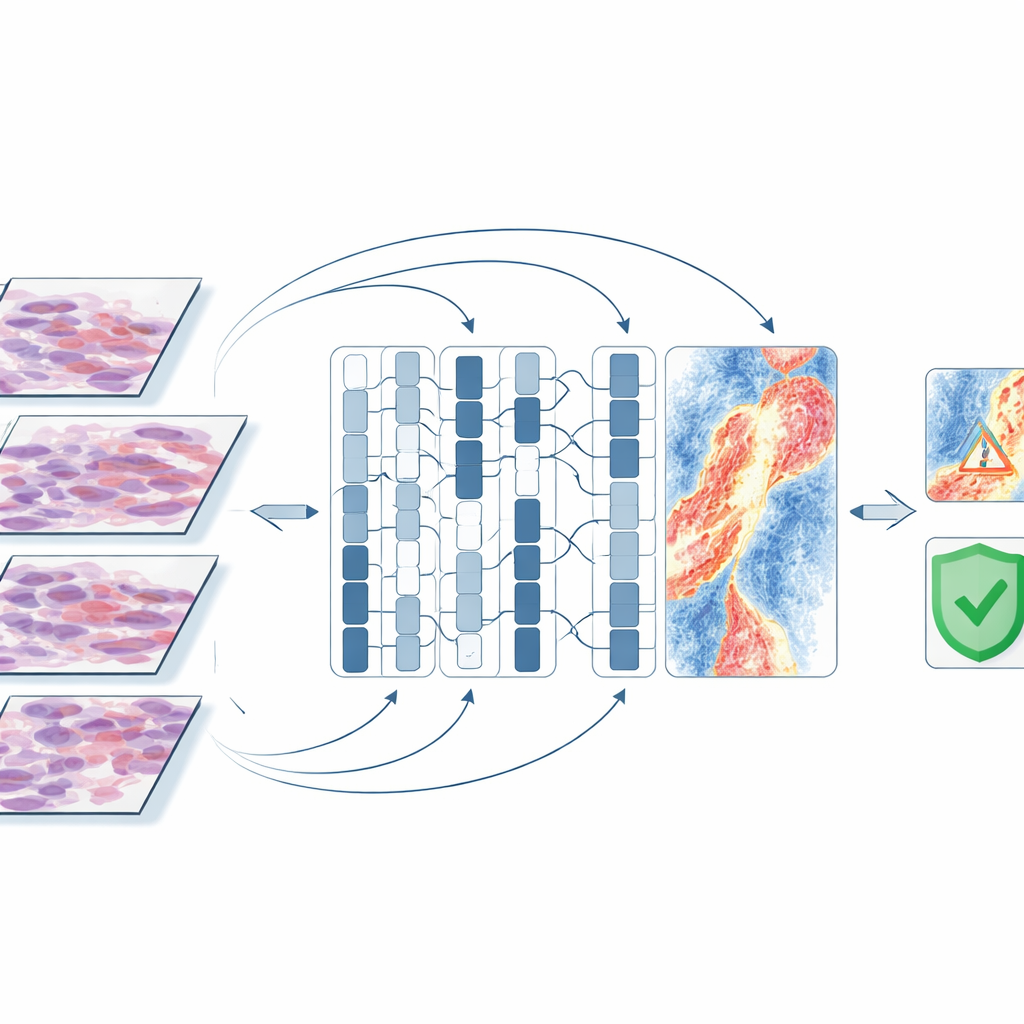
Worauf die KI im Tumor „blickt”
Um zu verstehen, welche Hinweise der Computer nutzte, erzeugten die Forschenden Aufmerksamkeitskarten, die die Regionen auf dem Objektträger hervorheben, die für eine bestimmte Vorhersage besonders einflussreich waren. Bei Tumoren, die schließlich streuten, konzentrierten sich die Modelle oft nicht auf dichte Zellklumpen des Tumors, sondern auf das umliegende Umfeld: Blutgefäße, Bereiche mit Oberflächenzerfall und Ansammlungen entzündlicher Zellen tiefer in der Haut. Bei Tumoren ohne Streuung hoben sich tendenziell intakte Oberflächenschichten mit wenigen Schadenszeichen hervor. Fehlklassifizierte Fälle enthielten oft unscheinbares Bindegewebe, Fett oder Artefakte aus der Präparation der Objektträger, was darauf hindeutet, dass der Computer Schwierigkeiten hatte, wenn klare Gewebezeichen schwach waren. Diese Muster stimmen mit dem aktuellen Verständnis überein, wie Melanomzellen in Lymphbahnen und Blutgefäße entkommen, und verleihen den Entscheidungen der KI biologische Plausibilität.
Grenzen, nächste Schritte und mögliche Bedeutung
Diese Arbeit wurde an einem einzigen Krankenhaus an einigen hundert Tumoren durchgeführt; die Modelle wurden noch nicht über verschiedene Zentren hinweg getestet und nicht zur Vorhersage der Überlebenszeit verwendet. Der Ansatz ersetzt auch nicht die Pathologin bzw. den Pathologen; vielmehr fügt er eine neue Ebene von Risikoinformationen hinzu, die automatisch aus Routinenpräparaten extrahiert wird. Trotzdem zeigen die Ergebnisse, dass schwach überwachbare KI sinnvolle Warnsignale einer Streuung direkt im Primärtumorgewebe aufdecken kann, ohne arbeitsintensive manuelle Markierungen. Wenn dies in größeren, multizentrischen Studien validiert und mit anderen Daten wie Hautfotos und Genexpressionsanalysen kombiniert wird, könnten solche Werkzeuge Ärztinnen und Ärzten helfen, Patientinnen und Patienten mit scheinbar frühem Stadium Melanom besser zu identifizieren, die heimlich ein hohes Metastasierungsrisiko tragen, und ihnen engmaschigere Kontrollen oder frühere präventive Behandlungen anbieten.
Zitation: Dahlén, F., Shujski, I., Yacob, F. et al. Early detection of metastatic risk in primary cutaneous melanoma using weakly supervised learning. Sci Rep 16, 11234 (2026). https://doi.org/10.1038/s41598-026-45588-w
Schlüsselwörter: Melanom, metastatisches Risiko, digitale Pathologie, künstliche Intelligenz, schwach überwachtes Lernen