Clear Sky Science · de
Machbarkeitsnachweis für die Extraktion von zellfreier DNA aus Plasma mittels eines wässrigen Zwei-Phasen-Systems für Anwendungen der Flüssigbiopsie
Warum ein Bluttest bei Krebs und anderen Erkrankungen wichtig ist
Viele moderne medizinische Tests suchen nach winzigen DNA-Fragmenten, die frei in unserem Blut zirkulieren. Diese Fragmente, als zellfreie DNA bezeichnet, können Hinweise darauf geben, ob ein Tumor genetisches Material abgibt, ob ein transplantiertes Organ abgestoßen wird oder wie sich eine Schwangerschaft entwickelt. Da diese DNA-Fragmente jedoch selten, kurz und mit einem Gemisch aus Proteinen und anderen Molekülen vermischt sind, ist ihre saubere und schnelle Gewinnung überraschend schwierig. Diese Studie stellt eine neue, einfachere Methode vor, um diese Fragmente aus Blutplasma mittels einer schonenden, wasserbasierten Trenntechnik zu extrahieren, was fortgeschrittene „Flüssigbiopsie“-Tests möglicherweise zugänglicher und kostengünstiger machen könnte.
Die Herausforderung, winzige DNA-Teile herauszufischen
Ärztinnen, Ärzte und Forschende nutzen Flüssigbiopsien, um genetische Hinweise aus einer einfachen Blutentnahme zu lesen statt Gewebe zu entnehmen. Das Problem ist, dass zellfreie DNA im Plasma typischerweise nur in wenigen Dutzend Nanogramm pro Milliliter vorliegt und in kurze Stücke zerkleinert ist. Ein kleiner Anteil dieses Materials kann von einem Tumor oder einem transplantierten Organ stammen, sodass jedes Fragment zählt. Gängige Extraktionskits binden DNA über Silikatoberflächen in Gegenwart starker Salze, gefolgt von mehreren Waschapparaten und Zentrifugationsschritten. Diese Kits funktionieren gut, benötigen aber Zeit, spezielle Geräte und können teuer sein. Sie haben außerdem Schwierigkeiten, die kürzesten Fragmente zu erfassen, und können langes genomisches DNA-Material mitnehmen, das seltene, krankheitsbezogene Signale überlagern kann.
Ein zwei-lagiger Wassertrick, um DNA zu fangen
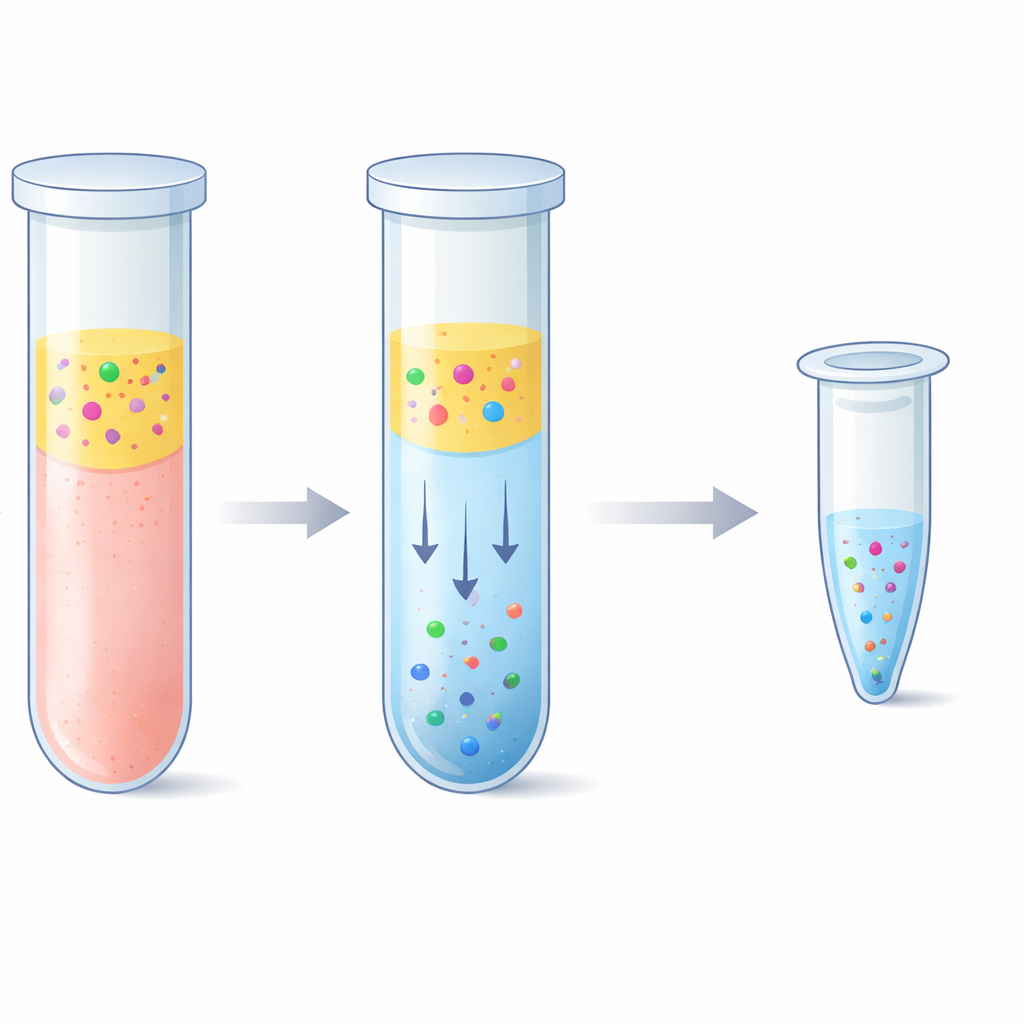
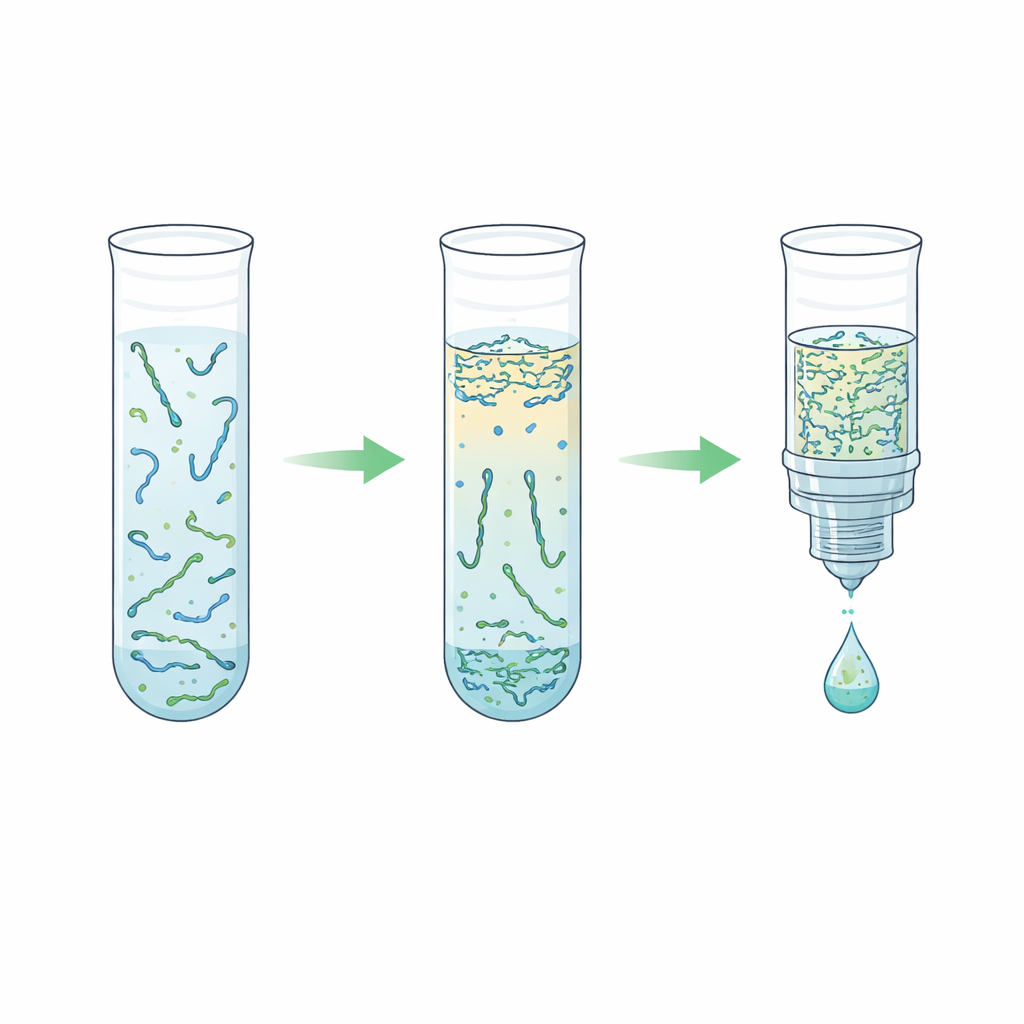
Das Team untersuchte eine Alternative, basierend auf einem „wässrigen Zwei-Phasen-System“ – einfach gesagt zwei wasserreiche Flüssigkeiten, die sich nicht vollständig mischen, ähnlich wie Öl und Essig, aber beide größtenteils aus Wasser bestehen. Durch Kombination von Plasma mit einem Polymer namens Polyethylenglykol und einfachen Phosphatsalzen trennte sich die Mischung von selbst in eine obere und eine untere Schicht. Bemerkenswerterweise bevorzugten die kurzen DNA-Fragmente stark die salzreiche untere Schicht, während die meisten Blutproteine und langen DNA-Stränge in der oberen Schicht oder an der Grenzfläche blieben. Die Forschenden stimmten das Rezept sorgfältig so ab, dass die untere Schicht klein genug blieb, um die DNA zu konzentrieren, aber schonend genug, um sie nicht zu beschädigen. Anschließend kombinierten sie diesen Schritt mit einer „Reverse-Elution“-Reinigung, bei der die salzreiche untere Schicht durch eine poröse Matrix gedrückt wird, um Salz zu entfernen und das Endvolumen zu verringern, was in einer saubereren und konzentrierteren DNA-Lösung endete.
Verfeinerung des Prozesses für die Praxis
In zahlreichen Tests passten die Autorinnen und Autoren das Verhältnis von Polymer und Salz, Zentrifugationsgeschwindigkeiten, Volumina und optionale Lyse-Schritte an, die Protein–DNA-Komplexe aufbrechen. Sie stellten fest, dass durch Erhöhen des Polymergehalts entlang bestimmter Zusammensetzungslinien die DNA-Konzentration verdoppelt werden konnte, ohne die Rückgewinnung zu beeinträchtigen, und dass eine stärkere Konditionierung im Reverse-Elution-Schritt die Konzentration im Vergleich zu früheren Arbeiten etwa vervierfachte. Überraschenderweise zeigte sich, dass das Auslassen harscher Lyse vor der Zwei-Phasen-Trennung oft am besten funktionierte; Lyse neigte dazu, die Phasen zu stören und den Ertrag zu verringern. Ein gestraffter, weitgehend lysefreier Arbeitsablauf entfernte rund 99,7 % der Plasmaproteine und gewann dabei bis zu etwa zwei Drittel der kurzen DNA-Eingangsmenge in einem um das Vierfache kleineren Volumen zurück – alles in etwa zehn Minuten Gesamtlaufzeit und nur wenigen Minuten manueller Arbeit.
Wie sich die neue Methode im Vergleich schlägt
Die Forschenden verglichen ihren Ansatz mit einem weit verbreiteten kommerziellen Silikat-Kit. Das Standardkit lieferte etwas höhere Gesamt-DNA-Ausbeuten und stärkere Konzentrationen, weil es in sehr kleine Volumina eluierte. Dennoch zeigte die Zwei-Phasen-Methode konsistente Rückgewinnungsraten oberhalb von 60 % über eine Bandbreite von DNA-Eingängen, selbst bei sehr kleinen Startmengen, und erforderte deutlich weniger manuelle Schritte und weniger Ausrüstung. Wichtig ist, dass der neue Prozess eine eingebaute Fragmentlängen-Filterwirkung zeigte: Er reicherte kurze, zellfreie-ähnliche DNA an und schloss weitgehend lange Stränge aus, die von zerstörten Blutzellen stammen können. Tests mittels quantitativer PCR zeigten, dass die gereinigten Extrakte die nachgelagerte Amplifikation nicht inhibierten. Als das Team eine kommerzielle Referenzprobe mit bekannten krebsrelevanten Mutationen verwendete, ließ sich die mit ihrer Methode gewonnene DNA zu Sequenzierbibliotheken aufbereiten, auf einem Hochdurchsatz-Sequenzer auslesen und zur Detektion aller erwarteten Varianten in den richtigen Frequenzen nutzen.
Was das für zukünftige Bluttests bedeuten könnte
Kurz gesagt zeigt diese Arbeit, dass eine vergleichsweise einfache, wasserbasierte Trennung die komplexere Feststoffoberflächenchemie zur Vorbereitung zellfreier DNA aus Plasma ersetzen kann. Obwohl die neue Methode derzeit etwas weniger DNA liefert als Spitzengeräte kommerzieller Kits, bietet sie schnelle Verarbeitung, eine starke Entfernung unerwünschter Proteine und langer DNA sowie gute Kompatibilität mit PCR und Next-Generation-Sequencing. Wenn sie an echten Patientenproben weiter validiert und für die Automatisierung verfeinert wird, könnte dieser Ansatz Kosten senken und Laborabläufe vereinfachen, wodurch präzise, genetisch basierte Bluttests für Krebs, Transplantationen und andere Erkrankungen breiter verfügbar werden könnten.
Zitation: Meutelet, R., Buerfent, B.C., Hess, T. et al. Proof of concept for aqueous two-phase system-based extraction of cell-free DNA from plasma for liquid biopsy applications. Sci Rep 16, 11232 (2026). https://doi.org/10.1038/s41598-026-45585-z
Schlüsselwörter: Flüssigbiopsie, zellfreie DNA, Krebs-Bluttest, DNA-Extraktion, Next-Generation-Sequencing