Clear Sky Science · de
Interferon-β und FTY720 lindern progressive ZNS-Entzündung durch SOCS1-assoziierte Astrozyten-Signalgebung
Warum diese Forschung für Menschen mit Multipler Sklerose wichtig ist
Für viele Menschen mit Multipler Sklerose (MS) ist die größte Sorge nicht das frühe Aufflammen von Symptomen, sondern der langsame, stetige Funktionsverlust, der folgen kann. In dieser späteren, progredienten Phase setzt sich der Schaden im Gehirn und Rückenmark fort, selbst wenn Standardmedikamente, die das Immunsystem im Blut anvisieren, wirken. Diese Studie untersucht einen Ansatz, um jene „versteckte“ Entzündung anzugehen, indem ein bereits verfügbares MS-Tablett mit einer Form eines lang genutzten Medikaments kombiniert wird, das gezielt zum Gehirn gelangt.
Eine langwierige Erkrankung des Gehirns mit wenigen Optionen
MS ist eine Autoimmunerkrankung, bei der körpereigene Immunzellen die Isolierung von Nervenfasern angreifen, was zu Sehstörungen, Schwäche und weiteren neurologischen Symptomen führt. Früh treten die Beschwerden oft schubartig auf und wieder ab. Im Laufe der Zeit treten viele Patientinnen und Patienten in eine progrediente Phase ein, die durch eine schrittweise, oft irreversible Behinderung gekennzeichnet ist. In diesem Stadium wird die Blut-Hirn-Schranke für Wirkstoffe schwerer zu durchdringen, und schädliche Aktivität von im Gehirn sitzenden Zellen, den Gliazellen – insbesondere Astrozyten und Mikroglia – gewinnt an Bedeutung. Die derzeitigen Therapien, die überwiegend Immunzellen im Blut blockieren, bieten in diesem Stadium nur begrenzte Hilfe.
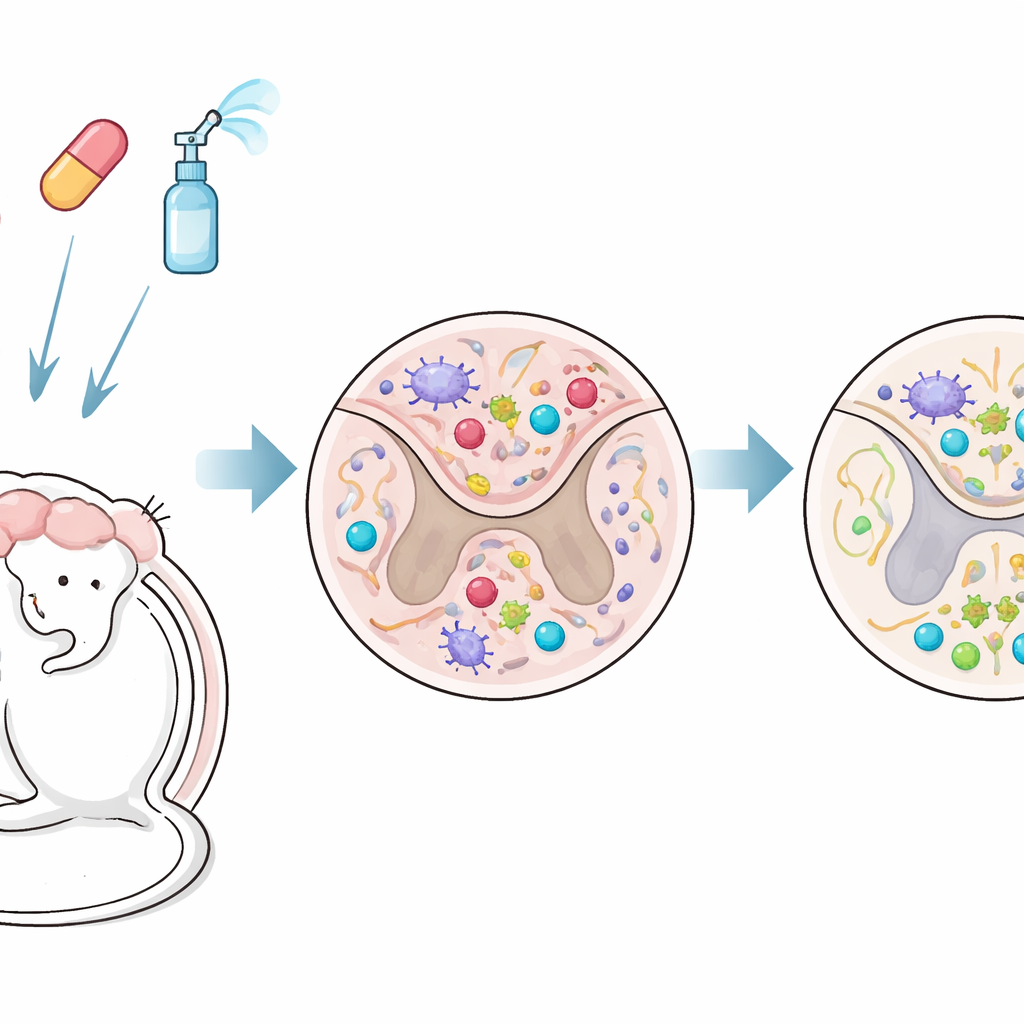
Zwei Medikamente kombinieren, um Blut und Gehirn zu erreichen
Die Forschenden testeten eine kombinierte Behandlung in einem Mausmodell, das die progrediente MS gut nachbildet. Ein Wirkstoff, Fingolimod (FTY720), ist eine Tablette, die Immunzellen in den Lymphknoten zurückhält und außerdem ins Gehirn gelangen kann. Der andere, Interferon‑beta, ist eine seit langem eingesetzte MS-Therapie, die normalerweise außerhalb des Gehirns wirkt, da sie die Blut-Hirn-Schranke nicht leicht überwindet. In dieser Studie wurde Interferon‑beta intranasal verabreicht – durch die Nase –, sodass es diese Schranke umgehen und das zentrale Nervensystem direkter erreichen konnte. Die Behandlung begann, nachdem die Mäuse bereits chronische neurologische Probleme entwickelt hatten, was einem Stadium entspricht, in dem Schäden typischerweise schwerer umkehrbar sind.
Weniger Schaden und gedämpfte Immunaktivität
Mäuse, die die kombinierte Behandlung mit Fingolimod plus intranasalem Interferon‑beta erhielten, schnitten besser ab als jene, die nur Fingolimod bekamen. Ihre Krankheitswerte verbesserten sich stärker, und einige bestehende neurologische Defizite nahmen ab. Bei der Untersuchung des Rückenmarks fanden die Wissenschaftler mehr erhaltene Myelinscheiden, weniger Zeichen axonaler Schädigung und weniger eindringende Immunzellen. Proinflammatorische T-Zellen und Monozyten waren reduziert, und die verbleibenden T-Zellen produzierten weniger der schädlichen Botenstoffe Interferon‑gamma und IL‑17. Wichtig ist, dass die Kombinationstherapie auch schädliche Signale von Astrozyten und Mikroglia dämpfte – den Gliazellen, die das lokale Umfeld im Gehirn und Rückenmark mitgestalten.
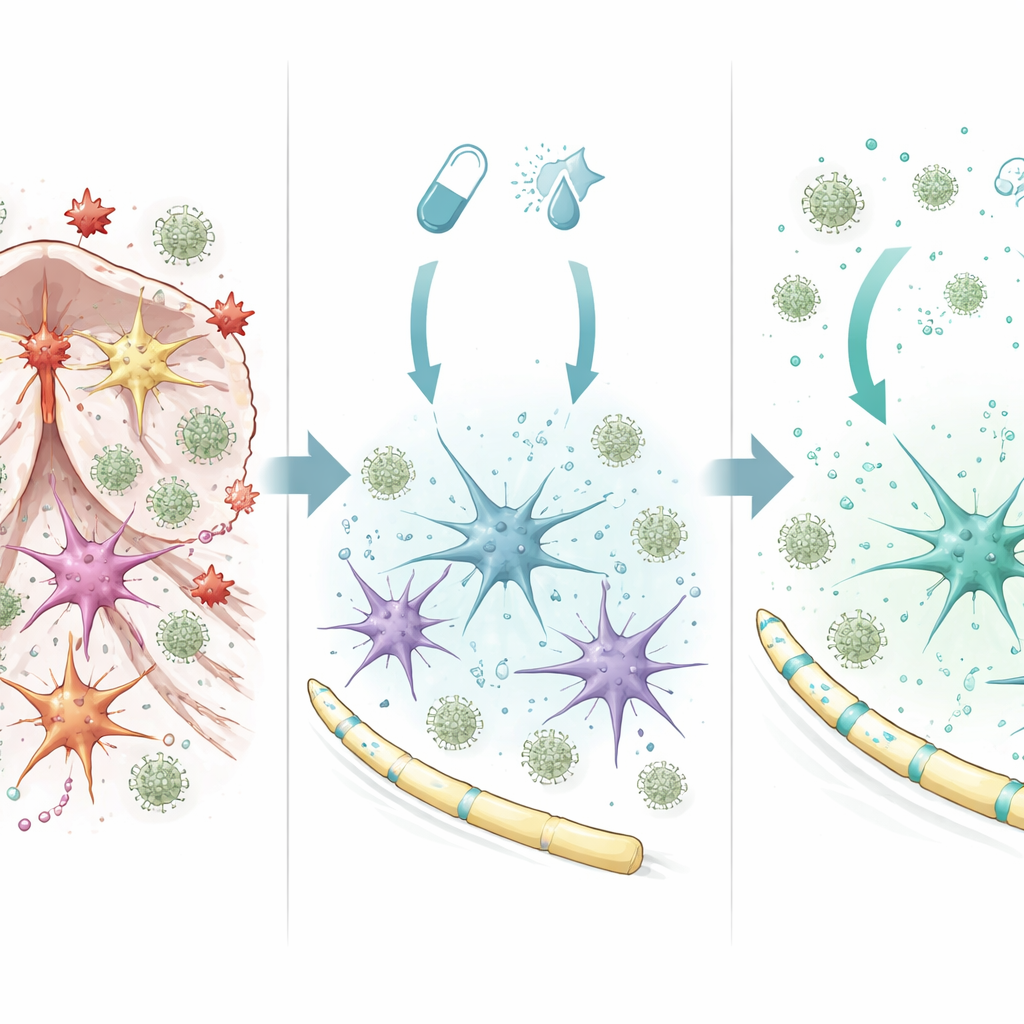
Astrozyten wechseln von schädlichem zu schützendem Verhalten
Um zu verstehen, wie die Kombinationstherapie im Gehirn wirkt, untersuchte das Team gereinigte Astrozyten in Kultur. Unter dem Einfluss von Fingolimod plus Interferon‑beta schalteten Astrozyten ein breites Genprogramm ein, das mit Zellüberleben, verringerter Entzündung und gesünderer Nervenisolation verknüpft ist. Ein zentraler Faktor war ein Regulator namens SOCS1, der als Bremse für entzündliche Signalwege wirkt. Die Blockade von SOCS1 in Astrozyten löschte einen Großteil des schützenden Genmusters und veranlasste diese Zellen dazu, mehr entzündliche Faktoren freizusetzen, die Immunzellen anlockten. Im Gegensatz dazu produzierten Astrozyten mit aktivem SOCS1 mehr Wachstums- und Reparatursignale und setzten ein Gemisch von Molekülen frei, das die Migration entzündlicher Monozyten verringerte. Ähnliche schützende Verschiebungen wurden in mit der Wirkstoffkombination behandelten humanen Astrozyten- und Mikroglia-Zelllinien beobachtet, was darauf hindeutet, dass der Mechanismus über Mäuse hinaus relevant ist.
Was das für zukünftige MS-Therapien bedeuten könnte
Die Studie zeigt, dass die Kombination von Fingolimod mit intranasal verabreichtem Interferon‑beta mehr bewirken kann, als nur Immunzellen im Blut zu blockieren. Sie kann Astrozyten im zentralen Nervensystem umprogrammieren und in einen ruhigeren, schützenden Zustand versetzen, wobei SOCS1 als zentrales Kontrollglied fungiert. Da die Arbeiten an Mäusen und in Zellkulturen durchgeführt wurden und Interferon‑beta nicht in allen Experimenten einzeln nebenverglichen wurde, sind weitere Untersuchungen nötig. Die Ergebnisse deuten jedoch auf eine vielversprechende Strategie hin: sowohl das periphere Immunsystem als auch die im Gehirn ansässigen Stützzellen gleichzeitig anzugreifen. Wenn ähnliche Effekte beim Menschen erzielt und als sicher nachgewiesen werden können, könnten solche kombinierten, gehirnzentrierten Ansätze dazu beitragen, den stillen Schaden zu verlangsamen oder teilweise umzukehren, der die progrediente MS vorantreibt.
Zitation: Tsaktanis, T., Beyer, T., Nirschl, L. et al. Interferon-β and FTY720 ameliorate progressive CNS inflammation via SOCS1-associated astrocyte signaling. Sci Rep 16, 9851 (2026). https://doi.org/10.1038/s41598-026-45303-9
Schlüsselwörter: progressive multiple Sklerose, Fingolimod, Interferon-Beta, Astrozyten, Neuroinflammation