Clear Sky Science · de
Kristallographische Daten für die Dolichylphosphat‑Mannose‑Synthase von Pyrococcus furiosus deuten darauf hin, dass das Enzym sein Glykolipid‑Produkt umschlagen könnte
Wie hitzeliebende Mikroben ihre Zellhüllen in Form halten
Viele Mikroben, die in kochend heißen Umgebungen gedeihen, überleben dank einer schützenden Zuckerschicht auf ihrer Zelloberfläche. Der Aufbau dieser Schicht erfordert spezielle Fett‑Zucker‑Moleküle, die auf einer Seite der Zellmembran gebildet und dann zur anderen Seite transportiert werden müssen. Diese Studie analysiert eines dieser Molekül‑herstellenden Enzyme aus einem hitzeliebenden Mikroben und legt nahe, dass erstaunlicherweise dasselbe Protein möglicherweise auch beim Umdrehen seines Produkts über die Membran hilft — es erfüllt also zwei Aufgaben zugleich.
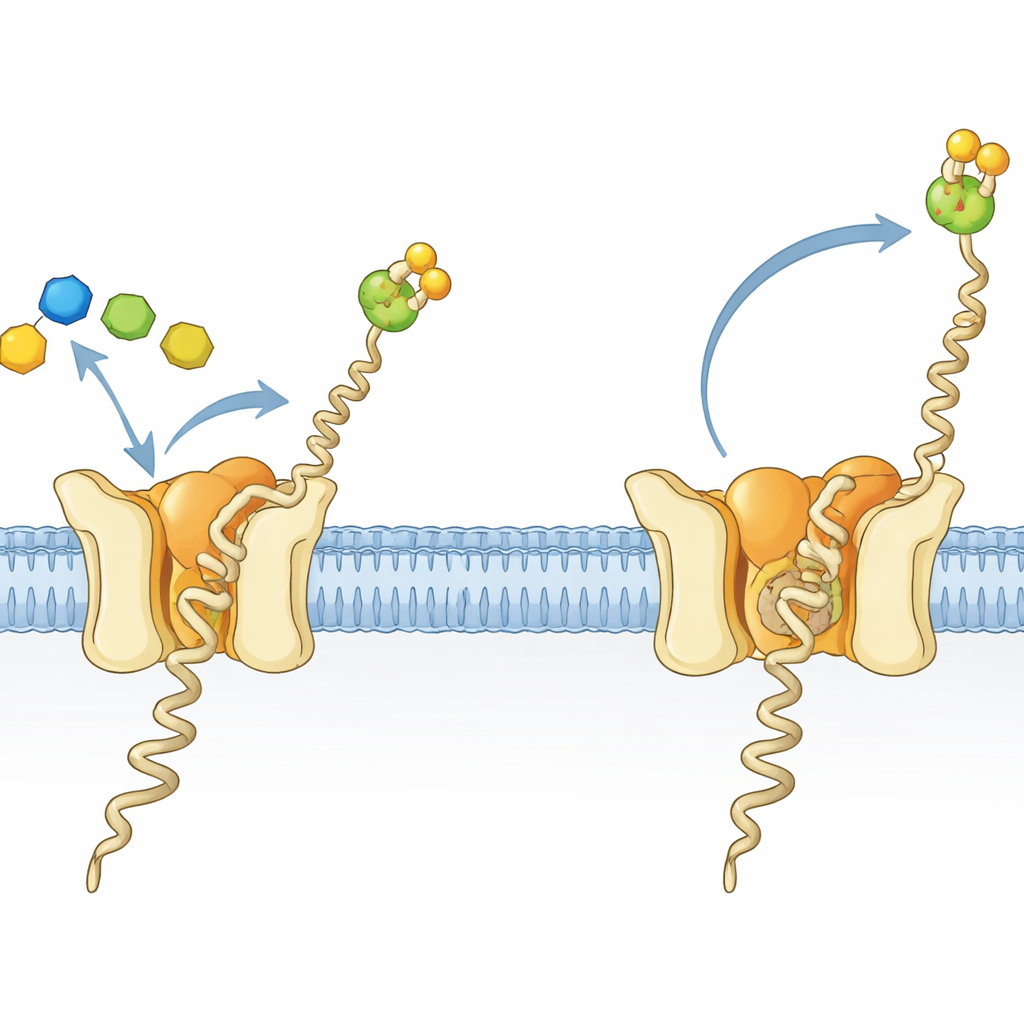
Eine winzige Fabrik für ein entscheidendes Zucker‑Fett‑Molekül
Zellen aller Lebensbereiche verzieren viele Proteine mit Zuckerketten, ein Prozess, der für korrektes Falten, Stabilität und Zell‑zu‑Zell‑Kommunikation unerlässlich ist. Bei Archaeen und Eukaryoten ist ein wichtiger Baustein für diese Modifikationen das Zucker‑Fett‑Molekül Dolichylphosphat‑Mannose (Dol‑P‑Man). Es besteht aus einem langen fettigen Schwanz, der in der Membran verankert ist, und einem Zucker‑Phosphat‑Kopf, der in die wässrige Umgebung herausragt. Dol‑P‑Man wird von der Dolichylphosphat‑Mannose‑Synthase (DPMS) hergestellt, die eine Mannose von einem löslichen Donor auf ein membrangebundenes Lipid überträgt. In dem hyperthermophilen Archaeon Pyrococcus furiosus ist DPMS ein Einkettenprotein, als Typ‑III‑DPMS bezeichnet, mit einem löslichen katalytischen Bereich, der an einen vierhelikalen, membrandurchspannenden Abschnitt angefügt ist, dessen Rolle bislang unklar war.
Das Enzym im Moment der Aktion einfangen
Die Forschenden kristallisierten die P. furiosus‑DPMS zusammen mit ihren Substraten und verfolgten die Reaktion mittels Röntgenkristallographie. Ihre neue Struktur, kombiniert mit drei früheren, fängt eine Serie von Schnappschüssen rund um den Moment der Zuckerübertragung ein. In einem Zustand sind das Donormolekül (GDP‑Mannose) und ein Dol‑P‑ähnlicher Akzeptor in einer präzisen Geometrie gebunden, die das reaktive Kohlenstoffatom der Mannose direkt vor der Phosphatgruppe von Dol‑P positioniert — eine ideale „Vor‑Transfer“‑Anordnung. Schleifen des Enzyms wirken wie Vorder‑ und Hintertüren: Sie schließen, um Donor und Metallion zu halten, und ordnen sich dann neu, um einen Weg für das Eindringen von Dol‑P zu öffnen und das verbrauchte GDP auszuschleusen, sobald die Mannose übertragen wurde. Diese Details klären, wie das Enzym eine effiziente und genaue Zuckerübertragung an der Membranoberfläche gewährleistet.
Ein kopfüber gelegenes Produkt in der Membran
Überraschender war ein zweiter, deutlich unterschiedlicher Zustand, der in denselben Kristallen gesehen wurde. Hier befindet sich das fertige Dol‑P‑Man nicht im aktiven Zentrum, sondern tiefer im membrandurchspannenden Teil des Proteins, in einer „kopfüber“ orientierten Lage. Sein Zucker‑Phosphat‑Kopf sitzt in einer polaren Tasche zwischen zwei Helixpaaren (TMD1 und TMD2), während der fettige Schwanz einer Rille folgt, die von den Helices gebildet wird. Eine entscheidende Aminosäure, ein Phenylalanin, scheint als Tor zu wirken, das den Zugang zu dieser Tasche entweder blockieren oder öffnen kann. Die Qualität der Elektronendichte und die Packungsweise des Proteins im Kristall sprechen dafür, dass dieses umgedrehte Dol‑P‑Man kein Kristallartefakt ist, sondern ein echter, gut besetzter Zustand, den das Enzym einnehmen kann.
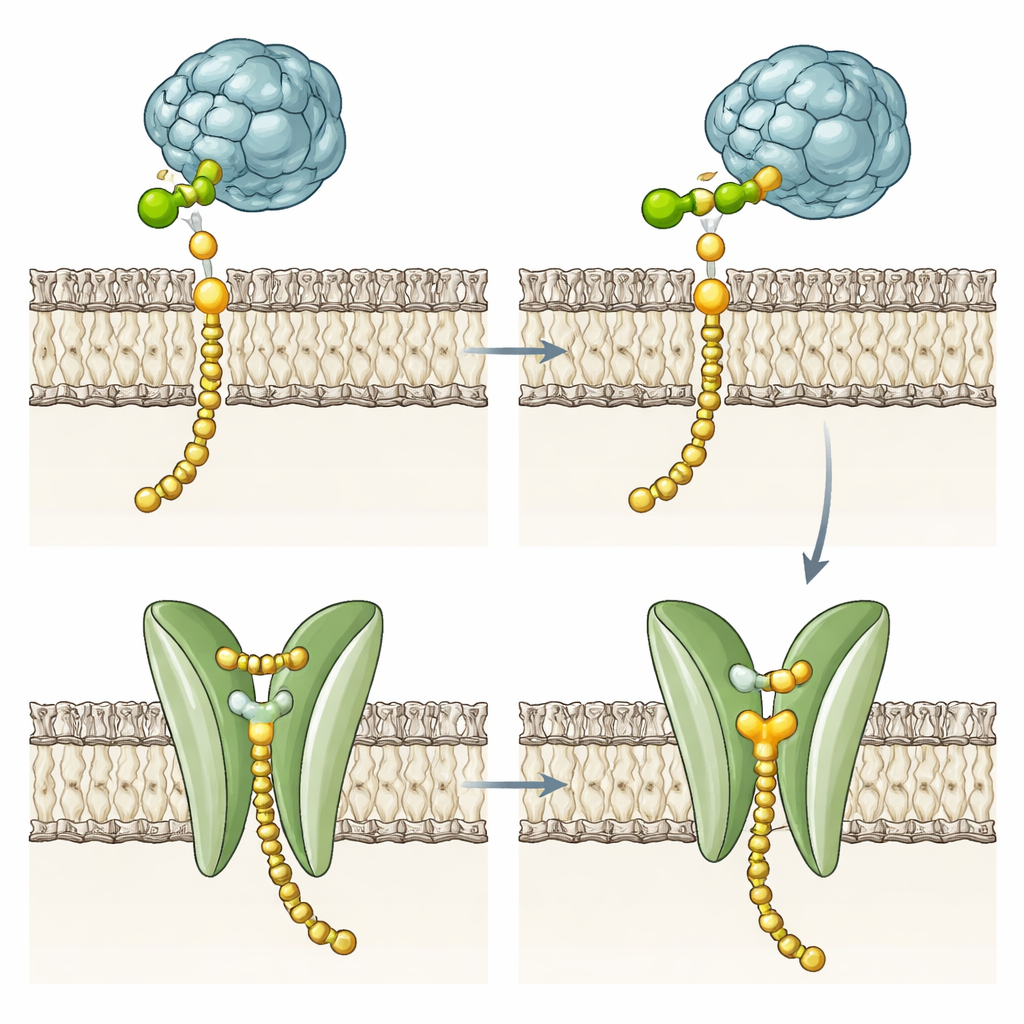
Mutanten deuten auf eine zweite Aufgabe hin
Um zu prüfen, ob die membrandurchspannende Domäne für die Zuckertransfer‑Chemie erforderlich ist, erzeugte das Team mehrere Varianten. Sie entfernten einen Großteil oder alle Helices, ersetzten sie durch ein anderes Membransektor von Hefen‑DPMS oder veränderten Schlüsselkavitäten‑Reste und das Phenylalanin‑Tor. Erstaunlicherweise stellten diese Mutanten Dol‑P‑Man mit ähnlichen Raten wie das intakte Enzym her, obwohl einige in der Membran etwas weniger stabil waren. Dies zeigt, dass die Kernchemie im löslichen katalytischen Bereich liegt und dass das vierhelikale Bündel nicht erforderlich ist, um Mannose an Dol‑P zu binden. Stattdessen deuten die konservierte polare Tasche, die Rille und das Gate‑Rest auf eine spezialisierte Rolle beim Umgang mit dem fertigen Produkt hin, insbesondere bei hyperthermophilen Archaeen, deren starre Membranen spontanes Lipid‑Umschlagen energetisch teuer machen.
Warum ein zweckentfremdendes Enzym wichtig ist
Setzt man die strukturellen und mutagenetischen Befunde zusammen, schlagen die Autoren vor, dass Typ‑III‑DPMS ein „Moonlighting“‑Protein ist. Zuerst synthetisiert es Dol‑P‑Man an der inneren Seite der archaealen Plasmamembran; dann könnte seine transmembrane Domäne helfen, das Zucker‑Fett‑Molekül umzuschlagen, sodass die Kopfgruppe an der Außenseite der Zelle erscheint und von anderen Enzymen weiterverarbeitet werden kann, die die Zuckerhülle der Zelle bauen. Die Evolution scheint dieses chimäre Design vor allem bei extrem hitzeliebenden Archaeen begünstigt zu haben, wo die Nähe des Syntheseorts zu einer dedizierten Flipping‑Rille Verschwendung und thermische Schäden minimieren könnte. Obwohl diese Arbeit die Flip‑Aktivität nicht direkt nachweist, liefert sie ein konkretes strukturelles Modell dafür, wie ein Enzym sowohl ein essentielles Lipidzwischenprodukt erzeugen als auch über eine harsche Membranbarriere neu positionieren kann.
Zitation: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
Schlüsselwörter: Dolichylphosphat Mannose, Lipid‑Flippase, Archaeen, Protein‑Glycosylierung, Membranenzyme