Clear Sky Science · de
Modellierung der Toxinenwirkung von Clostridioides difficile und des Schutzes durch Antiserum in einer immunkompetenten Intestine‑on‑Chip‑Plattform
Warum dieses Darminfektionsmodell wichtig ist
Antibiotika retten Leben, können den Darm aber auch anfällig für gefährliche Infektionen machen. Einer der schlimmsten Verursacher ist Clostridioides difficile, ein Bakterium, das insbesondere bei Krankenhauspatienten schwere Durchfälle und lebensgefährliche Entzündungen des Dickdarms auslösen kann. Diese Studie stellt ein kleines „Darm‑auf‑einem‑Chip“ vor, das zentrale Merkmale des menschlichen Darms nachbildet, einschließlich Blutgefäßen und Immunzellen, um in Echtzeit zu beobachten, wie C. difficile-Toxine den Darm schädigen und wie Antikörperbehandlungen diese Schäden verhindern könnten.
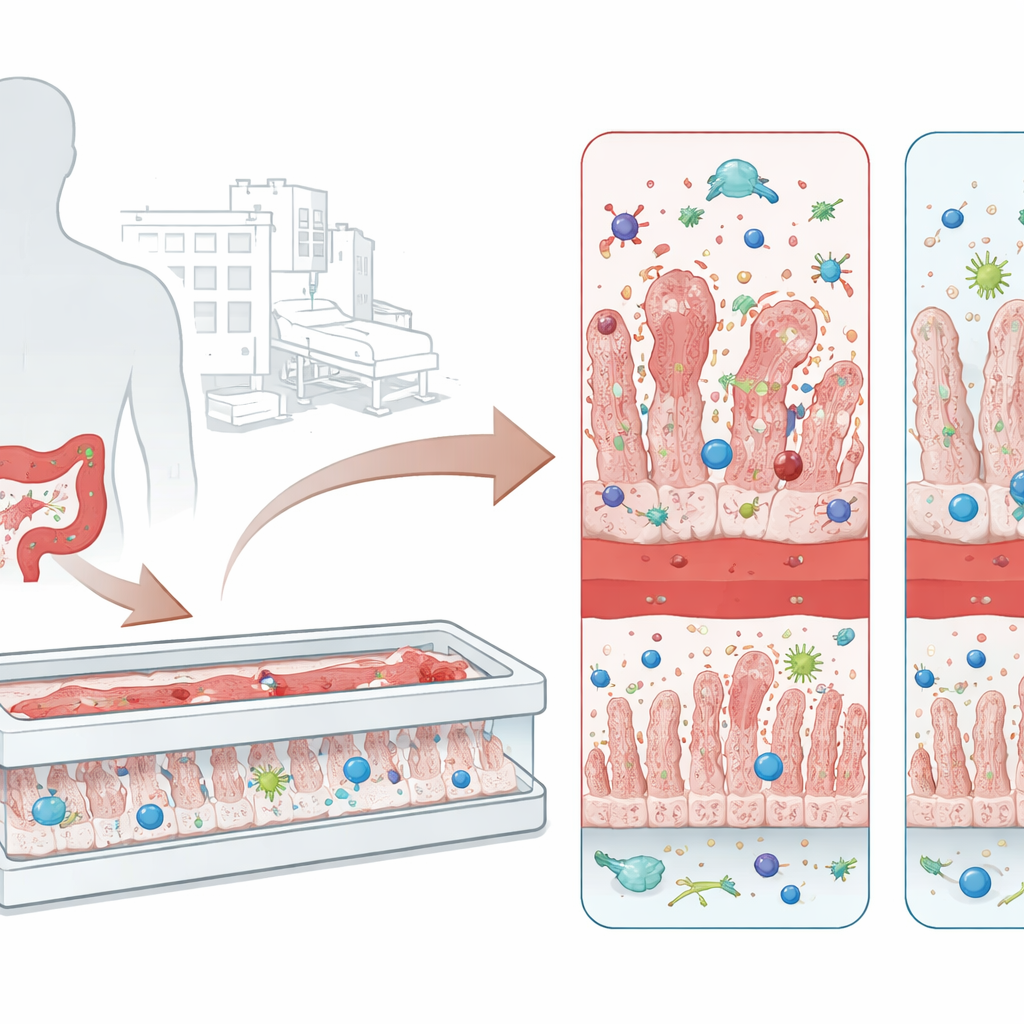
Vom hartnäckigen Krankenhauskeim zur Darmschädigung
C. difficile gedeiht bei Menschen, deren normale Darmflora gestört ist, häufig nach einer Behandlung mit Breitbandantibiotika. Der Erreger überdauert ungünstige Bedingungen als widerstandsfähige Sporen und setzt, einmal im Dickdarm etabliert, zwei Haupttoxine frei, bekannt als TcdA und TcdB. Diese Toxine greifen Darmzellen an, lösen die Verbindungen zwischen ihnen und lösen Entzündungsreaktionen aus. Das Spektrum reicht von lästigem Durchfall bis zur pseudomembranösen Kolitis, einer Erkrankung, bei der die Darmwand von abgetöteten Gewebeschichten und Immunzellen überzogen ist. Die derzeitigen Behandlungen beruhen hauptsächlich auf weiteren Antibiotika und gelegentlich auf Stuhltransplantationen; viele Patientinnen und Patienten erleiden jedoch wiederkehrende Infektionen, was den Bedarf an besseren Modellen zur Erforschung der Krankheit und zur Prüfung toxinblockierender Therapien unterstreicht.
Aufbau eines winzigen lebenden Darms auf einem Chip
Traditionelle Labormodelle kultivieren eine ebene Schicht von Darmzellen in einer Schale. Diese zweidimensionalen Kulturen sind zwar nützlich, haben aber keine Blutgefäße, keine Immunzellen und keinen sanften Flüssigkeitsfluss, die einen echten Darm prägen. Die Forschenden verwendeten stattdessen ein mikrotechnisch hergestelltes „Intestine‑on‑Chip“-Gerät mit zwei parallelen Kanälen, getrennt durch eine poröse Membran. Auf einer Seite wachsen Darmzellen aus und bilden fingerartige Rillen, die den Zotten ähneln, und eine dichte Barriere. Auf der gegenüberliegenden Seite liegen menschliche Gefäßzellen. In dieses Mini‑Gewebe wurden monocyten‑abgeleitete Makrophagen eingebracht, die sich in der Darmwand ansiedeln, sowie zirkulierende Neutrophile, die durch den Gefäßkanal wandern und ins Gewebe eindringen können, wodurch ein immunkompetenter Intestine‑on‑Chip (i‑IoC) entsteht, der den lebenden Darm realitätsnäher nachbildet.
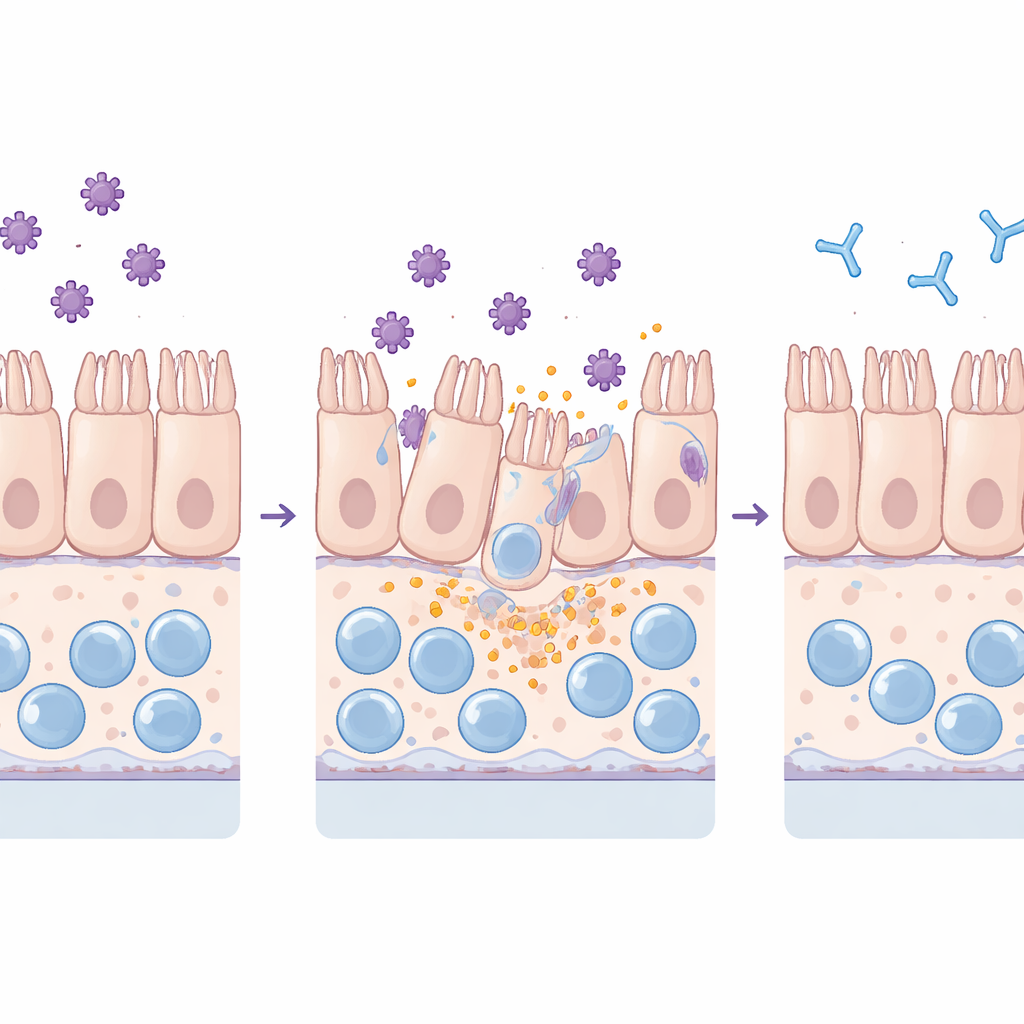
Beobachtung, wie Toxine die Barriere schädigen
Das Team setzte sowohl herkömmliche flache Kulturen als auch den komplexeren Chip gereinigten TcdA‑ und TcdB‑Toxinen aus. Sie überwachten, wie gut die Darmbarriere ein fluoreszierendes Farbstoffmolekül zurückhielt, untersuchten Verbindungsproteine, die benachbarte Zellen zusammenhalten, und maßen Entzündungsmoleküle sowie Marker für Zellschädigung in der umgebenden Flüssigkeit. Beide Toxine schädigten das Gewebe, jedoch auf unterschiedliche Weise: TcdA störte vor allem die dichten Verbindungen und ließ Zellen sich zusammenziehen, während TcdB zu einem großflächigen Verlust von Zellen aus der Schicht führte. Entscheidend war, dass der Chip diese Effekte bei deutlich geringeren Toxinmengen als die flachen Kulturen nachwies, was seine höhere Sensitivität und sein lebensechteres Verhalten unter kontinuierlichem Fluss widerspiegelt.
Immunzellen schüren die Reaktion — und können geschützt werden
Das Hinzufügen von Makrophagen und Neutrophilen zum Chip verstärkte die Reaktion auf die Toxine. Makrophagen förderten die Freisetzung wichtiger Entzündungsbotenstoffe wie IL‑6 und IL‑8, wurden dabei aber selbst reduziert, was mit einer entzündungsbedingten Form des Zelltods übereinstimmt. Neutrophile hefteten sich an die Gefäßwand und wanderten in das Darmgewebe ein, was dem Zustrom von Immunzellen bei Patientinnen und Patienten ähnelt. Längere Toxinexposition schädigte nicht nur die Darmschleimhaut, sondern schließlich auch die Gefäßschicht. Wenn die Forschenden die Toxine jedoch vorab mit toxinnneutralisierenden Antikörper‑Seren versetzten, waren strukturelle Schäden, Barrierelecks, Cytokinanstiege, Makrophagenverluste und Neutrophileninfiltrate deutlich reduziert. In länger angelegten Experimenten konnten sich durch TcdB geschädigte Gewebe teilweise erholen, sobald die Toxine entfernt wurden, während TcdA anhaltendere Schäden hinterließ, was auf unterschiedliche Reparaturkapazitäten nach den einzelnen Toxinen hindeutet.
Was das für Patientinnen, Patienten und Therapien bedeutet
Für eine allgemeine Leserschaft lautet die Kernbotschaft, dass dieses winzige lebende Darmmodell realistisch nachbilden kann, wie C. difficile-Toxine den Darm verletzen und das Immunsystem aktivieren, und zugleich zeigt, wie gut Antitoxin‑Antikörper das Gewebe schützen. Im Vergleich zu einfachen Zellschichten ist der Intestine‑on‑Chip empfindlicher, enthält Blutgefäße und Immunzellen und lässt sich über Tage betreiben, um sowohl frühe Schäden als auch Reparaturversuche zu erfassen. Das macht ihn zu einer vielversprechenden Testplattform für neuartige Behandlungen und Impfstoffe, die Toxine neutralisieren, ohne die Darmflora weiter zu stören, und potenziell zu einem Werkzeug, um Therapien künftig mit patienteneigenen Zellen zu personalisieren.
Zitation: Wegner, V.D., Warschinke, M., Brahim, I.B. et al. Modeling Clostridioides difficile toxin pathogenesis and antiserum protection in an immunocompetent intestine-on-chip platform. Sci Rep 16, 9233 (2026). https://doi.org/10.1038/s41598-026-44170-8
Schlüsselwörter: Clostridioides difficile, intestine-on-chip, Darminfektion, neutralisierende Antikörper, Organ‑on‑Chip‑Modelle