Clear Sky Science · de
Fehlen des Luciferase-Gens im Genom des kleptoprotein-biolumineszenten Fisches Parapriacanthus ransonneti
Fische, die ihr Leuchten stehlen
Wenn wir an leuchtende Tiere denken, stellen wir uns meist Lebewesen vor, die ihr eigenes Licht mit speziellen Genen erzeugen. Diese Studie kehrt diese Vorstellung um. Der kleine Riff-Fisch Parapriacanthus ransonneti leuchtet im Dunkeln, trägt aber offenbar nicht das genetische Rezept für sein Lichtproduktionswerkzeug; stattdessen scheint er das fertige Protein von den winzigen Krebstieren zu entlehnen, die er frisst. Aus dieser Arbeit kann ein nicht spezialisiertes Publikum nachvollziehen, wie flexibel das Leben sein kann — und wie die Evolution manchmal „nutze es, statt es herzustellen“ als erfolgreiche Strategie wählt.
Geliehenes Licht von winziger Beute
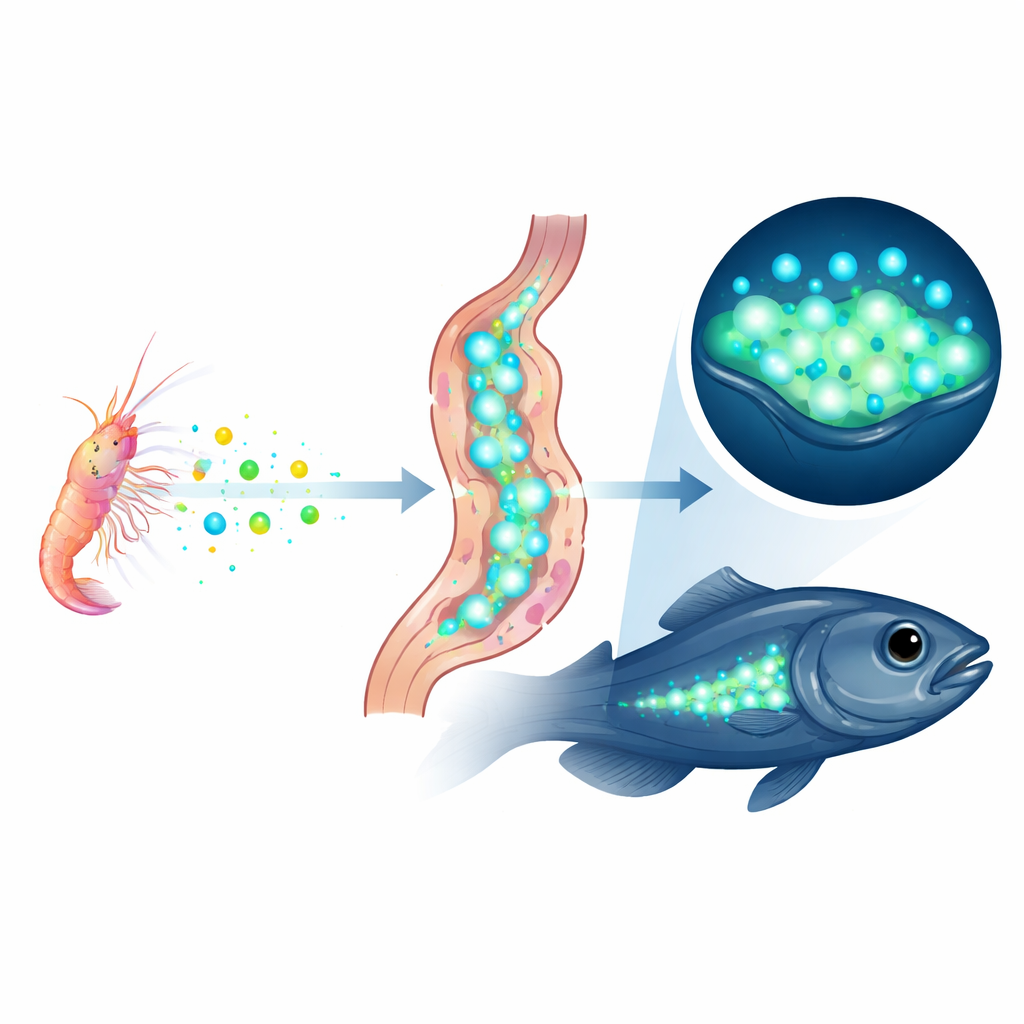
Wissenschaftler wussten bereits, dass dieser Fisch mit demselben lichtproduzierenden Protein, der sogenannten Luciferase, leuchtet wie ein biolumineszenter Ostracode, ein winziges planktonisches Krebstier. Frühere Untersuchungen zeigten, dass das Luciferase-Protein im Fisch exakt mit der Ostracoden-Version übereinstimmt und dass die Fische ihr Leuchten verlieren, wenn sie monatelang ohne leuchtende Beute gehalten werden. Werden sie mit einem anderen leuchtenden Ostracoden gefüttert, ersetzt dieses den Proteinbestand in den Lichtorganen des Fisches durch das neue Protein. Diese Hinweise legten nahe, dass die Fische Luciferase nicht selbst herstellen, sondern sie aus ihrer Nahrung ansammeln — ein Prozess, den die Autoren „Kleptoproteinismus“ nennen, wörtlich Proteindiebstahl. Dennoch war es möglich, dass versteckte Luciferase-Gene im Fischgenom lauerten, die frühere Methoden übersehen hatten.

Das genetische Bauplan des Fisches lesen
Um die Frage zu klären, erstellten die Forscher einen hochwertigen genetischen Bauplan bzw. ein Genom für Parapriacanthus ransonneti. Sie züchteten die Fische sorgfältig über mehr als ein Jahr mit nicht leuchtender Nahrung, um Kontaminationen durch Beute-DNA zu vermeiden, und extrahierten dann die eigene DNA der Fische und sequenzierten sie mit moderner Langread-Technologie. Das zusammengesetzte Genom war etwa 625 Millionen „Buchstaben“ lang, entsprach unabhängigen Größenschätzungen und wies sehr wenige Lücken auf. Anschließend sagten sie zehntausende Gene voraus und überprüften die Gesamtqualität mit gängigen Benchmarks, was bestätigte, dass nahezu alle erwarteten Fischgene vorhanden waren. Mit anderen Worten: Dies war eine solide, nahezu vollständige Karte, auf der ein Luciferase-Gen, falls vorhanden, sichtbar hätte sein müssen.
Auf der Jagd nach einem fehlenden Gen
Mit diesem Genom ging das Team auf eine gezielte Schatzsuche. Sie verglichen bekannte Luciferase-Sequenzen mehrerer leuchtender Ostracoden mit den vorhergesagten Proteinen des Fisches, seinen zusammengesetzten Chromosomen und sogar den rohen, unzusammengesetzten DNA-Reads. Mehrere Suchwerkzeuge mit unterschiedlichen Stärken wurden eingesetzt, um blinde Flecken zu vermeiden. Wiederholt tauchte kein echter Luciferase-Treffer auf. Einige Fischgene wirkten entfernt ähnlich, aber eine genauere Untersuchung ergab, dass sie zu einer verbreiteten Familie immunbezogener Proteine gehören, nicht zu lichtbildenden Enzymen, und ihre Evolutionsbäume passten zur normalen Fischgeschichte statt zu einem Signal jüngeren Transfers von Krebstieren. Das Fehlen von Luciferase nicht nur im ausgefeilten Genom, sondern auch in den rohen Sequenzdaten macht es äußerst unwahrscheinlich, dass das Gen einfach in einer unzusammengesetzten Ecke versteckt ist.
Suche nach anderen genetischen Abkürzungen
Die Wissenschaftler fragten außerdem, ob der Fisch vielleicht stillschweigend andere nützliche Gene von Ostracoden übernommen haben könnte, etwa solche, die mit der Handhabung der lichtproduzierenden Chemikalie Luciferin zu tun haben. Mit schnellen, groß angelegten Vergleichsverfahren durchsuchten sie jedes vorhergesagte Fischprotein gegen Datenbanken von Fisch- und Ostracodenproteinen und markierten Fälle, in denen ein Fischgen einem Ostracodengen stärker ähnelte als den Genen anderer Fische. Etwa zwanzig solche Kandidaten tauchten auf, aber detaillierte evolutionäre Stammbäume zeigten, dass diese Gene weiterhin fest mit Fischen gruppierten und nicht innerhalb von Ostracoden-Zweigen lagen. Kurz: Es gab kein überzeugendes Anzeichen dafür, dass irgendwelche Gene, einschließlich solcher, die Luciferin verarbeiten, seitlich von Krebstieren in die DNA dieses Fisches gesprungen sind.
Eine neue Art zu leuchten
Zusammengefasst deutet die Evidenz auf eine eindrückliche Schlussfolgerung hin: Parapriacanthus ransonneti leuchtet, ohne die genetischen Anweisungen für sein wichtiges lichtbildendes Enzym zu besitzen. Stattdessen fängt es fertige Luciferase-Proteine aus den Ostracoden, die es frisst, ein und speichert sie in seinen Lichtorganen — ein lebendiges Beispiel für „Du bist, was du isst“ auf molekularer Ebene. Das zeigt, dass Tiere komplexe Fähigkeiten nicht nur durch Evolution oder Import neuer Gene erwerben können, sondern auch, indem sie funktionierende Bauteile anderer Arten direkt wiederverwenden. Das neu zusammengesetzte Genom bietet nun eine Grundlage für weitere Arbeiten, um zu klären, wie der Fisch diese gestohlenen Proteine sicher transportiert, schützt und steuert — und wie oft die Natur ähnliche Tricks bei anderen leuchtenden Lebewesen anwendet.
Zitation: Bessho-Uehara, M., Yamaguchi, K., Koeda, K. et al. Absence of the luciferase gene in the genome of the kleptoprotein bioluminescent fish Parapriacanthus ransonneti. Sci Rep 16, 9211 (2026). https://doi.org/10.1038/s41598-026-43942-6
Schlüsselwörter: biolumineszenter Fisch, Proteinakkumulation, Kleptobiologie, Luciferase, Genomsequenzierung