Clear Sky Science · de
Etikettenfreie Mehrphotonenmikroskopie und maschinelles Lernen zur Erkennung von hepatozellulärem Karzinom
Warum das für Menschen mit Leberkrebs wichtig ist
Leberkrebs, insbesondere das hepatozelluläre Karzinom, ist weit verbreitet und oft tödlich; die Operation ist häufig die einzige Chance auf Heilung. Während einer Operation müssen Chirurgen den gesamten Tumor entfernen und gleichzeitig so viel gesundes Lebergewebe wie möglich erhalten — ein schwieriger Balanceakt, weil krankes Lebergewebe bereits abnormal aussehen kann. Diese Studie untersucht eine neue Methode, um Krebs in Echtzeit während der Operation sichtbar zu machen, ohne Farbstoffe oder langwierige Laboruntersuchungen, indem fortschrittliche Lasermikroskopie mit künstlicher Intelligenz kombiniert wird. Ziel ist es, Chirurgen zu helfen, den tatsächlichen Tumorrand schneller und genauer zu finden und so möglicherweise die Ergebnisse für Patientinnen und Patienten zu verbessern.
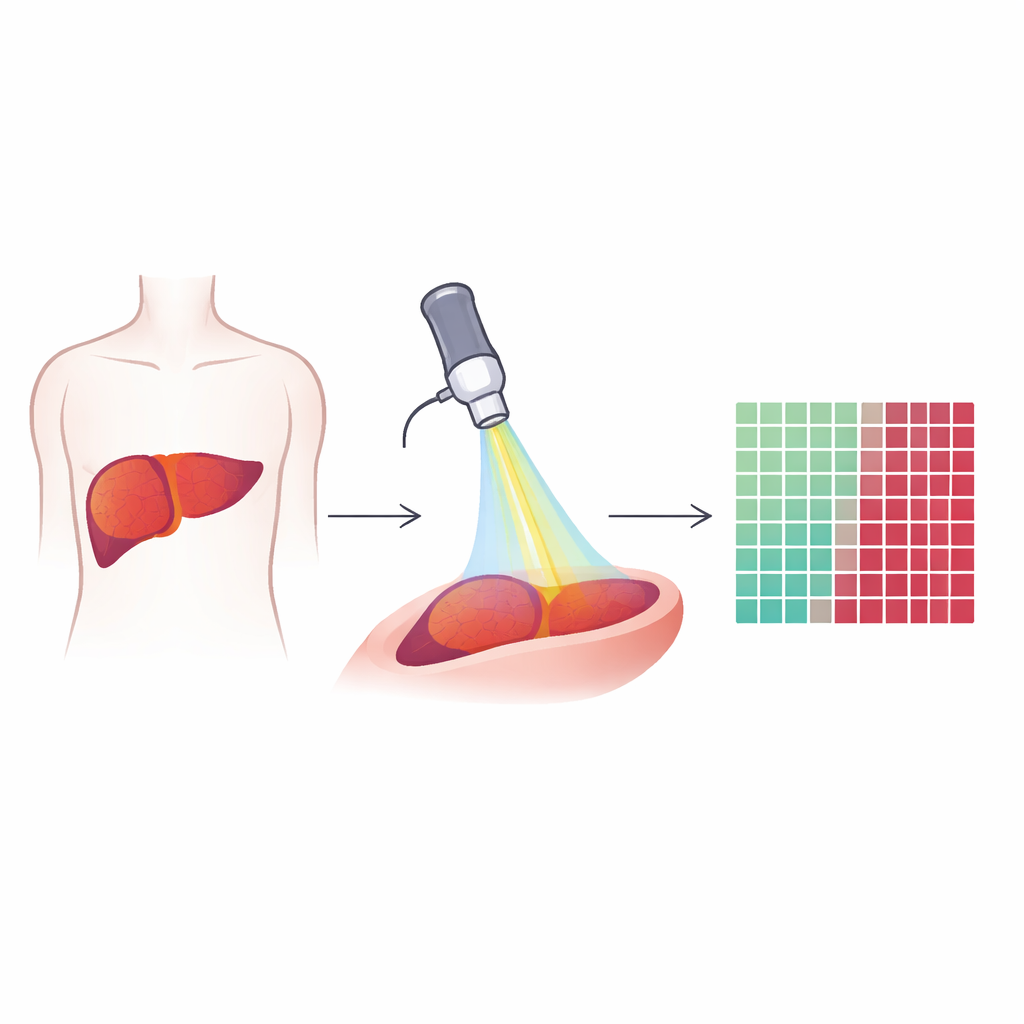
Ins Gewebe blicken mit speziellem Licht
Die Forschenden nutzten eine Technik namens Mehrphotonenmikroskopie, die sehr kurze Laserpulse verwendet, damit natürliche Moleküle im Gewebe aufleuchten oder Signale erzeugen. Anstatt Farbstoffe oder Kontrastmittel zuzugeben, liest die Methode das aus, was bereits vorhanden ist: Fette, Kollagenfasern und natürlich fluoreszierende Substanzen in Zellen. Aus jedem winzigen Sichtfeld in Leberproben wurden drei Signalarten aufgezeichnet: eines, das Lipide hervorhebt, eines, das Autofluoreszenz von Molekülen wie NADH und Vitamin A zeigt, und eines, das steife Kollagenfasern sichtbar macht. Zusammen erzeugen diese Signale bunte, hochaufgelöste Bilder, die sowohl einzelne Zellen als auch die Gesamtarchitektur von Lebergewebe und Tumoren zeigen.
Die vielen Gesichter des Leberkrebses erfassen
Das Team untersuchte Gewebe von 76 Patientinnen und Patienten, die wegen Leberkrebs operiert wurden, und betrachtete sowohl den Tumor als auch die umgebende Leber. Sie zeigten, dass diese etikettenfreie Bildgebung klassische Wachstumsformen des hepatozellulären Karzinoms darstellen kann, etwa dünne oder dicke Zellplatten, solide Bezirke und drüsenartige Strukturen. Sie macht auch Veränderungen in der umgebenden Leber sichtbar, darunter Fettansammlungen und Narbenbildung, die bei chronischen Leberkrankheiten häufig sind. Wichtig ist, dass diese Muster selbst bei vergleichsweise niedriger Auflösung erkennbar waren — ähnlich der Auflösung, die künftige endoskopische Geräte im Körper liefern könnten. Das deutet darauf hin, dass der Ansatz nicht nur im Labor, sondern auch im Operationssaal praktisch einsetzbar sein könnte.
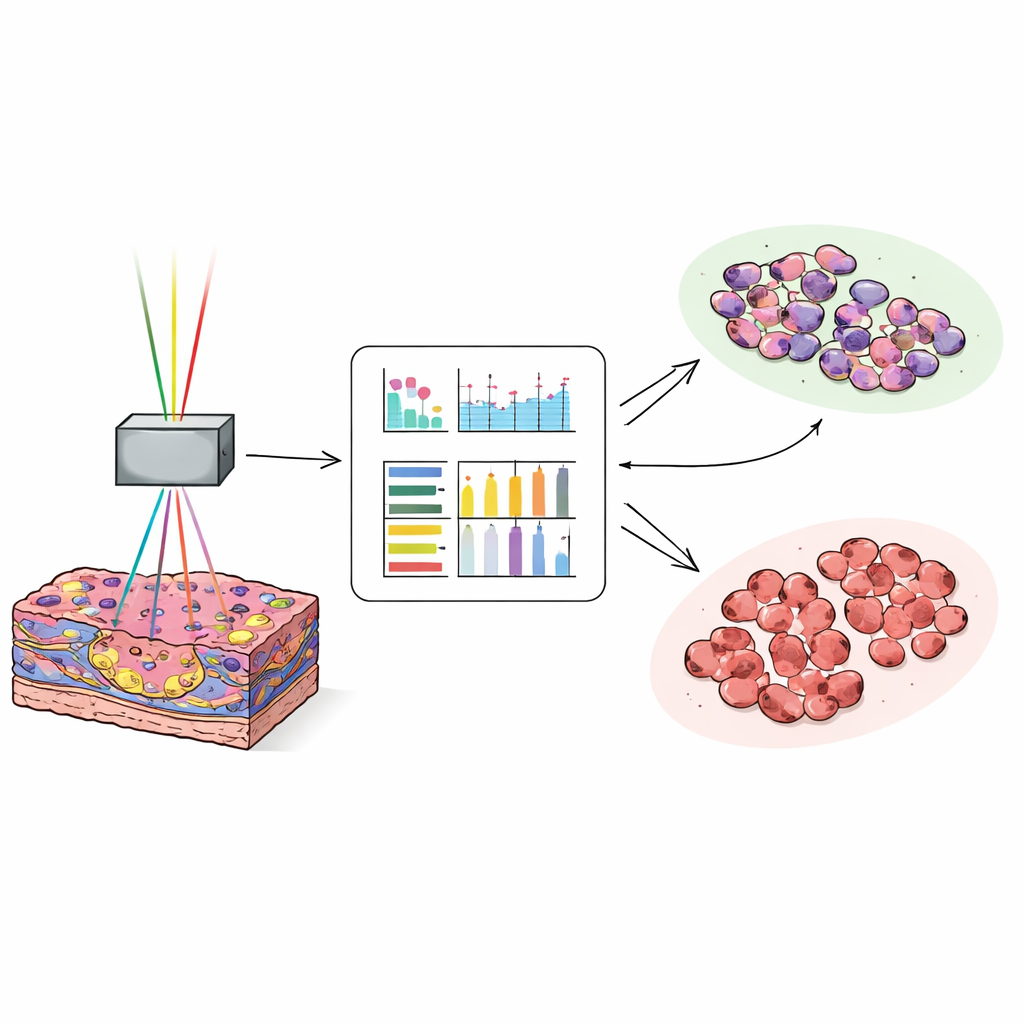
Dem Computer beibringen, den Tumorrand zu erkennen
Um die reichen, aber komplexen Bilder in schnelle Entscheidungen zu überführen, wandelten die Wissenschaftlerinnen und Wissenschaftler jedes Bild in Zahlen um, die Textur beschreiben — etwa wie glatt, grob oder abwechslungsreich die Pixelmuster sind. Für jeden Bildkanal berechneten sie 17 solcher Messgrößen und trainierten dann ein neuronales Netzwerk mit etwa 25.000 Bildern von 35 Patientinnen und Patienten, um Tumorgewebe von nicht-krebserregender Leber zu unterscheiden. Anschließend testeten sie das Modell an rund 27.000 neuen Bildern von weiteren 38 Patientinnen und Patienten. Wenn der Computer die Kombination aus Autofluoreszenz- und Kollagen-empfindlichen Signalen nutzte, klassifizierte er Bilder in etwa 97 von 100 Fällen korrekt als Tumor oder normal. Selbst die subtilsten, gut differenzierten Tumoren, die bei schnellen Gefrierschnitten für Pathologen schwer zu erkennen sein können, wurden mit hoher Genauigkeit eingeordnet.
Was die Lichtmuster über den Krebs verraten
Im Vergleich verschiedener Signal-Kombinationen zeigte die Studie, dass die Autofluoreszenz die nützlichsten Informationen zur Unterscheidung von Krebs und Nicht-Krebs liefert. Dieses Leuchten stammt von vielen natürlichen Molekülen in Zellen und von Strukturen wie Elastin und Kollagen und enthält daher Hinweise auf Zelldichte, Kerngröße und -form (als dunklere Bereiche sichtbar), Fetttröpfchen und die Zusammensetzung des umgebenden Gewebes. Das Hinzuziehen des kollagen-spezifischen Signals schärfte den Kontrast zwischen Tumor und Leber weiter, was bekannte Unterschiede in der Anordnung von Fasern und Blutgefäßen widerspiegelt. Überraschenderweise trug das lipidfokussierte Signal weniger zur automatischen Klassifikation bei — ein praktischer Befund, da dies einfachere Gerätedesigns ermöglichen könnte, die nur einen Laserstrahl statt komplexerer Zwei-Strahl-Systeme benötigen.
Vom Labortisch in den Operationssaal
Um die reale chirurgische Anwendung zu simulieren, wandte das Team sein bestes Modell auch auf Gewebeproben an, die die tatsächliche Grenze zwischen Tumor und Leber enthielten, und erzeugte Wahrscheinlichkeitskarten, die zeigten, wo der Krebs endet und normales Gewebe beginnt. Diese Karten stimmten größtenteils gut mit herkömmlicher Histologie überein, wenngleich stark fettige oder kollagenreiche Bereiche den Klassifikator gelegentlich verwirrten. Die Autorinnen und Autoren nennen weiterhin bestehende Hürden, bevor diese Technologie bei lebenden Operationen anleiten kann, darunter die begrenzte Eindringtiefe der optischen Bildgebung, die Notwendigkeit robuster, steriler Endoskope, Bewegung und Blut im Operationsfeld sowie die Herausforderung, künstliche Intelligenz an großen, realen Datensätzen zu validieren. Dennoch zeigt die Arbeit, dass etikettenfreie Mehrphotonenbildgebung in Kombination mit maschinellem Lernen wie ein schnelles, digitales Mikroskop wirken kann, das künftig Chirurgen helfen könnte, präziser und sicherer zu schneiden und so die Chancen erhöht, den gesamten Krebs zu entfernen und gleichzeitig so viel gesundes Lebergewebe wie möglich zu erhalten.
Zitation: Galli, R., Korn, S., Aust, D. et al. Label-free multiphoton microscopy and machine learning for recognition of hepatocellular carcinoma. Sci Rep 16, 8734 (2026). https://doi.org/10.1038/s41598-026-43831-y
Schlüsselwörter: Leberkrebs-Bildgebung, Mehrphotonenmikroskopie, Autofluoreszenz, Operationsränder, maschinelles Lernen