Clear Sky Science · de
Natürliche genetische Variation beeinflusst die komplementinhibitorische Aktivität von PFam54-Orthologen von asiatischem Borrelia bavariensis
Warum das für die Lyme-Borreliose wichtig ist
Die Lyme-Borreliose ist bereits die häufigste durch Zecken übertragene Erkrankung auf der Nordhalbkugel, doch nicht alle Lyme-erzeugenden Bakterien verhalten sich im Körper gleich. Diese Studie untersucht Borrelia bavariensis, einen nahen Verwandten des Hauptverursachers, und stellt eine einfache Frage mit weitreichenden Folgen: Verändern natürliche genetische Unterschiede zwischen asiatischen und europäischen Stämmen, wie gut diese Bakterien eine unserer ersten Abwehrlinien—das Komplementsystem im Blut—umgehen? Die Antwort hilft zu erklären, wie sich diese Mikroben ausbreiten, wie sie Krankheiten verursachen und wo wir zukünftige Therapien oder Impfstoffe ansetzen könnten.
Eine Geschichte von zwei Kontinenten
Borrelia bavariensis zirkuliert zwischen Kleintieren und Zecken in Eurasien und kann beim Menschen Lyme-Borreliose auslösen. Europäische Stämme zeigen häufig eine starke Präferenz für das Nervensystem und treten in Fällen von Neuroborreliose auf, während asiatische Stämme weniger mit Hirn‑ und Nerveninfektionen verknüpft zu sein scheinen. Genetische Untersuchungen legen nahe, dass die europäischen Stämme von einem vielfältigeren asiatischen Vorfahren abstammen und bei der Anpassung an eine andere Zeckenart in Europa einen Flaschenhals durchlaufen haben. Dieser evolutionäre Umweg könnte Teile des bakteriellen Genoms umgestaltet haben, einschließlich eines Genclusters namens PFam54 auf einem Plasmid namens lp54. Viele PFam54-Gene kodieren für Oberflächenproteine, die den Bakterien helfen, im Blut zu überleben, indem sie das Komplementsystem stören—ein Proteinnetzwerk, das eindringende Zellen zerstören kann.
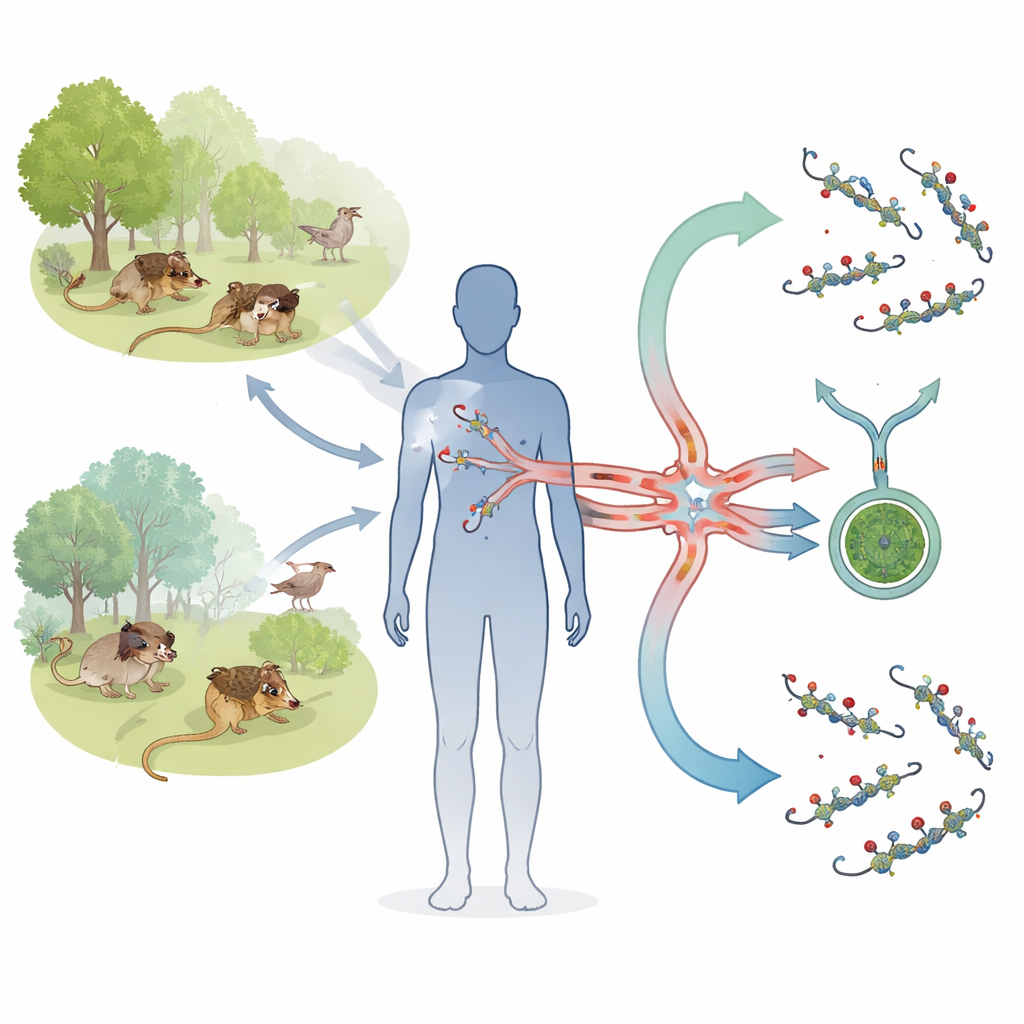
Wie die Bakterien dem Angriff im Blut entkommen
Man kann sich das Komplementsystem als molekularen Alarm vorstellen, der—einmal ausgelöst—in der Bildung eines „Membranangriffskomplexes“ (MAC) endet, der Poren in bakterielle Membranen bohrt. Frühere Arbeiten an einem europäischen Referenzstamm zeigten, dass zwei PFam54-Proteine, BGA66 und BGA71, auf der Bakterienoberfläche sitzen und an späte Komplementkomponenten (C7, C8, C9) binden, wodurch die Assemblierung dieses terminalen Porenkomplexes blockiert wird. Asiatische B. bavariensis‑Stämme tragen jedoch oft eine andere Zusammenstellung von PFam54‑Genen, und einige fehlen sogar die exakt gleichen BGA66‑ und BGA71‑Gene wie in Europa. Die Forscher fragten, ob diese asiatischen Varianten weiterhin als Komplementschilde funktionieren und ob neue, nur in Asien vorkommende PFam54‑Familienmitglieder alternativen Schutz bieten könnten.
Vielfalt mit Genetik und Struktur untersuchen
Das Team durchkämmte zunächst PFam54‑Gene in Dutzenden asiatischer und europäischer B. bavariensis‑Genome. Wie zu erwarten, zeigten asiatische Stämme mehr Sequenzvielfalt in dieser Familie, doch die Gesamtmuster deuteten darauf hin, dass die Proteine weiterhin einem Selektionsdruck unterliegen, ihre Grundfunktion zu bewahren. Mit AlphaFold zur Vorhersage von 3D‑Strukturen stellten sie fest, dass die asiatischen Versionen von BGA66 und BGA71 sowie mehrere verwandte Proteine trotz zahlreicher Aminosäureänderungen alle sehr ähnliche, vollständig helikale Formen annahmen. Diese Mutationen konzentrierten sich tendenziell an oberflächenexponierten Regionen—genau dort, wo Wechselwirkungen mit dem Komplement stattfinden würden—was darauf hindeutet, dass eher eine Feineinstellung der Bindung als ein vollständiger Funktionsverlust evolutionär entstanden sein könnte.
Die Proteine auf die Probe stellen
Um zu sehen, was diese Unterschiede praktisch bedeuten, exprimierten die Forscher asiatische PFam54‑Proteine in Bakterien und testeten sie in humanem Serum. Zwei japanische B. bavariensis‑Isolate, NT24 und JHM1114, erwiesen sich als hochresistent gegen das Abtöten durch aktives menschliches Komplement, ähnlich dem europäischen Typstamm. Rein isolierte Proteine aus diesen Stämmen wurden dann in kontrollierten Assays mit menschlichen Komplementkomponenten gemischt. Asiatisches BGA66 konnte die Bildung des Membranangriffskomplexes weiterhin blockieren, wenn auch weniger effizient als sein europäisches Gegenstück. Eine asiatische BGA71‑Variante beeinträchtigte einen späten Schritt des Weges teilweise, benötigte aber höhere Dosen, um eine Wirkung zu zeigen. Auffällig war ein neues, nur in Asien vorkommendes Protein, BGA67b, das den terminalen Weg stark hemmte, ohne direkt die Polymerisation von C9 zu blockieren, was auf eine andere Art der Verhinderung der Porenbildung hindeutet. Wenn diese PFam54‑Proteine auf der Oberfläche eines ansonsten komplementempfindlichen Surrogatstamms produziert wurden, machten sie diesen Stamm serumresistent und bestätigten damit ihre schützende Rolle.
Was das für Patienten und zukünftige Forschung bedeutet
Vereinfacht gesagt zeigt diese Arbeit, dass sowohl asiatische als auch europäische B. bavariensis‑Stämme mit effektiven molekularen „Schilden“ ausgestattet sind, die sie davor schützen, durch das Komplementsystem im Blut aufgerissen zu werden. Die spezifischen Schutzproteine und ihre Wirkstärken unterscheiden sich, doch die übergeordnete Strategie—spät in der Angriffssequenz einzugreifen, um die Porenbildung zu verhindern—ist über die Kontinente hinweg erhalten geblieben. Das bedeutet, dass die Komplement‑Evasion durch PFam54‑Proteine allein nicht erklärt, warum europäische Stämme häufiger mit Erkrankungen des Nervensystems in Verbindung stehen. Weitere Faktoren, wie zusätzliche Oberflächenproteine, Mechanismen der Gewebe‑Targetierung oder Unterschiede in Wirts‑ oder Zeckenökologie, müssen eine Rolle spielen. Gleichzeitig hebt die Studie eine kleine Gruppe konservierter Proteinformen und Interaktionsflächen hervor, die für das bakterielle Überleben im Blut entscheidend sind und sie als vielversprechende Ziele für Wirkstoffe oder Impfstoffe auswies, die die Bakterien für die angeborene Immunabwehr enttarnen sollen.
Zitation: Langhoff, L., Kapfer, P., Röttgerding, F. et al. Natural genetic variation impacts complement inhibitory activity of PFam54 orthologs of Asian Borrelia bavariensis. Sci Rep 16, 9080 (2026). https://doi.org/10.1038/s41598-026-43598-2
Schlüsselwörter: Lyme-Borreliose, Borrelia bavariensis, Komplementsystem, Immunevasion, PFam54-Proteine