Clear Sky Science · de
Stratifizierung nach Verschreibungsdosis verbessert die tiefenlernbasierte VMAT‑Dosisvorhersage bei lokal fortgeschrittenem NSCLC
Warum klügere Bestrahlungspläne wichtig sind
Wenn Ärztinnen und Ärzte fortgeschrittenen Lungenkrebs mit Strahlung behandeln, balancieren sie sorgsam: genügend Energie, um den Tumor zu kontrollieren, bei gleichzeitiger Schonung empfindlicher Nachbarorgane. Die Erstellung dieser Pläne ist langsam, komplex und stark von der Erfahrung des Planers abhängig. Diese Studie untersucht, wie künstliche Intelligenz das Dosismuster im Brustkorb vorhersagen kann, und zeigt vor allem, dass das Training der KI mit sorgfältig gruppierten Dosisniveaus ihre Vorhersagen genauer und klinisch nützlicher macht.
Wie Lungenkrebs mit fokussierten Strahlen behandelt wird
Die meisten Menschen mit lokal fortgeschrittenem nicht‑kleinzelligem Lungenkrebs kommen nicht für eine operative Entfernung des Tumors in Frage. Stattdessen erhalten sie häufig Chemotherapie zusammen mit stark geformten Strahlenbündeln, die in Bögen um den Brustkorb fahren — eine Technik, die als VMAT bekannt ist. Ziel ist es, den Tumor mit einer hohen, gleichmäßigen Dosis zu versehen und dabei die Exposition von Lungen, Herz, Speiseröhre und Rückenmark zu begrenzen. Dieses Gleichgewicht erfordert meist mehrere Durchläufe mit Trial‑and‑Error‑Anpassungen, was Zeit kostet und Behandlungsentscheidungen verzögern kann. Könnten Ärztinnen und Ärzte schnell abschätzen, welches Dosismuster für einen bestimmten Patienten realistisch erreichbar ist, könnten sie früher die beste Behandlungsstrategie wählen.
Ein Algorithmus lernt, Dosismuster zu erkennen
Die Forschenden wandten sich dem Tiefenlernen zu, einer Form der KI, die Muster direkt aus Bildern erlernt. Sie sammelten CT‑Scans und fertige Behandlungspläne von 72 Lungenkrebspatienten, die mit VMAT behandelt wurden. Für jede Person berechneten sie neu, wie dasselbe Strahlenarrangement drei verschiedene Gesamtdosen liefern würde: 50, 54 und 60 Gray (Gy), die standardmäßigen Einheiten für Strahlung. Jeder Fall wurde in ein dreidimensionales Gitter überführt, das den Tumor, wichtige Organe und das zugrundeliegende CT‑Bild markierte. Diese neun Informationskanäle wurden einem 3D‑U‑Net zugeführt, einem gebräuchlichen neuronalen Netzdesign, das lernen kann, wie Dosis anhand der Anatomie durch den Körper fließt.
Warum die Gruppierung nach Verordnungsdosis wichtig ist
Eine zentrale Frage war, wie mit der Tatsache umzugehen ist, dass Patientinnen und Patienten unterschiedliche Gesamtdosen verordnet bekommen. Das Team erstellte vier ansonsten identische KI‑Modelle. Drei davon waren „Einzel‑Verordnungsdosis“-Modelle, die jeweils nur mit Plänen einer Dosisstufe (50, 54 bzw. 60 Gy) trainiert wurden. Das vierte Modell mischte 50‑ und 60‑Gy‑Fälle, ohne dem Netz mitzuteilen, welche Verordnung es gerade sah. Beim Testen an neuen Patienten passten die verordnungsspezifischen Modelle besser an die tatsächliche Dosis im Tumor, wobei sowohl die Abdeckung als auch Hot‑Spots dicht an den klinischen Plänen blieben — typischerweise innerhalb weniger Gy. Im Gegensatz dazu machte das gemischte Modell spürbar größere Fehler in den höchsten Dosisregionen des Tumors und rund um das Rückenmark, wo die Dosis streng unter Sicherheitsgrenzen bleiben muss.
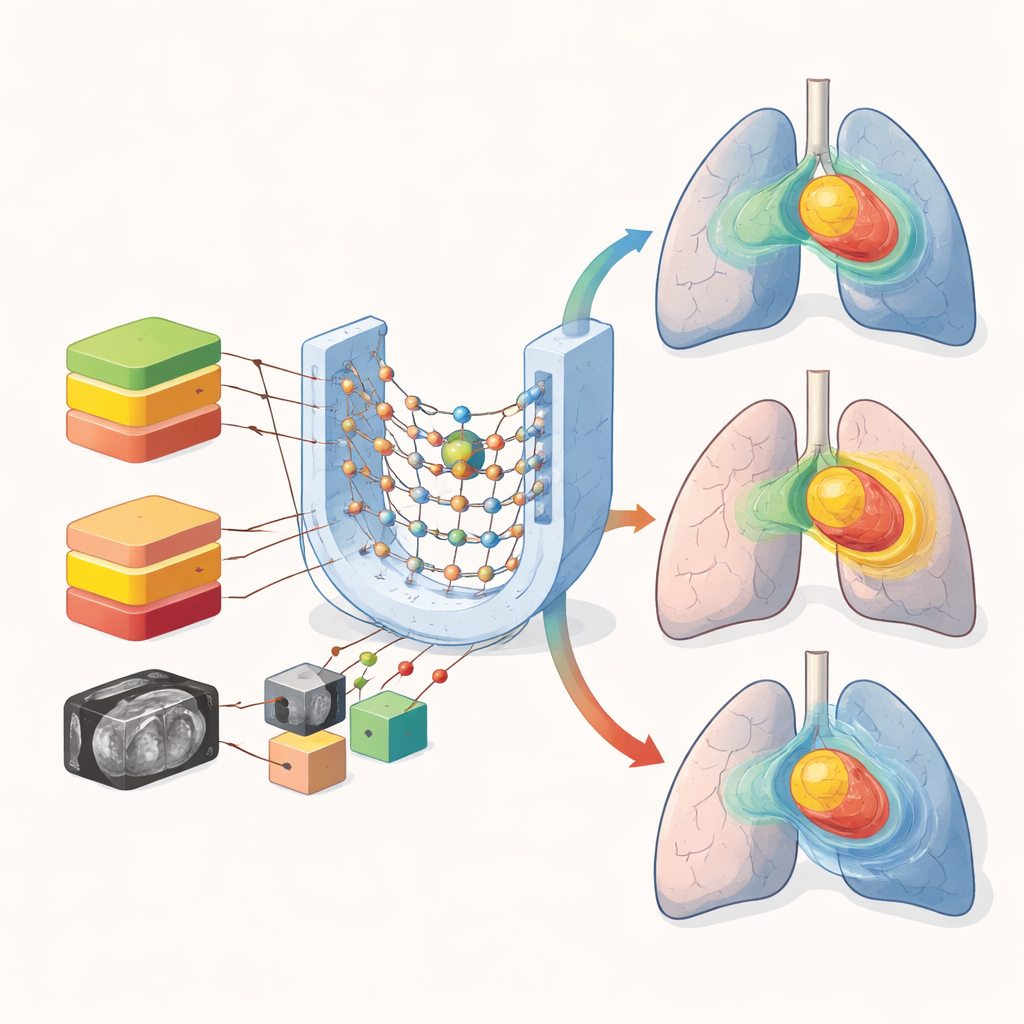
Schutz lebenswichtiger Organe bei schnellerer Planung
Interessanterweise schnitten für viele Organe wie Lungen, Herz und Speiseröhre das gemischte und die stratifizierten Modelle ähnlich ab. Die durchschnittlichen Dosisfehler für diese größeren Strukturen blieben bei allen Ansätzen moderat. Die Hauptschwäche des Mischens der Verordnungen zeigte sich in kleinen, sensiblen Strukturen wie dem Rückenmark, wo ein steiler Dosisabfall entscheidend ist. Visuelle Kontrollen der vorhergesagten Dosisverteilungen zeigten, dass alle Modelle die Gesamtform der Hochdosisregion im Tumor erfassten, das Mischen der Verordnungen aber zu mehr Unschärfe bei scharfen Gradienten und in Niedrigdosisbereichen der Lunge führte. Diese Unterschiede, wenn auch numerisch subtil, können wichtig sein, wenn Ärztinnen und Ärzte entscheiden, ob eine höhere Verordnung sicher ist.
Was das für Patientinnen, Patienten und Kliniken bedeutet
Für Patientinnen und Patienten ersetzt diese Arbeit nicht die sorgfältigen Dosisberechnungen klinischer Systeme, könnte aber dazu beitragen, dass Zeit und Aufwand auf Pläne konzentriert werden, die wirklich machbar und sicher sind. Indem die Studie zeigt, dass das Gruppieren der Trainingsdaten nach Verordnungsdosis die KI‑Vorhersagen deutlich schärft — insbesondere für Tumorabdeckung und Schutz des Rückenmarks —, wird eine praktische Designentscheidung hervorgehoben, die Computerhilfe vertrauenswürdiger machen kann. Mit weiterführenden Tests in größeren und diverseren Patientengruppen könnten solche Modelle zu alltäglichen Werkzeugen werden, die Ärztinnen und Ärzten eine schnelle, anatomiebasierte Vorschau wahrscheinlicher Strahlungskompromisse geben und so eine bessere, konsistentere Behandlungsplanung unterstützen.
Zitation: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
Schlüsselwörter: Strahlentherapie bei Lungenkrebs, Tiefenlern‑Dosisvorhersage, VMAT‑Planung, Behandlungsplanoptimierung, Risikoorgane