Clear Sky Science · de
β‑Nicotinamid‑mononukleotid erhält die Muskelkraft bei septischen männlichen Mäusen
Warum das Überleben einer Sepsis zu anhaltender Schwäche führen kann
Die moderne Intensivmedizin rettet mehr Menschen mit schweren Infektionen als je zuvor, doch viele Überlebende entlassen das Krankenhaus mit einem beunruhigenden Erbe: Ihre Muskeln fühlen sich monatelang oder sogar jahrelang schwach an. Diese anhaltende Gebrechlichkeit, als Intensivstations‑assoziierte Schwäche bezeichnet, erschwert Gehen, Arbeiten und ein selbstständiges Leben. Die hier zusammengefasste Studie stellt eine einfache, aber dringende Frage: Kann ein gezielter Nährstoff die Muskeln während einer Sepsis schützen, sodass Überlebende mehr ihrer Kraft behalten?
Von schwerer Infektion zu müden Muskeln
Um dieses Problem zu untersuchen, nutzten die Forschenden ein Mausmodell, das die menschliche Sepsis gut nachbildet — eine lebensbedrohliche Überreaktion des Körpers auf eine Infektion. Die Tiere verloren während der akuten Erkrankung Gewicht und Muskelmasse und gewannen beides in den folgenden zwei Wochen allmählich zurück. Als die Wissenschaftler jedoch die Kraft maßen, mit der die Mäuse ihre Hinterbeine strecken konnten, blieben die Tiere, die eine Sepsis durchgemacht hatten, deutlich schwächer als gesunde Kontrolltiere. Unter dem Lichtmikroskop erschienen ihre Beinmuskeln in der Größe normal, doch ein genauerer Blick mit der Elektronenmikroskopie zeigte, dass viele der winzigen Kraftwerke in den Muskelzellen — die Mitochondrien — geschwollen, verformt und strukturell geschädigt waren. 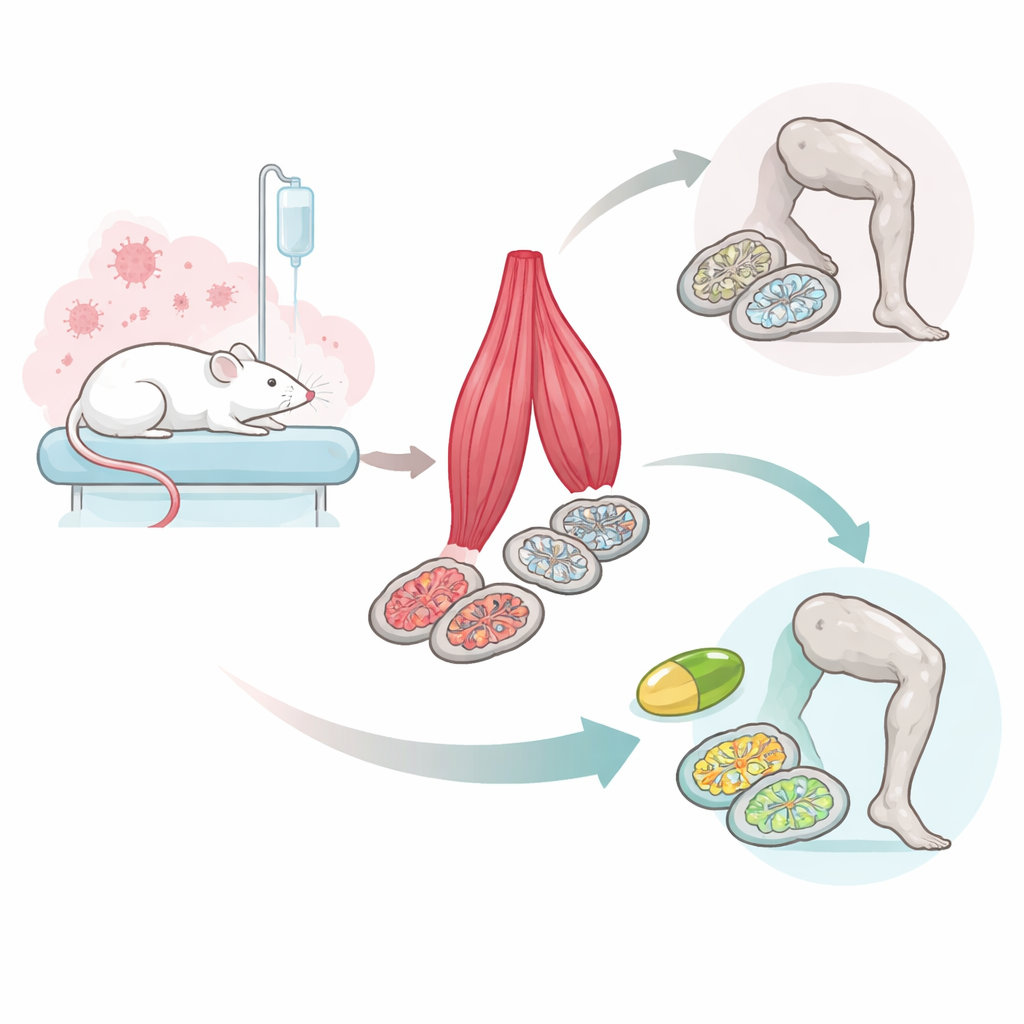
Fokus auf die Kraftwerke der Zelle
Das Team untersuchte anschließend, welche Gene in Muskelgewebe nach einer Sepsis hoch- oder herunterreguliert waren. Sie fanden weitreichende Veränderungen in der Genaktivität, insbesondere in Signalwegen, die mit Energieproduktion und mitochondrialer Gesundheit verknüpft sind. Ein wichtiges Molekül, das auffiel, war Sirt3, ein Protein, das normalerweise dabei hilft, mitochondriale Proteine durch Entfernen chemischer Markierungen namens Acetylgruppen funktionsfähig zu halten. In septischen Muskeln sanken die Sirt3‑Spiegel, während mitochondriale Proteine vermehrt Acetylmarkierungen trugen — ein Muster, das mit verlangsamter Energieproduktion assoziiert ist. Als die Forschenden Sirt3 in kultivierten Muskelzellen gezielt reduzierten, verbrauchten die Mitochondrien der Zellen weniger Sauerstoff und erzeugten weniger Energie, ein Bild, das den Befunden bei den septischen Mäusen entsprach. Das legt nahe, dass ein Abfall der Sirt3‑Aktivität während der Sepsis direkt die Fähigkeit der Muskelmitochondrien, Kontraktionen mit Energie zu versorgen, beeinträchtigen kann.
Ein Nährstoff, der die zelluläre Energie auffüllt
Sirt3 ist auf ein kleines Molekül namens NAD+ angewiesen, und frühere Arbeiten haben gezeigt, dass die NAD+-Vorräte während einer Sepsis abnehmen. Die Forschenden prüften daher, ob eine Erhöhung von NAD+ helfen könnte. Sie verwendeten β‑Nicotinamid‑mononukleotid (β‑NMN), eine Verbindung, die der Körper leicht in NAD+ umwandeln kann. In Muskelzellen mit reduziertem Sirt3 erhöhte die Zugabe von β‑NMN die NAD+-Spiegel und stellte teilweise die mitochondriale Atmung und Energieproduktion wieder her. Der eindrücklichste Test erfolgte in lebenden Mäusen: Tiere mit Sepsis erhielten während der akuten Krankheitsphase Injektionen von β‑NMN, Vergleichstiere bekamen lediglich eine Kochsalzlösung. Beide Gruppen gewannen vergleichbare Mengen an Muskelmasse und Körpergewicht zurück, doch die β‑NMN‑behandelten Mäuse erlangten deutlich mehr ihrer Beinmuskraft zurück. Die Elektronenmikroskopie zeigte, dass ihre Muskelmitochondrien weniger deformiert und strukturell intakter waren als die der unbehandelten septischen Mäuse. 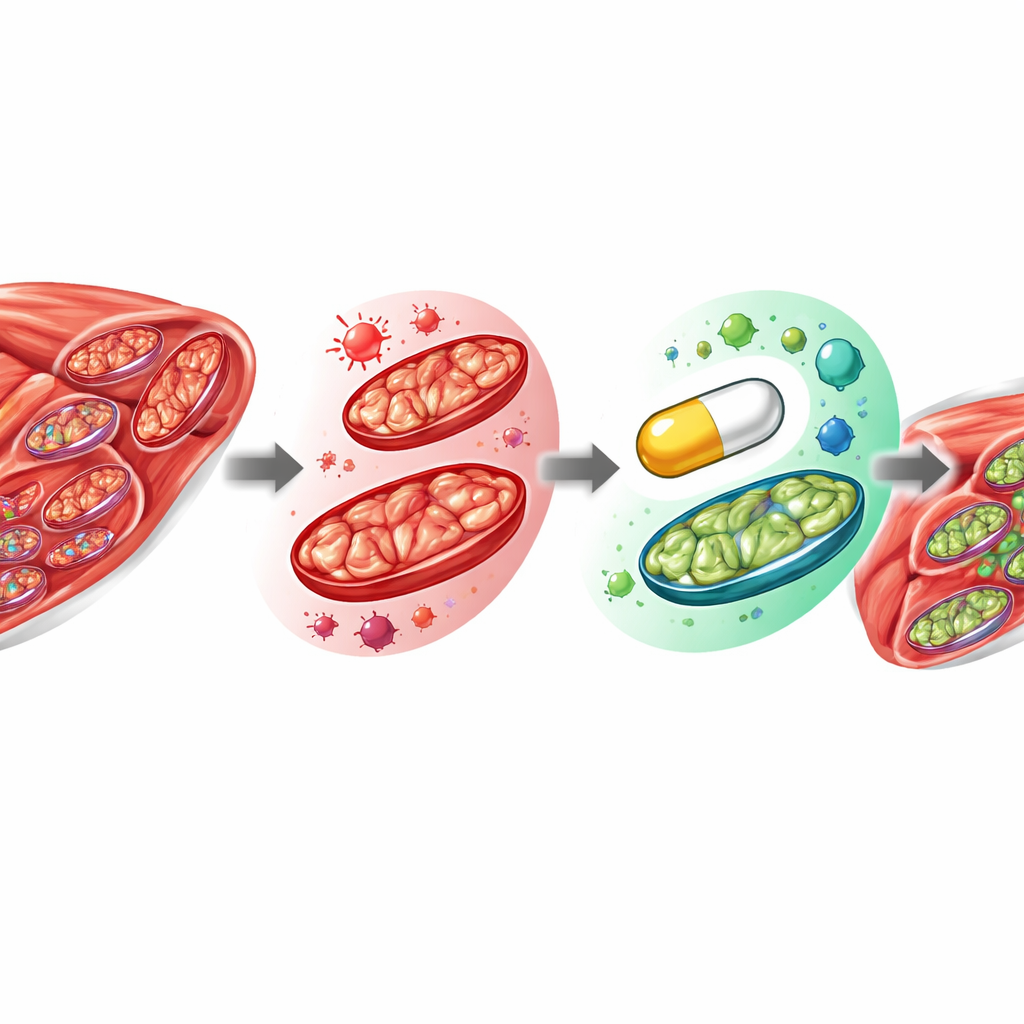
Neu denken über Ernährung nach kritischer Erkrankung
Die traditionelle Ernährung auf der Intensivstation konzentriert sich auf Kalorien und Protein, um Muskelabbau zu verhindern. Diese Studie legt nahe, dass solche Maßnahmen zwar wichtig sind, möglicherweise aber nicht ausreichen, um die Muskelqualität zu erhalten. Die Arbeit rückt die mitochondriale Gesundheit und den NAD+-Stoffwechsel in den Mittelpunkt für langfristige Kraft nach einer Sepsis. Anstatt die Muskeln nur zu „füttern“, könnten künftige Therapien darauf abzielen, ihre Mitochondrien zu „ernähren“ — etwa mit Verbindungen wie β‑NMN, um die zellulären Stoffwechselbedingungen zu erhalten, die Sirt3 und verwandte Proteine aktiv halten. Die Autoren betonen, dass ihre Experimente an jungen männlichen Mäusen und über vergleichsweise kurze Zeiträume durchgeführt wurden, sodass noch viel zu klären ist, bevor sich dieser Ansatz auf Patienten übertragen lässt.
Was das für Patienten bedeuten könnte
Einfache gesagt zeigt die Studie, dass Muskeln nach einer lebensbedrohlichen Infektion äußerlich normal wirken können, aber innerlich erschöpft sind, weil ihre Motoren beschädigt sind. Durch die Bereitstellung eines Bausteins für ein zentrales Energiemolekül half β‑NMN, diese Motoren bei Mäusen zu schützen und mehr Kraft zu erhalten, ohne die Muskelgröße zu verändern. Obwohl es noch zu früh ist, solche Ergänzungen für Menschen mit Sepsis zu empfehlen, deuten die Ergebnisse auf eine neue Art von Ernährungsstrategie hin — eine, die darauf abzielt, die Energiewährung der Zelle wiederherzustellen und die Selbstständigkeit von Überlebenden kritischer Erkrankungen zu sichern.
Zitation: Saida, M., Saeki, N., Sakai, H. et al. β-Nicotinamide mononucleotide preserves muscle strength in septic male mice. Sci Rep 16, 8905 (2026). https://doi.org/10.1038/s41598-026-43172-w
Schlüsselwörter: Sepsis, Muskelkraftverlust, Mitochondrien, NAD+-Stoffwechsel, β‑Nicotinamid‑mononukleotid