Clear Sky Science · de
Ernährungsmuster beeinflussen die in silico GABA‑Produktionskapazität von Bifidobacterium adolescentis HD17T2H und anderen menschlichen Darmbakterien
Warum Ihr Abendessen Ihrer Stimmung schaden oder nützen könnte
Viele Menschen haben gehört, dass der Darm wie ein „zweites Gehirn“ ist, doch es ist weiterhin unklar, wie unsere Nahrung diese verborgene Welt von Mikroben formt und damit unsere psychische und Verdauungsgesundheit beeinflusst. Diese Studie untersucht einen wichtigen Botenstoff, Gamma‑Aminobuttersäure (GABA), ein chemischer Stoff, der die Nervenaktivität dämpft und nicht nur im Gehirn, sondern auch von Darmbakterien produziert wird. Die Forschenden stellten eine scheinbar einfache Frage: Wenn man die Ernährung verändert, wie verändert das die Fähigkeit der Darmmikroben, GABA herzustellen?
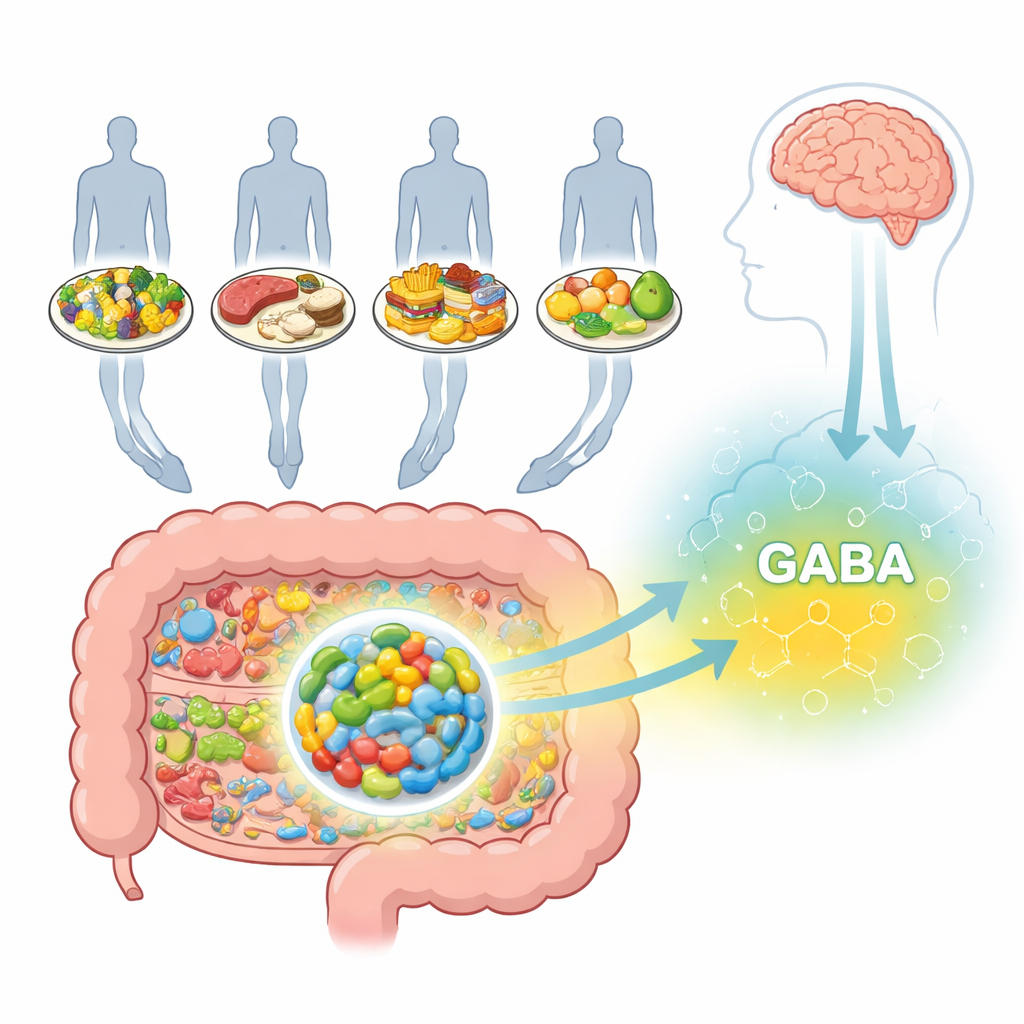
Ein beruhigender Botenstoff, der im Darm entsteht
GABA ist vor allem als beruhigendes Signal im Gehirn bekannt, wo es verhindert, dass Nervenzellen überaktiv werden, und mit Angststörungen und Depression in Verbindung gebracht wurde. GABA wirkt aber auch direkt im Darm, wo es die Darmbewegung, die Sekretion von Flüssigkeiten und die Freisetzung von Hormonen beeinflusst. Einige Darmbakterien können aus gebräuchlichen Nährstoffen über gut charakterisierte biochemische Wege GABA herstellen. Ein solches Mikrobe, Bifidobacterium adolescentis HD17T2H, sticht als starker GABA‑Produzent hervor und gehört zu einer Gruppe von Bakterien, die häufig in probiotischen Produkten vorkommen. Bislang fehlte jedoch ein systematischer Überblick darüber, wie unterschiedliche Ernährungsweisen die Fähigkeit dieses Bakteriums zur GABA‑Produktion verändern könnten.
Computer‑Modelle als virtuelles Darmlabor
Anstatt dutzende aufwändige Laborversuche durchzuführen, erstellte das Team ein detailliertes Computermodell von B. adolescentis auf Grundlage seines Genoms. Dieses virtuelle Mikrobenmodell wurde dann mit elf realistischen Tagesdiäten „gefüttert“, die aus einer Ernährungsdatenbank stammten, darunter vegetarische, vegane, proteinreiche, durchschnittlich europäische, mediterrane, kohlenhydratarme und ketogene Muster. Mit mathematischen Werkzeugen, die abschätzen, wie Nährstoffe durch den Stoffwechsel fließen, berechneten die Forschenden, wie viel GABA das Bakterium prinzipiell unter jeder Diätsekretion abgeben könnte, während es noch wächst. Außerdem führten sie tausende virtuelle „Supplementierungs“-Tests durch, indem sie in silico einzelne Nährstoffe erhöhten, um zu sehen, welche die GABA‑Produktion am stärksten steigern.
Wie verschiedene Diäten das GABA‑Potenzial formen
Die Simulationen zeigten auffällige Unterschiede zwischen den Ernährungsweisen. Unter den Basisbedingungen ergab die vegetarische Diät das höchste GABA‑Produktionspotenzial für dieses Bakterium, dicht gefolgt von einer proteinreichen Diät und einer für Typ‑2‑Diabetes konzipierten Ernährung. Am anderen Ende der Skala lieferte ein ketogenes, sehr kohlenhydratarmes Programm den niedrigsten Basis‑GABA‑Output; auch eine vegane Ernährung lag eher niedriger. Als das Team künstlich die Versorgung mit einzelnen Verbindungen erhöhte, trieben zwei breite Nährstoffklassen die GABA‑Produktion konsequent nach oben: Kohlenhydrate und stickstoffreiche Moleküle, insbesondere Aminosäuren. In kohlenhydratarmen Diäten hatte die Zugabe zuckerähnlicher Verbindungen den größten Effekt, was darauf hindeutet, dass Kohlenstoffenergie der begrenzende Faktor war. Im Gegensatz dazu hatten in kohlenhydratreichen Diäten wie vegetarischen und veganen Mustern zusätzliche Aminosäuren und verwandte Stickstoffquellen den stärksten Einfluss, was darauf hinweist, dass dort Stickstoff zur Engstelle wurde.
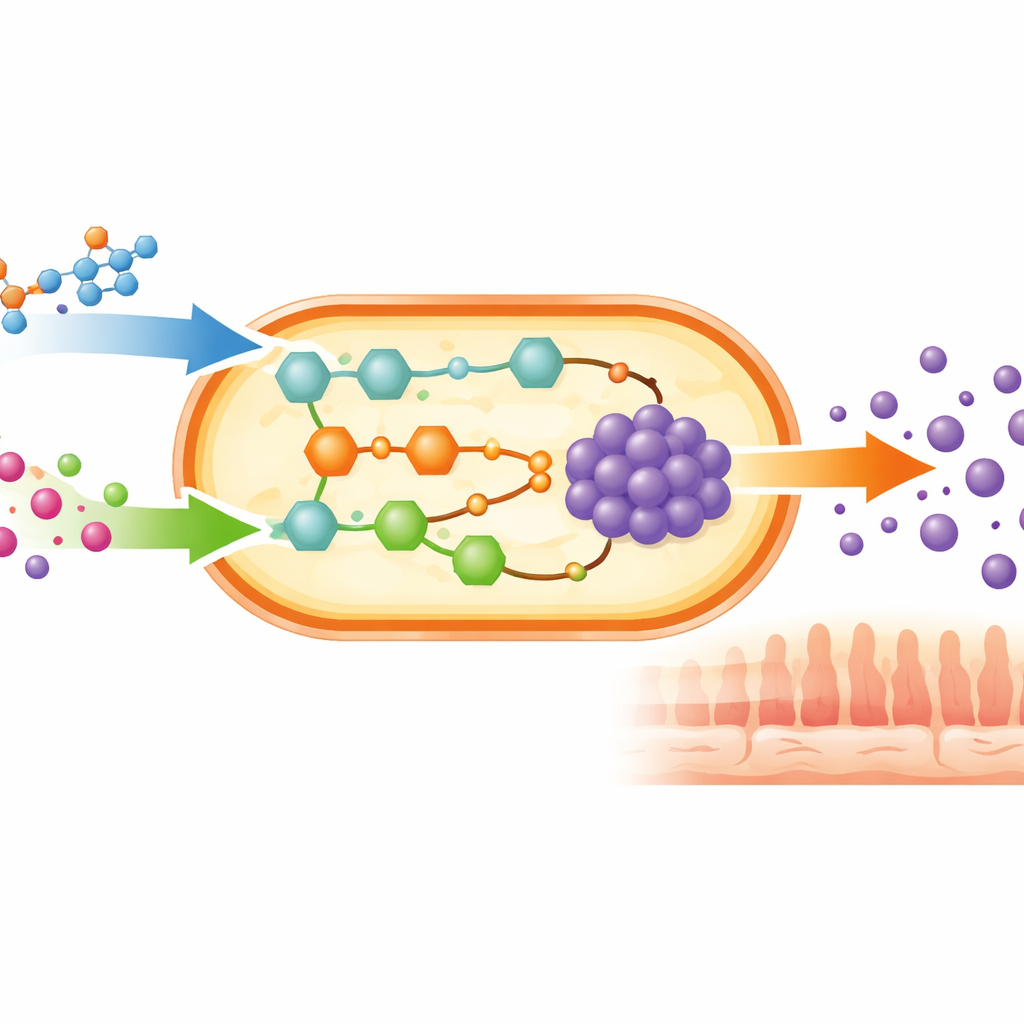
Über ein Bakterium hinausblicken
Um zu prüfen, wie sich diese Befunde beim Menschen auswirken könnten, nutzten die Forschenden detaillierte Ernährungsaufzeichnungen von mehr als tausend Erwachsenen aus der Kieler Kohorte. Für jede Person berechneten sie, wie viel GABA ihre persönliche B. adolescentis‑Population theoretisch aus der angegebenen Nahrungsaufnahme produzieren könnte. Ein Machine‑Learning‑Ansatz bestätigte, dass Aminosäuren die mit Abstand wichtigsten Ernährungsfaktoren waren, gefolgt von anderen stickstoffhaltigen Verbindungen, bestimmten Zuckern, Fettsäuren und B‑Vitamine, die enzymatische Reaktionen unterstützen. Das Team erweiterte anschließend seine Modellierung auf vollständige mikrobielle Gemeinschaften derselben Kohorte unter Verwendung einer großen Bibliothek von Darmmikrobenmodellen. Sie identifizierten 87 bakterielle Stämme aus 47 Gattungen, die GABA herstellen können, darunter sowohl harmlose Bewohner als auch potenzielle Krankheitserreger, was unterstreicht, dass GABA‑Produktion eine weit verbreitete Überlebensstrategie im Darmökosystem ist und nicht nur ein Merkmal weniger „guter“ Mikroben.
Folgen für Gesundheit und künftige Forschung
Insgesamt zeigt die Studie, dass die Fähigkeit von Darmbakterien, GABA zu produzieren, sehr empfindlich auf die Ernährung reagiert und dass die begrenzenden Nährstoffe vom Gesamternährungsmuster abhängen: kohlenstoffreiche Zucker in Low‑Carb‑Situationen und stickstoffreiche Bausteine in kohlenhydratreichen. Das bedeutet nicht, dass Menschen nun Zucker oder Eiweiß in großen Mengen zu sich nehmen sollten, um höhere GABA‑Werte zu erzielen — zuckerreiche Diäten sind beispielsweise mit Gesundheitsrisiken verbunden und können psychische Störungen trotz möglicher mikrobieller Effekte verschlechtern. Vielmehr liefert die Arbeit eine mechanistische Karte, welche Nährstoffe für mikrobielle GABA‑Produktion besonders wichtig sind, und hebt hervor, dass viele Darmarten, nicht nur klassische Probiotika, zu diesem beruhigenden Molekül beitragen können. Künftige Labor‑ und klinische Studien sind notwendig, um zu prüfen, wie sich diese in silico‑Erkenntnisse in reale Veränderungen von Darm‑ und Hirnfunktion übersetzen lassen und ob gezielt gestaltete Diäten oder Ergänzungen die mikrobielle GABA‑Produktion sicher nutzen können, um mentale und Verdauungsgesundheit zu unterstützen.
Zitation: Homscheid, A., Moors, K.A., Nap, B. et al. Dietary patterns influence the in silico GABA production capacity of Bifidobacterium adolescentis HD17T2H and other human gut bacteria. Sci Rep 16, 8961 (2026). https://doi.org/10.1038/s41598-026-43006-9
Schlüsselwörter: Darmmikrobiom, GABA, Ernährungsmuster, Bifidobacterium adolescentis, Darm‑Hirn‑Achse