Clear Sky Science · de
PGE2 reguliert Ferroptose und Osteogenese von MC3T3-E1-Zellen über NOS2
Warum das Zähne-Richten Ihre Knochen beeinflusst
Zahnspangen und transparente Aligner verschieben nicht nur die Zähne — sie fordern den umgebenden Knochen dazu auf, sich umzubauen. Diese langsame biologische Aufbauarbeit erklärt zum Teil, warum kieferorthopädische Behandlungen Jahre dauern können. Die vorliegende Studie blickt in knochenbildende Zellen, um zu verstehen, wie ein häufiger Entzündungsmediator, Prostaglandin E2, sowohl die Zahnbewegung beschleunigen als auch die neu gebildete Knochensubstanz unauffällig schwächen könnte. Die Ergebnisse deuten auf zukünftige Ansätze hin, kieferorthopädische Behandlungen schneller und stabiler zu machen.
Signale, die beim Verschieben von Zähnen freigesetzt werden
Wenn ein Kieferorthopäde Kraft auf einen Zahn ausübt, erfahren das Parodontalligament und der umgebende Knochen am Zahnwurzelbereich eine kontrollierte Verletzung. Zellen in diesem Bereich setzen chemische Botenstoffe frei, darunter Prostaglandin E2, die koordinieren, wie Knochen auf der einen Seite abgebaut und auf der anderen neu aufgebaut wird. Die Autoren konzentrierten sich auf knochenbildende Zellen, sogenannte Osteoblasten, und nutzten eine standardisierte Maus-Zelllinie als Modell. Sie wollten wissen, wie Prostaglandin E2 zwei zentrale Ergebnisse in diesen Zellen beeinflusst: ihre Fähigkeit, mineralisierten Knochen zu bilden, und ihre Neigung, an einer kürzlich entdeckten, eisenabhängigen Form des Zelltods namens Ferroptose zu sterben.
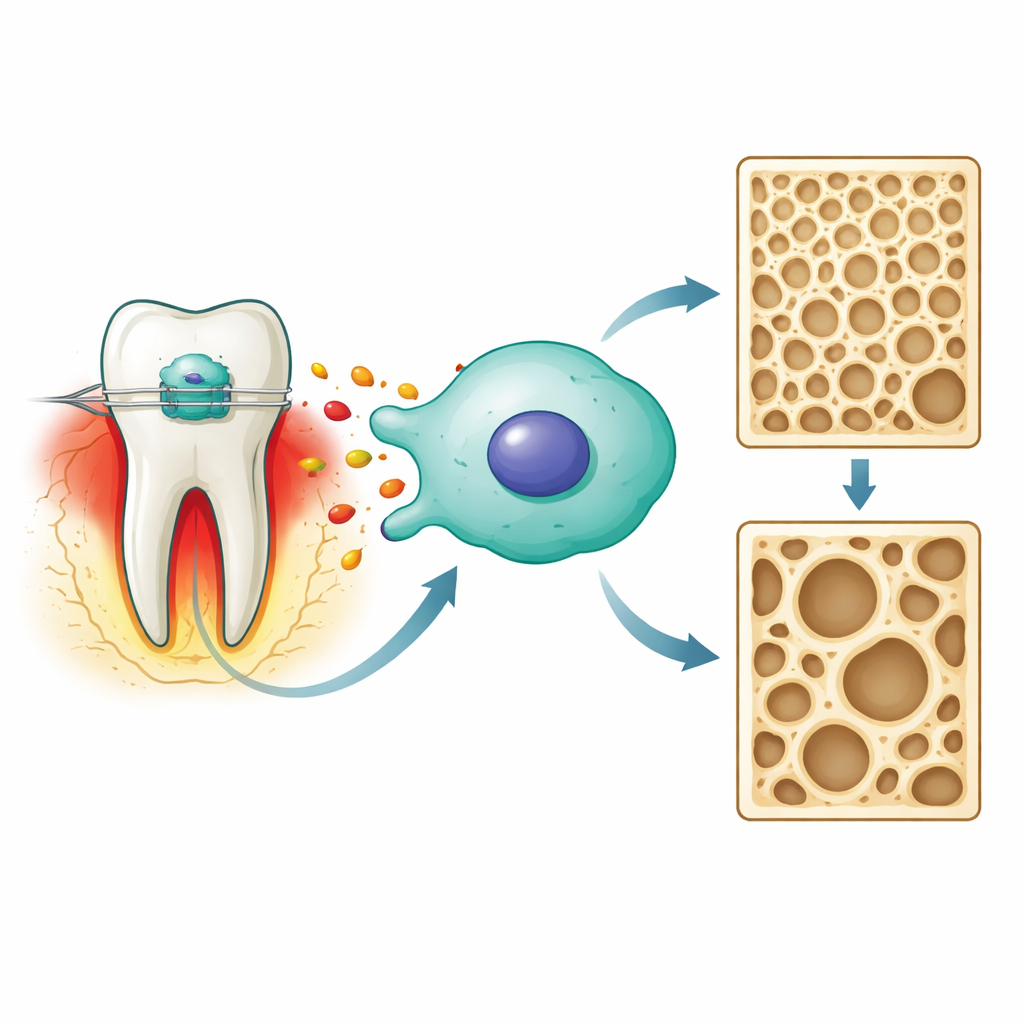
Ein Stressweg, zentriert um ein einzelnes Enzym
Anhand von Genexpressionsdaten aus Ratten mit Zahnbewegung suchte das Team zunächst nach Molekülen, die sowohl mit kieferorthopädischer Belastung als auch mit Ferroptose verknüpft sind. Ein Kandidat, ein Enzym namens Stickstoffmonoxid-Synthase 2 (NOS2), stach als zentrales Bindeglied hervor. In Kultur führte die Exposition osteoblastenähnlicher Zellen gegenüber einer klinisch relevanten Dosis Prostaglandin E2 zu einem Zustand „steriler“ Entzündung — keine Keime beteiligt, nur mechanischer Stress. Unter diesem Signal stiegen NOS2-Werte, ebenso wie andere Stressmarker und schädliche reaktive Sauerstoffspezies, während schützende Antioxidantien und eisenregulierende Proteine abnahmen. Zusammen sind diese Verschiebungen Kennzeichen des Einsetzens von Ferroptose in der Zelle.
Wenn die Knochenbauer abschalten
Die gleiche Behandlung mit Prostaglandin E2 verschlechterte außerdem die osteoblastischen Eigenschaften der Zellen. Klassische Marker der Knochenbildung sanken, und Tests, die frühe knochenähnliche Mineralisation und das Schlüsselenzym alkalische Phosphatase sichtbar machen, zeigten schwächere Färbung und geringere Mineralablagerung. Als die Forschenden Ferrostatin-1 hinzufügten, ein Wirkstoff, der Ferroptose blockiert, kehrte ein großer Teil dieses Schadens um: oxidativer Stress ließ nach, Ferroptose-Signale wurden gedämpft und die osteogene Aktivität erholte sich. Das legt nahe, dass in diesem Modell das entzündliche Signal die Knochenbildung zumindest teilweise dadurch hemmt, dass es Zellen in Richtung Ferroptose treibt.
NOS2 wie einen Schalter hoch- und runterregeln
Um zu klären, ob NOS2 nur Nebenakteur oder aktiver Treiber ist, veränderte das Team genetisch die NOS2-Level nach oben und unten. Die Reduktion von NOS2 in prostaglandinbehandelten Zellen verringerte Ferroptose-Marker, senkte oxidativen Schaden und stellte das knochenbildende Verhalten weitgehend wieder her. Die Überexpression von NOS2 hatte den umgekehrten Effekt: Sie verstärkte Stress und unterdrückte die knochenaufbauenden Merkmale weiter. Bemerkenswert war, dass die alleinige Erhöhung von NOS2 — ohne zusätzliches Prostaglandin E2 — ausreichte, ferroptoseähnliche Veränderungen auszulösen und die Osteogenese abzuschwächen. Das zeigt, dass NOS2 nicht nur auf Entzündungen reagiert; es kann selbst Osteoblasten davon abbringen, stabilen mineralisierten Knochen zu bilden.
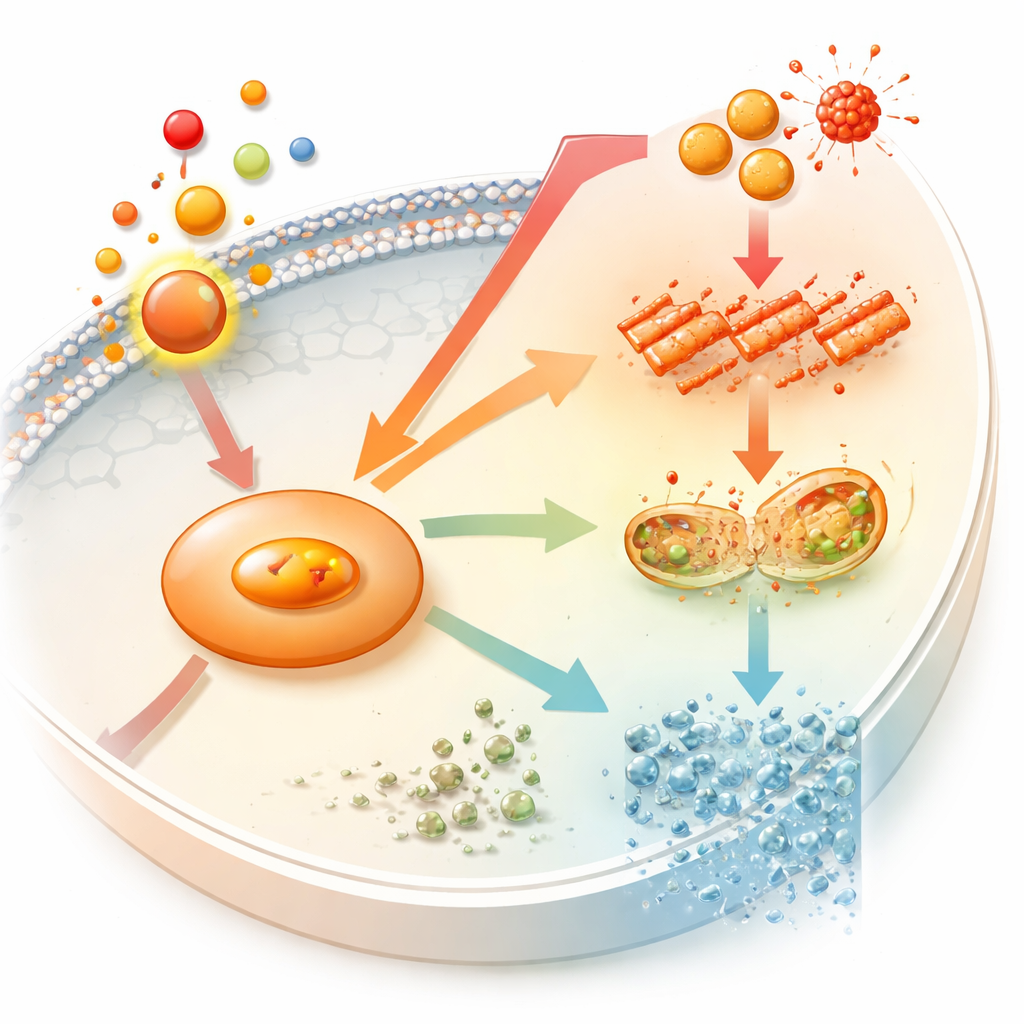
Was das für zukünftige Zahnspangen bedeutet
Zusammen zeichnen diese Experimente eine neue Achse in der Knochenbiologie während der Zahnbewegung nach: Prostaglandin E2 erhöht NOS2, NOS2 fördert oxidativen Schaden und Ferroptose, und die knochenbildende Kapazität nimmt ab. Für Patientinnen und Patienten bedeutet das nicht, dass Zahnspangen unsicher sind, aber es erklärt, warum die Behandlung ein sensibles Gleichgewicht zwischen schneller Zahnbewegung und dem Erhalt starken Knochens um die Zähne herum erfordert. Langfristig könnten Wirkstoffe oder Materialien, die NOS2-Aktivität feinjustieren oder Osteoblasten vor Ferroptose schützen, Kieferorthopäden helfen, Behandlungszeiten zu verkürzen und gleichzeitig die Qualität und Stabilität des stützenden Knochens zu erhalten oder sogar zu verbessern.
Zitation: Sun, M., Yang, Y., Pang, L. et al. PGE2 regulates ferroptosis and osteogenesis of MC3T3-E1 cells via NOS2. Sci Rep 16, 8893 (2026). https://doi.org/10.1038/s41598-026-43001-0
Schlüsselwörter: kieferorthopädische Zahnbewegung, Knochenumbau, Ferroptose, Stickstoffmonoxid-Synthase, Osteoblastenfunktion