Clear Sky Science · de
Erforschung der doppelten Rolle extrazellulärer Vesikel bei Gerinnung und Immunmodulation im Glioblastom
Warum Blutgerinnsel bei Hirntumoren wichtig sind
Patienten mit Glioblastom, der aggressivsten Form von Hirntumoren, sehen sich häufig einer unerwarteten Gefahr gegenüber: lebensbedrohlichen Blutgerinnseln in Beinen oder Gehirn. Diese Gerinnsel können das Überleben verkürzen und bereits anspruchsvolle Behandlungen weiter verkomplizieren. Die Studie stellt eine einfache, aber entscheidende Frage: Was ist es an Glioblastomzellen, das das umgebende Blut so gerinnungsfreudig macht, und wie verändern die winzigen Partikel, die sie ins Blut abgeben, die Abwehrkräfte des Körpers?
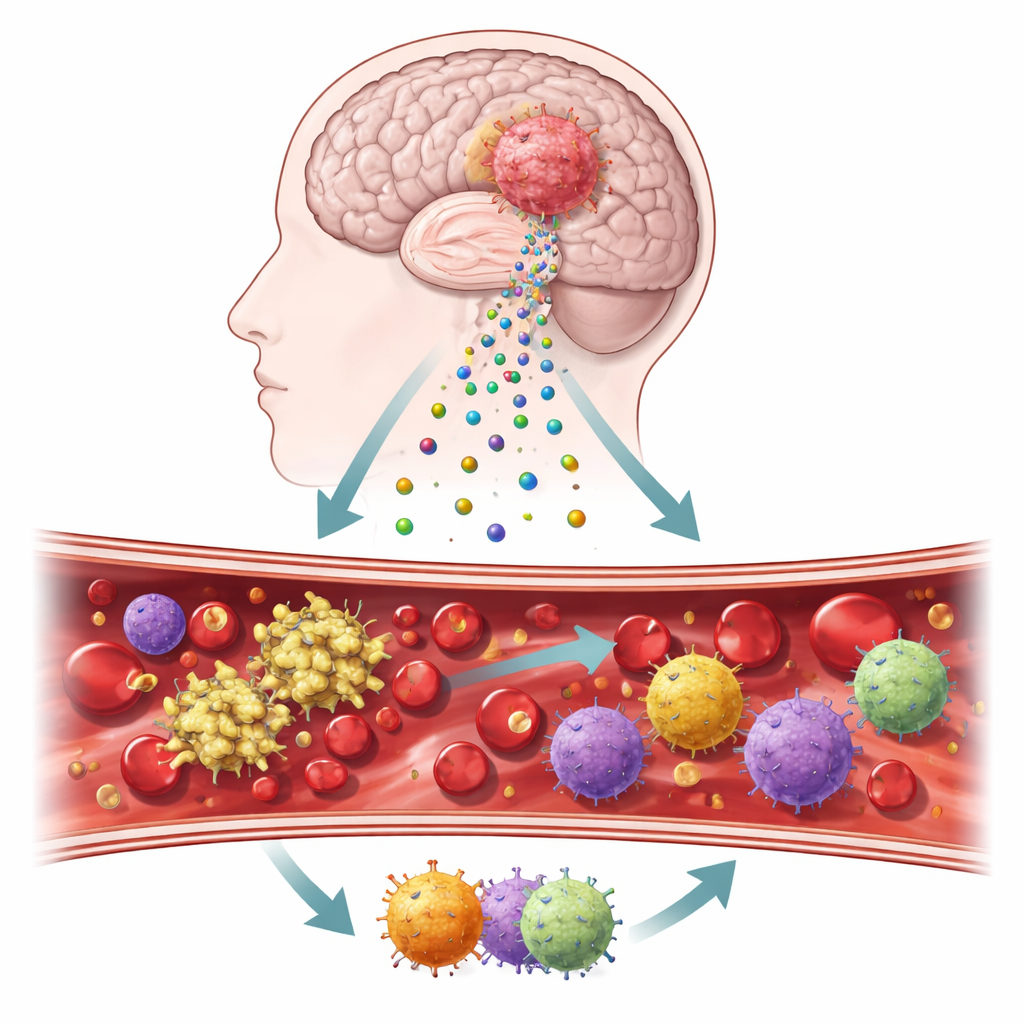
Kleine Botenstoffe, die einen Hirntumor verlassen
Die Forschenden konzentrierten sich auf mikroskopische Bläschen, sogenannte extrazelluläre Vesikel, die von Tumorzellen abschnüren und durch Blut und Hirngewebe schweben. Auf ihrer Oberfläche tragen diese Vesikel zwei Schlüsselproteine, Gewebsfaktor und Podoplanin, die bekannt dafür sind, Gerinnung auszulösen und Entzündungen zu beeinflussen. Mit Tumorproben, während der Operation entnommenem Blut und aus Patienten-Tumoren gezüchteten Zellkulturen entwickelte das Team einen stufenweisen Workflow, um nachzuverfolgen, wie diese Moleküle bei realen Patienten sowie in kontrollierten Labortests agieren. Sie verglichen außerdem Tumorgewebe mit normalem Gehirngewebe, um zu sehen, wie stark diese gerinnungsassoziierten Signale aktiviert sind.
Ein ruhiger Blutkreislauf, aber eine vorgespannte Tumorzone
Standard-Labortests im Krankenhaus deuteten darauf hin, dass das Blut vieler Patienten vor der Operation überraschend normal aussah: übliche Gerinnungszeiten und Werte zur Gerinnungsstärke lagen größtenteils im Referenzbereich. Sobald die Forschenden jedoch das Tumorgewebe untersuchten, zeichnete sich ein anderes Bild ab. Glioblastomgewebe zeigte durchgehend hohe Mengen an Gewebsfaktor und Podoplanin sowie sehr niedrige Spiegel eines natürlichen Bremssystems, des Gewebsfaktor-Weg-Inhibitors. Aus Patienten gewonnene Tumorzelllinien behielten dieses Muster überwiegend auch in der Kulturschale bei, was bestätigt, dass die „gerinnungsfreundliche“ Signatur eine intrinsische Eigenschaft der Krebszellen ist. Wenn diese Zellen oder die von ihnen freigesetzten Vesikel im Labor mit Plasma vermischt wurden, bildeten sich schneller Gerinnsel, vor allem über den sogenannten extrinsischen Weg, der auf Gewebsfaktor beruht.
Verschiedene Tumorzellen, verschiedene Gerinnungsstrategien
Nicht alle Glioblastome verhielten sich gleich. Manche aus Patienten stammende Zelllinien wiesen sehr hohe Gewebsfaktorspiegel auf, andere mehr Podoplanin, und einige nur wenig von beidem. Zellen mit hohem Gewebsfaktor waren am wirksamsten darin, die Gerinnungszeit zu verkürzen, während podoplaninreiche Zellen eher über Wirkungen auf Thrombozyten einen moderaten Beitrag leisteten. Wenn eine solche Zelllinie in Untergruppen aufgetrennt wurde, die nur Gewebsfaktor, nur Podoplanin, beides oder keines von beiden exprimierten, blieben die Gruppen nicht lange stabil. Innerhalb von drei Wochen drifteten die Zellen zurück zu gemischten Profilen, was eine hohe Plastizität offenbarte. Dieser dynamische Umbau ging mit Verschiebungen im oxidativen Stress innerhalb der Zellen einher, was nahelegt, dass chemischer Stress im Tumor die Zellen in stärker gerinnungsfördernde Zustände treiben kann.
Vesikel als Gestalter der Immunität in Gehirn und Blut
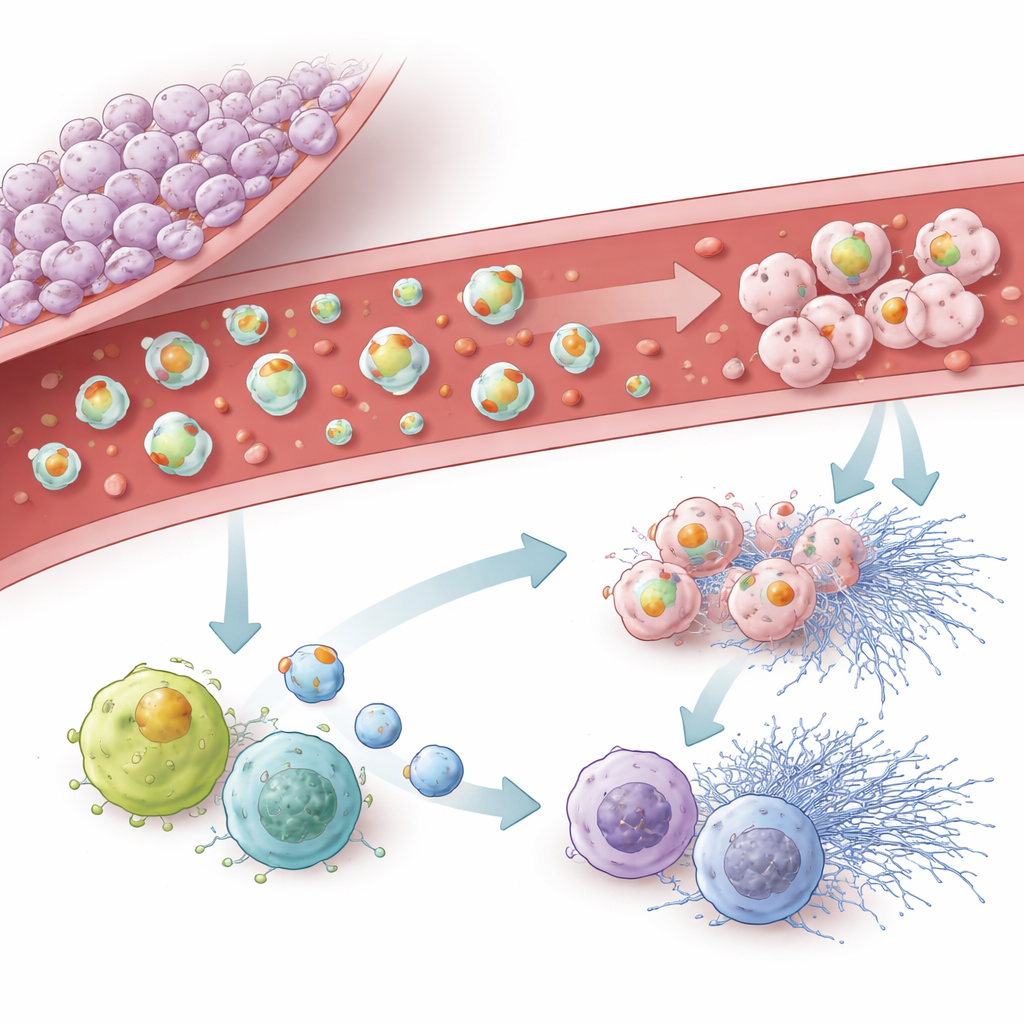
Das Team untersuchte anschließend genauer, wie tumorderivierte Vesikel die Immunzellen des Gehirns, die Mikroglia, sowie zirkulierende Leukozyten und Neutrophile beeinflussen. Vesikel aus stark pro‑gerinnenden Tumorzelllinien wurden von Mikroglia leicht aufgenommen und verlangsamten deren Wanderung, gleichzeitig drängten sie die Mikroglia in einen entzündlicheren, „M1‑ähnlichen“ Zustand und zeigten Merkmale zellulären Alterns. Im Blut aktivierten vesikelreiche an Gewebsfaktor Leukozyten, erhöhten die Produktion reaktiver Sauerstoffspezies und förderten die Freisetzung klebriger, netzartiger Strukturen von Neutrophilen, bekannt als neutrophile extrazelluläre Fallen. Vesikel mit Podoplanin waren weniger kraftvoll in der Auslösung dieser explosiven Immunreaktionen, förderten jedoch stark ein seneszenzähnliches Programm, in dem Immunzellen aufhören zu teilen und ihr Verhalten ändern. Selbst Vesikel ohne beide Schlüsselproteine konnten noch eine gewisse Seneszenz hervorrufen, was darauf hindeutet, dass auch andere Frachtstoffe eine Rolle spielen.
Was das für Patienten und künftige Therapien bedeutet
In der Summe zeigen die Ergebnisse, dass Glioblastom nicht einfach überall das Blut dickflüssiger macht. Stattdessen schaffen der Tumor und die von ihm freigesetzten Vesikel eine lokalisierte, hochkomplexe Zone, in der Gerinnung und Entzündung sich gegenseitig antreiben. Gewebsfaktor erweist sich als treibende Kraft der Gerinnselbildung und der entzündlichen Aktivierung, während Podoplanin zusätzlichen Einfluss auf Thrombozyten, Immunalterung und Mikroglia‑Verhalten ausübt. Da diese Vesikel zirkulieren und den Zustand des Tumors spiegeln, könnten sie künftig als blutbasierte Marker dienen, um Patienten mit besonders hohem Gerinnselrisiko zu identifizieren. Sie könnten auch auf gezieltere Präventionsstrategien hinweisen, die die gerinnungsfördernden Mechanismen des Tumors anvisieren, ohne das Blut allgemein stärker zu verdünnen.
Zitation: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
Schlüsselwörter: Glioblastom, Blutgerinnsel, extrazelluläre Vesikel, Tumormikroumgebung, Immunantwort