Clear Sky Science · de
Bewertung des Dodecin-Gerüsts von Mycobacterium tuberculosis als Multimerisierungsplattform für die Immunogenität von HPV L2-Antigenen
Warum diese Forschung für künftige Impfstoffe wichtig ist
Humanes Papillomavirus (HPV) verursacht nahezu alle Zervixkarzinome sowie einen wachsenden Anteil anderer Krebsarten, doch die aktuellen Impfstoffe sind komplex herzustellen und decken nicht alle gefährlichen Virustypen vollständig ab. In dieser Studie wird ein neuer Ansatz untersucht, um einen einfacheren, breit wirkenden HPV-Impfstoff zu entwickeln, der günstiger, stabiler und weltweit leichter einsetzbar sein könnte – insbesondere in Ländern mit niedrigem und mittlerem Einkommen. Durch eine Umgestaltung, wie zentrale Virusproteinfragmente dem Immunsystem präsentiert werden, wollen die Forschenden den Körper dazu anregen, starke Antikörper gegen viele HPV-Typen gleichzeitig zu bilden.
Ein neuer Baustein für HPV-Schutz
Die heutigen HPV-Impfstoffe beruhen auf einem Hüllprotein namens L1, das zu virusähnlichen Partikeln assembliert wird und zwar starke Antikörperreaktionen auslöst, diese aber vor allem gegen die wenigen in jedem Impfstoff enthaltenen HPV-Typen. Das Team konzentrierte sich stattdessen auf ein zweites Virusprotein, L2, das kurze Regionen enthält, die über viele HPV-Typen hinweg ähnlich sind und daher breiteren Schutz auslösen können. Sie verwendeten ein zuvor entwickeltes Antigen namens Trx-8mer, bei dem kleine konservierte L2-Stücke aus acht HPV-Typen aneinandergereiht und auf einem stabilen Trägerprotein präsentiert werden. Frühere Arbeiten zeigten bereits, dass das Bündeln von sieben dieser Trx-8mer-Einheiten zu einem ringförmigen Komplex (ein Impfstoff namens PANHPVAX) starke, kreuzschützende Antikörperantworten erzeugt und sich nun in frühen klinischen Tests befindet.
Ein bakterielles Protein als Impfstoffplattform
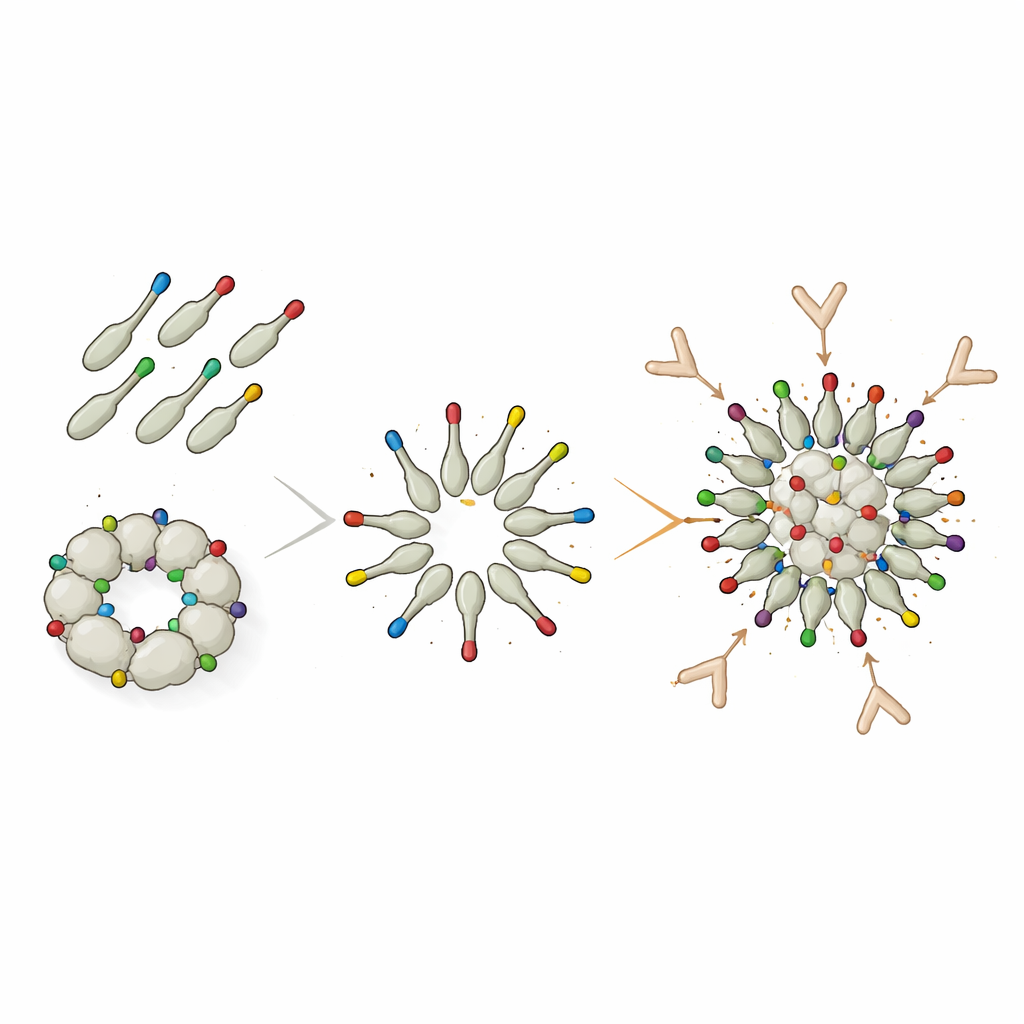
In dieser Studie versuchten die Forschenden, über sieben Kopien hinauszugehen und noch mehr L2-Antigene pro Partikel unterzubringen, in der Annahme, dass hoch repetitive Muster besonders gut B-Zellen, die antikörperproduzierenden Zellen des Immunsystems, aktivieren. Sie wählten ein kleines, hitzeresistentes Protein aus dem Tuberkulosebakterium, Dodecin genannt, das natürlicherweise zu hohlen Kugeln aus zwölf identischen Untereinheiten assembliert. Durch die genetische Fusion von Trx-8mer an Dodecin schufen sie mehrere neue Impfstoffkandidaten, die sich selbst zu multimeren Nanopartikeln zusammenfügen und viele Kopien von L2 präsentieren sollten. Diese Partikel konnten in Bakterien produziert, dank ihrer Robustheit bei hohen Temperaturen gereinigt und mit mehreren biophysikalischen Methoden als die beabsichtigten nanoskaligen Strukturen verifiziert werden.
Wenn direkte Fusion nicht ausreicht
Überraschenderweise war das einfache Anhängen der L2-Fracht direkt an das Dodecin-Gerüst in Mäusen nicht überlegen gegenüber dem bestehenden heptameren Referenzimpfstoff PANHPVAX. Obwohl die multimeren Partikel wie geplant gebildet wurden und neutralisierende Antikörper gegen sowohl Impfstoff- als auch Nicht-Impfstoff-HPV-Typen induzierten, lagen die Titer in der Regel unter denen von PANHPVAX. Auch das Hinzufügen eines eingebauten Helfer-T-Zell-Epitope, das manchmal die Antikörperantwort verstärkt, verbesserte die Wirkung nicht. Strukturelle Modellierung und funktionelle Daten deuteten darauf hin, dass die voluminösen, direkt gefuseten Trx-8mer-Einheiten sich gegenseitig verdrängen und kritische L2-Regionen für B-Zell-Rezeptoren verdecken könnten, was die Immunantwort abschwächt, obwohl formal mehr Antigenkopien vorhanden sind.
"Click-on"-Dekoration steigert die Reaktionen dramatisch
Um diese strukturellen Beschränkungen zu überwinden, wechselte das Team zu einem modularen „Protein‑Kleber“-System namens DogTag/DogCatcher. In diesem Design wurde Dodecin zunächst nur mit einem winzigen DogTag‑Peptid an seiner Oberfläche produziert, sodass es frei zu sauberen Nanopartikeln assembleiren konnte. Separat wurde das Trx-8mer-Antigen an den passenden DogCatcher‑Partner gefügt. Beim Mischen verriegeln Tag und Catcher über eine spontane kovalente Bindung, sodass die L2‑tragenden Trx-8mer‑Einheiten an die vorgeformten Dodecin‑Partikel geschnappt werden. Obwohl nur etwa die Hälfte der Trx-8mer an die Nanopartikel gebunden war und der Rest frei in Lösung blieb, erzeugten Mäuse, die mit diesem dekorierten Konstrukt immunisiert wurden, deutlich höhere neutralisierende Antikörpertiter gegen mehrere Hochrisiko‑HPV‑Typen als mit den direkt gefuseten Partikeln. Bei einigen Typen, etwa HPV16, übertrafen die dekorierten Partikel sogar PANHPVAX.
Folgen für erschwingliche, breite HPV-Impfstoffe
Insgesamt zeigt die Studie, dass die räumliche Anordnung von Antigenen wichtiger sein kann als die bloße Anzahl der Kopien auf dem Papier. Ein robustes Nanopartikel‑Gerüst vorzubilden und anschließend Antigene aufzuschnappen führte zu vorteilhafterer Abstandshaltung und Orientierung der L2‑Fragmente und erzeugte stärkere sowie breiter wirkende Antikörperantworten in Mäusen. Da die dodecinbasierten Partikel klein, hoch thermostabil und in Bakterien herstellbar sind, stellen sie vielversprechende Kandidaten für Impfstoffe der nächsten Generation dar, die kostengünstiger produziert werden könnten und weniger auf Kühlketten angewiesen wären. Mit weiterer Verfeinerung und Prüfung könnte diese modulare Plattform Impfstoffe unterstützen, die in einer einzigen, zugänglichen Injektion gegen viele HPV‑Typen schützen und möglicherweise sogar präventive und therapeutische Komponenten in demselben Nanopartikel kombinieren.
Zitation: Kaplan, E., Mariz, F.C., Zhao, X. et al. Assessment of Mycobacterium tuberculosis dodecin scaffold as a multimerization platform on the immunogenicity of HPV L2 antigens. Sci Rep 16, 9086 (2026). https://doi.org/10.1038/s41598-026-42678-7
Schlüsselwörter: HPV-Impfstoff, Nanopartikel-Immunogen, L2-Antigen, Dodecin-Gerüst, Protein-Konjugation