Clear Sky Science · de
Kartierung nächtlicher Erregung bei Schlaf- und Schmerzstörungen
Warum unruhige Nächte wichtig sind
Die meisten von uns denken an Schlaf als einen ruhigen, gleichmäßigen Zustand, doch unter der Oberfläche justiert das Gehirn ständig, wie tief wir ruhen. Kleine Aktivitätsausbrüche — kurze „Regungen“, die uns nicht vollständig wecken — tragen dazu bei, den Schlaf stabil zu halten. Diese Studie fragt, wie sich diese verborgenen Regungen über die Nacht in mehreren Zuständen entfalten, die mit gestörtem Schlaf verbunden sind: eine Bewegungsstörung beim Träumen, Narkolepsie, Nachtangst und Schlafwandeln sowie die chronische Schmerzerkrankung Fibromyalgie. Indem die Autoren diesen Moment‑für‑Moment‑Veränderungen folgen, statt nur die Stunden in den einzelnen Schlafstadien zu zählen, hoffen sie Muster aufzudecken, die eines Tages Diagnose und Behandlung leiten könnten.
Der verborgene Rhythmus im Tiefschlaf
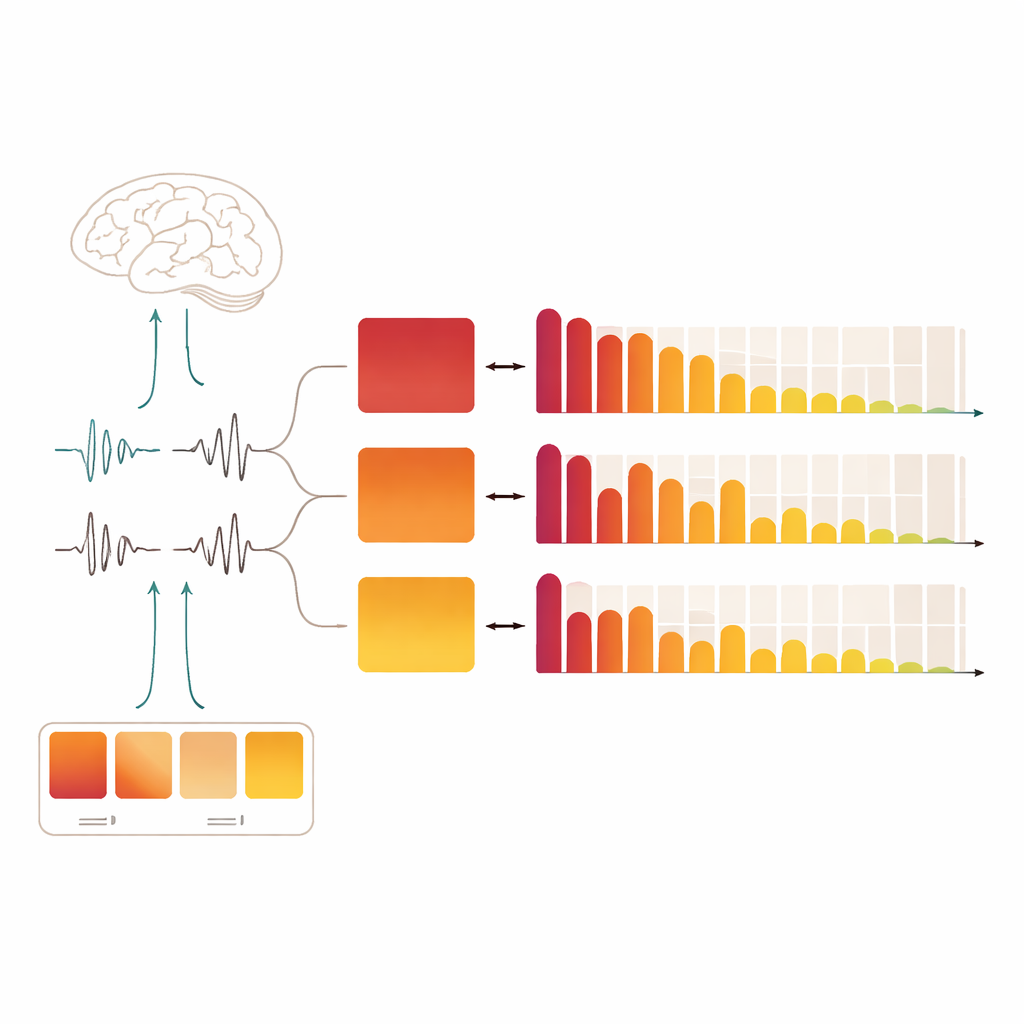
Im Non‑Rapid‑Eye‑Movement‑Schlaf (non‑REM) wechselt das Gehirn zwischen ruhigeren Phasen und kurzen Aktivitätsaufblühungen. Schlafforscher bezeichnen dies als zyklisches Alternationsmuster: kurze „A‑Phasen“ der Aktivierung, gefolgt von ruhigeren „B‑Phasen“. Innerhalb der A‑Phasen treten drei Varianten auf. Der erste Subtyp, A1, ist stark mit langsamen, hochamplitudigen Gehirnwellen verbunden und gilt als stabilisierend für den Tiefschlaf. Die zweite und dritte Variante, A2 und A3, spiegeln jeweils stärkere Aktivierung wider und rücken das Gehirn näher an das Wachwerden. Anstatt diese Ereignisse als zufälliges Rauschen zu betrachten, sehen neuere Arbeiten sie als einen zentralen Teil davon, wie das Gehirn das Schlafen mit der Fähigkeit, auf die Umwelt zu reagieren, austariert.
Eine neue Methode, nächtliche Erregung zu verfolgen
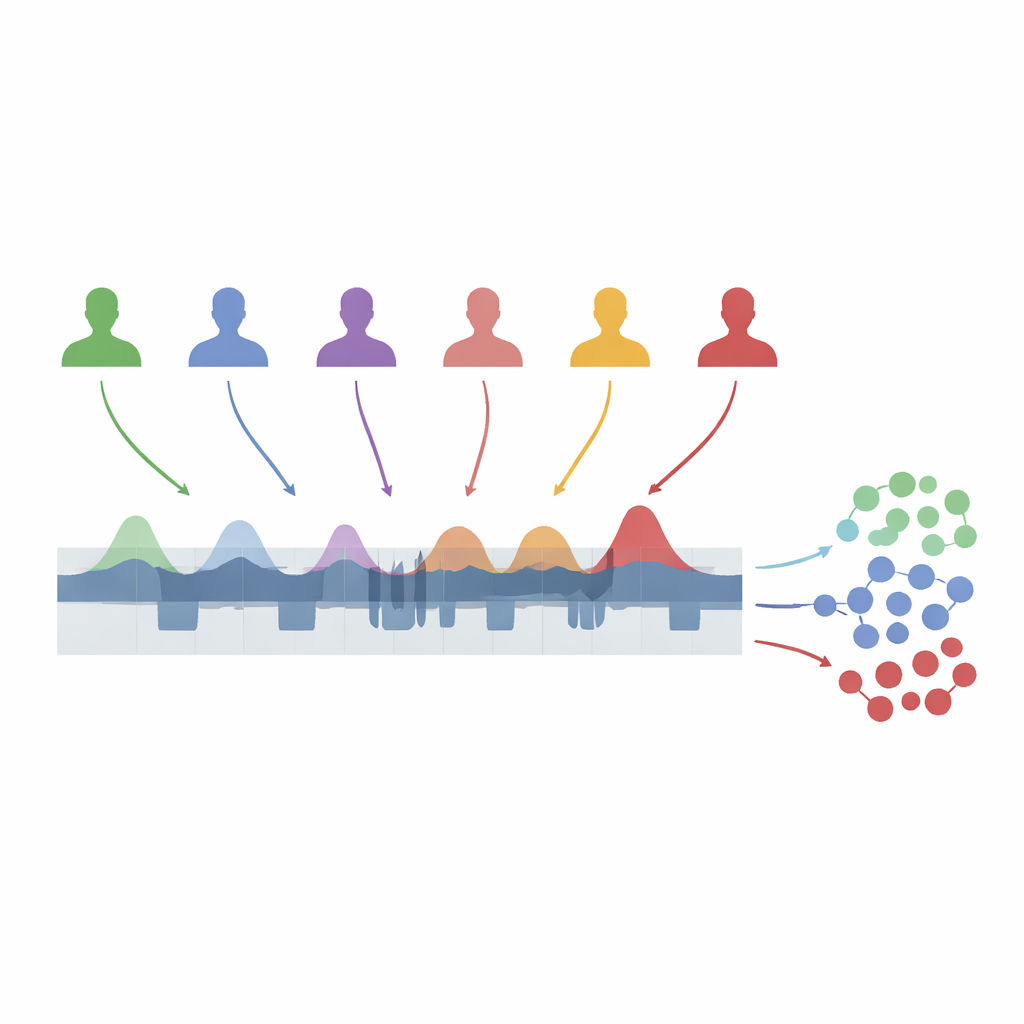
Das Team analysierte nächtliche EEG‑Aufzeichnungen von 109 Erwachsenen: gesunden Freiwilligen und Patientinnen und Patienten mit idiopathischer REM‑Schlaf‑Verhaltensstörung, Narkolepsie Typ 1, non‑REM‑Parasomnien und Fibromyalgie. Mit einem automatisierten Algorithmus, der an Experten‑markierten Daten trainiert wurde, erfassten sie jeden Moment, in dem das Gehirn während des non‑REM‑Schlafs in A1, A2 oder A3 wechselte. Anschließend teilten sie die Nacht jeder Person in einminütige Abschnitte und berechneten für jeden Abschnitt, welchen Anteil der Zeit jede Subtyp einnahm. Dieser „A‑Phasen‑Index“ liefert eine laufende Messung, wie stark das Gehirn kurzzeitig aktiviert wird, ohne zu versuchen, jeden vollständigen Zyklus von Aktivierung und Ruhe nachzubilden. Um Personen mit sehr unterschiedlichen Zubettgeh‑ und Aufwachzeiten vergleichbar zu machen, streckten die Autoren jede Nacht auf eine Standardskala von Licht aus bis Licht an.
Wie verschiedene Störungen den nächtlichen Verlauf umformen
Bei gesunden Schläfern waren A1‑Ereignisse früh in der Nacht am häufigsten, wenn der Schlafdruck hoch ist, und nahmen dann kontinuierlich bis zum Morgen ab. Das passt zur Vorstellung, dass starke, langsame Wellen die frühen Zyklen des Tiefschlafs stabilisieren und mit fortschreitender Erholung des Gehirns weniger benötigt werden. Über alle Teilnehmergruppen hinweg waren A2 und A3 weniger ausgeprägt und veränderten sich im Zeitverlauf moderater. Im Gegensatz dazu zeigten alle vier klinischen Gruppen eine abgeschwächte Version des gesunden A1‑Musters. Menschen mit REM‑Schlaf‑Verhaltensstörung und solche mit Narkolepsie hatten deutlich weniger A1‑ und A2‑Ereignisse in der mittel‑tiefen Non‑REM‑Phase, und bei der REM‑Schlaf‑Verhaltensstörung fehlte A1 außerdem in der tiefsten Phase. Bei Fibromyalgie zeigte sich ein breiter Rückgang von sowohl A1 als auch A2, insbesondere in dieser mittel‑tiefen Phase. Non‑REM‑Parasomnien hoben sich ab: Sie zeigten einen frühen Nachtanstieg von A1 und A2 im leichten Schlaf, später jedoch eine Reduktion von A1 im Tiefschlaf. Zusammengenommen deuten diese Profile darauf hin, dass jede Störung ihren eigenen „Fingerabdruck“ hat, wie die kurzzeitigen Erregungs‑Ausbrüche des Gehirns durch die Nacht gewebt sind.
Was die Muster für das Gehirn bedeuten könnten
Diese störungsspezifischen Fingerabdrücke weisen auf unterschiedliche Arten von Ungleichgewicht zwischen Systemen hin, die tiefe, erholsame langsame Wellen fördern, und Systemen, die das Gehirn zur Erregung treiben. Reduzierte A1‑ und A2‑Muster bei REM‑Schlaf‑Verhaltensstörung und Narkolepsie könnten eine schwächere Rekrutierung stabilisierender Slow‑Wave‑Antworten widerspiegeln, wodurch der Schlaf fragiler wird, selbst wenn die Gesamtzeit des Tiefschlafs normal erscheint. Bei Parasomnien passt die Mischung aus zusätzlicher Aktivierung im leichten Schlaf und schwächerer Pufferung im Tiefschlaf zu der Idee instabiler Grenzen zwischen Schlaf‑ und Wachzuständen, was zu dramatischen Verhaltensweisen wie Schlafwandeln führen kann. Bei Fibromyalgie könnte der weitreichende Verlust von A1 und A2 erklären, warum Schlaf trotz scheinbar normaler Tiefschlafmengen nicht erholsam wirkt: die feingliedrige, schützende Mikrostruktur ist verändert und macht möglicherweise empfindlicher für Schmerz und andere Empfindungen.
Von beschreibenden Karten zu zukünftigen Schlafwerkzeugen
Die Autoren betonen, dass ihre Arbeit explorativ ist: Die Gruppengrößen waren moderat, die gesunden Freiwilligen nicht perfekt an die Patientengruppen angepasst, und sie konzentrierten sich nur auf die aktiven A‑Phasen, nicht auf die vollständigen Zyklen, die auch die ruhigeren B‑Phasen einschließen. Dennoch zeigen die Ergebnisse, dass das Folgen des Anstiegs und Abfalls kurzer Erregungsereignisse über die Nacht charakteristische Signaturen verschiedener Schlaf‑ und Schmerzstörungen offenlegen kann. Wenn diese Befunde in größeren, prospektiven Studien bestätigt werden, könnte diese Art der nächtlichen Kartierung zu neuen Biomarkern beitragen — objektiven Messgrößen, die helfen, Patienten zu klassifizieren, den Krankheitsverlauf zu verfolgen und Behandlungen zu steuern, die das Gleichgewicht zwischen Stabilität und Erregung im Schlaf feinjustieren, anstatt die Patienten einfach nur „auszuschalten“.
Zitation: Biabani, N., Mendonça, F., Mutti, C. et al. Mapping nocturnal arousal across sleep and pain disorders. Sci Rep 16, 8668 (2026). https://doi.org/10.1038/s41598-026-42639-0
Schlüsselwörter: Mikrostruktur des Schlafs, nächtliche Erregung, zyklisches Alternationsmuster, Schlafstörungen, Fibromyalgie und Schlaf