Clear Sky Science · de
Entdeckung natürlicher Apigenin-Analoga als Inhibitoren der lysin-spezifischen Demethylase 1 gegen tumorelle Keimzelltumoren des Hodens
Warum diese Forschung für die Gesundheit von Männern wichtig ist
Keimzelltumoren des Hodens sind die häufigsten Hodentumoren bei jungen Männern. Zwar können viele Patientinnen und Patienten geheilt werden, doch bedrohen die aktuellen Behandlungen oft die Fruchtbarkeit und gehen mit schweren Nebenwirkungen einher. In dieser Studie wird untersucht, ob eine natürliche Verbindung, die mit dem Pflanzenfarbstoff Apigenin verwandt ist und in Obst und Gemüse vorkommt, zu einem präziseren Wirkstoff entwickelt werden kann, der das Wachstum von Hodentumorzellen verlangsamt, während gesundes Hodengewebe geschont bleibt.
Eine natürliche Idee aus alltäglichen Pflanzen
Apigenin ist ein gelber Pflanzenfarbstoff, der in Lebensmitteln wie Petersilie, Sellerie und Kamille vorkommt. Chemiker wissen seit langem, dass es das Verhalten von Zellen beeinflussen kann, doch sein Potenzial gegen Keimzelltumoren des Hodens war bisher unerforscht. Die Autorinnen und Autoren begannen damit, eine kleine Bibliothek natürlich vorkommender Apigenin-ähnlicher Moleküle zusammenzustellen. Sie konzentrierten sich auf ein Protein namens LSD1, ein Enzym, das durch subtile Modifikationen der DNA-verpackenden Proteine mitbestimmt, welche Gene an- oder abgeschaltet werden. Da LSD1 in mehreren Krebsarten, einschließlich Keimzelltumoren des Hodens, übermäßig hoch vorhanden ist, ist die Blockade dieses Enzyms eine vielversprechende Strategie zur Verlangsamung des Tumorwachstums.
Das effektivste pflanzenbasierte Blocker-Molekül finden
Die Forschenden testeten systematisch sechzehn natürliche Apigenin-Analoga, um zu prüfen, wie stark jedes einzelne LSD1 im Reagenzglas hemmen konnte. Viele Verbindungen zeigten eine gewisse Wirkung, doch eine stach hervor: eine Variante namens 8,3'-Diprenylapigenin war der potenteste Inhibitor und wirkte in niedrigen Mikromolarkonzentrationen. Durch den Vergleich der chemischen Eigenschaften aller Apigenin-Analoga kartierte das Team, welche kleinen strukturellen Änderungen die Enzymhemmung verstärkten oder abschwächten. Sie fanden heraus, dass eine bestimmte chemische Gruppe, die 7-Hydroxy-Gruppe, besonders wichtig für das Festhalten an LSD1 ist und dass das Anbringen sperriger „Prenyl“-Seitenketten an bestimmten Positionen die Potenz deutlich erhöhte.
Wie die neue Verbindung Tumorzellen anvisiert
Im nächsten Schritt gingen die Forschenden von Enzymtests zu lebenden Zellen über. Sie setzten menschliche Keimzelltumorzelllinien, genannt NCCIT und NTERA-2, 8,3'-Diprenylapigenin aus. Die Verbindung reduzierte die Teilungsfähigkeit der Zellen deutlich, wiederum in relativ niedrigen Konzentrationen. Im Gegensatz dazu blieben bei denselben Dosierungen zwei normale Hoden-Zelllinien, TM3 und TM4, kaum betroffen. Diese Selektivität deutet darauf hin, dass Tumorzellen, die stark von überaktivem LSD1 abhängig sind, viel anfälliger für dessen Hemmung sind als normale Zellen — ein ermutigendes Zeichen für mögliche zukünftige Therapien.
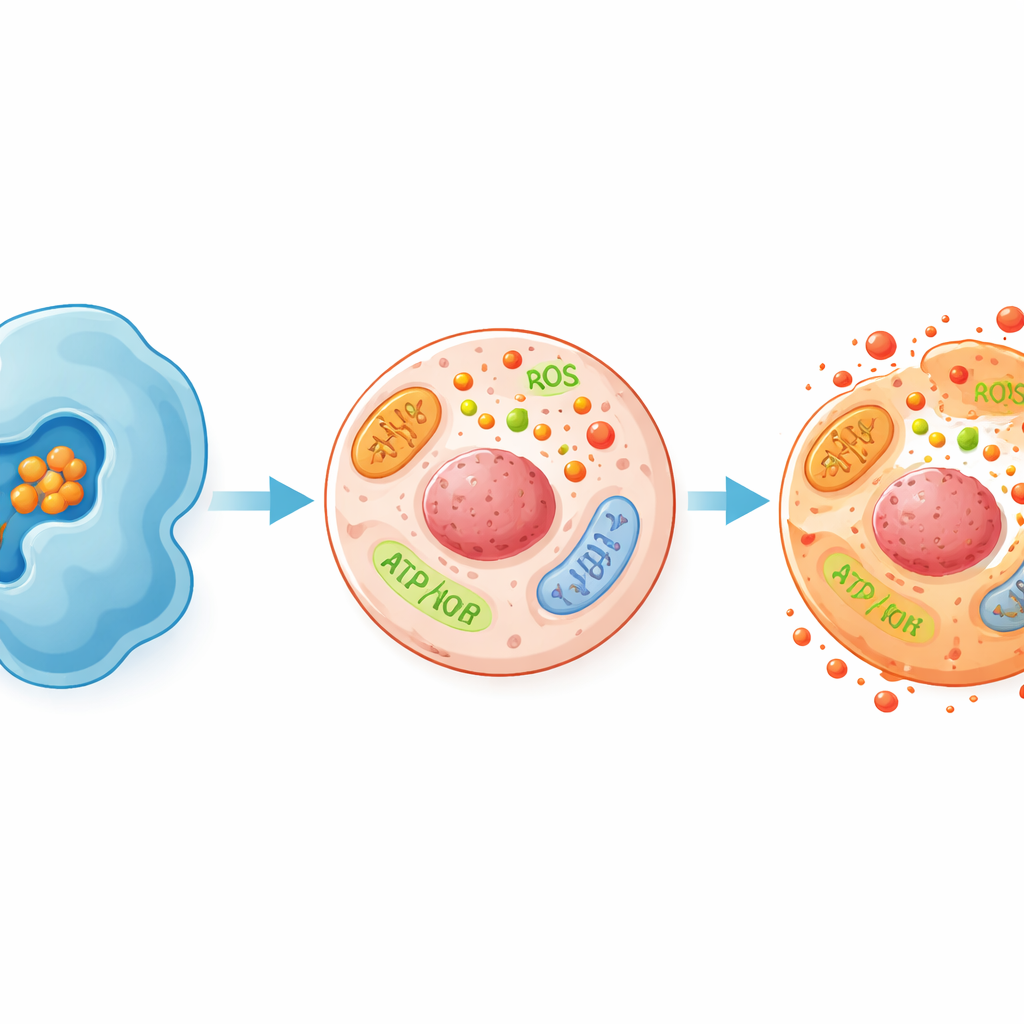
Ein Blick in die Stressantwort der Zelle
Um zu verstehen, was in Tumorzellen passiert, wenn LSD1 durch 8,3'-Diprenylapigenin blockiert wird, maßen die Wissenschaftler mehrere Marker zellulären Stresses. Sie fanden heraus, dass behandelte NTERA-2-Zellen mehr reaktive Sauerstoffspezies produzierten — hochreaktive Moleküle, die Proteine, Fette und DNA schädigen können. Gleichzeitig ging die Aktivität von Katalase, einem schützenden Enzym, das schädliche Oxidantien abbaut, zurück. Auch die zelluläre Energieeinheit ATP sank, was auf eine beeinträchtigte Energieproduktion hinweist. Weitere Schadensanzeichen, darunter das Austreten des Enzyms LDH aus Zellen, erhöhte Aktivität des antioxidativen Enzyms SOD und höhere Werte des Lipid-Schadensmarkers MDA, stiegen alle dosis- und zeitabhängig an. Zusammengenommen zeichnen diese Veränderungen das Bild von Tumorzellen, die in einen oxidativen Stress geraten, den sie nicht bewältigen können, was schließlich zu ihrem Absterben führt.
Vom molekularen Sitz zur möglichen zukünftigen Medizin
Computersimulationen halfen zu erklären, warum 8,3'-Diprenylapigenin so gut wirkt. Docking- und Dynamikstudien zeigten, wie die Verbindung sich passgenau in eine Tasche von LSD1 einfügt und stabilisierende Wasserstoffbrücken sowie hydrophobe Kontakte bildet, dabei jedoch reversibel bindet. Diese Reversibilität ist wichtig, weil einige frühere, irreversible LSD1-Blocker in Studien Blut- und Immunnebenwirkungen verursacht haben. Hier hemmte 8,3'-Diprenylapigenin LSD1 stark und selektiv, ohne eng verwandte Enzyme wie MAO-A und MAO-B signifikant zu beeinflussen, was das Risiko unerwünschter Wirkungen im Gehirn und anderen Geweben reduziert.
Was das für Patientinnen und Patienten bedeuten könnte
Einfach gesagt identifiziert diese Arbeit ein pflanzliches Molekül, das gezielt ein krebsassoziiertes Enzym in Hodentumorzellen anvisieren, deren Wachstum stoppen und einen kontrollierten Zelltod auslösen kann, während normale Hoden-Zellen in Labortests weitgehend verschont bleiben. Obwohl noch viel Forschung nötig ist — einschließlich Tierversuchen und Sicherheitsprüfungen am Menschen — bietet 8,3'-Diprenylapigenin ein vielversprechendes Anfangsgerüst für die Entwicklung schonenderer, gezielterer Behandlungen von Keimzelltumoren des Hodens, die Fruchtbarkeit und allgemeine Gesundheit besser schützen könnten.
Zitation: Sun, LW., Zhang, M., Li, CF. et al. Discovery of natural apigenin analogues as lysine-specific demethylase 1 inhibitors against tumoral testicular germ cells. Sci Rep 16, 8917 (2026). https://doi.org/10.1038/s41598-026-42263-y
Schlüsselwörter: Hodenkrebs, LSD1-Inhibitoren, Apigenin, oxidativer Stress, zielgerichtete Therapie