Clear Sky Science · de
GV1001 reduziert pathologisches 4R-Tau und funktionelle Defizite in Modellen, die für progressive supranukleäre Blickparese relevant sind
Warum das für Betroffene und Familien wichtig ist
Die progressive supranukleäre Blickparese (PSP) ist eine seltene, aber verheerende Hirnerkrankung, die Menschen innerhalb weniger Jahre Gleichgewicht, Bewegung und klares Denken raubt. Es gibt derzeit keine Medikamente, die das Fortschreiten wirksam verlangsamen. Diese Studie untersucht ein kleines Wirkstoffmolekül namens GV1001, das ursprünglich für die Krebstherapie entwickelt wurde, und zeigt, dass es in Labor-Modellen der PSP Bewegungsprobleme lindern und krankheitsrelevante Veränderungen in Gehirnzellen reduzieren kann. Die Arbeit deutet auf einen neuen Weg hin, eine Gruppe von Erkrankungen anzugehen, die von einer schädlichen Form des Proteins Tau getrieben werden.
Der Helfer des zellulären Transports gerät außer Kontrolle
Viele Hirnerkrankungen betreffen Tau, ein Protein, das normalerweise hilft, die internen „Schienen“ zu stabilisieren, entlang derer Materialien in Nervenzellen transportiert werden. Bei PSP sammelt sich eine bestimmte Form, das sogenannte 4R-Tau, in tiefen Hirnregionen an, insbesondere im Mittelhirn, wo es die Zellstruktur stört, Verbindungen beschädigt und schließlich zum Zelltod führt. Betroffene entwickeln Steifheit, Stürze, Blickbewegungsstörungen und Denkprobleme und verschlechtern sich häufig schnell über fünf bis acht Jahre. Im Gegensatz zur Alzheimer-Krankheit dominiert bei PSP diese 4R-Tau-Form, was sie zu einem wichtigen Ziel für Therapien macht, die speziell auf bewegungsbezogene Tau-Erkrankungen ausgerichtet sind.
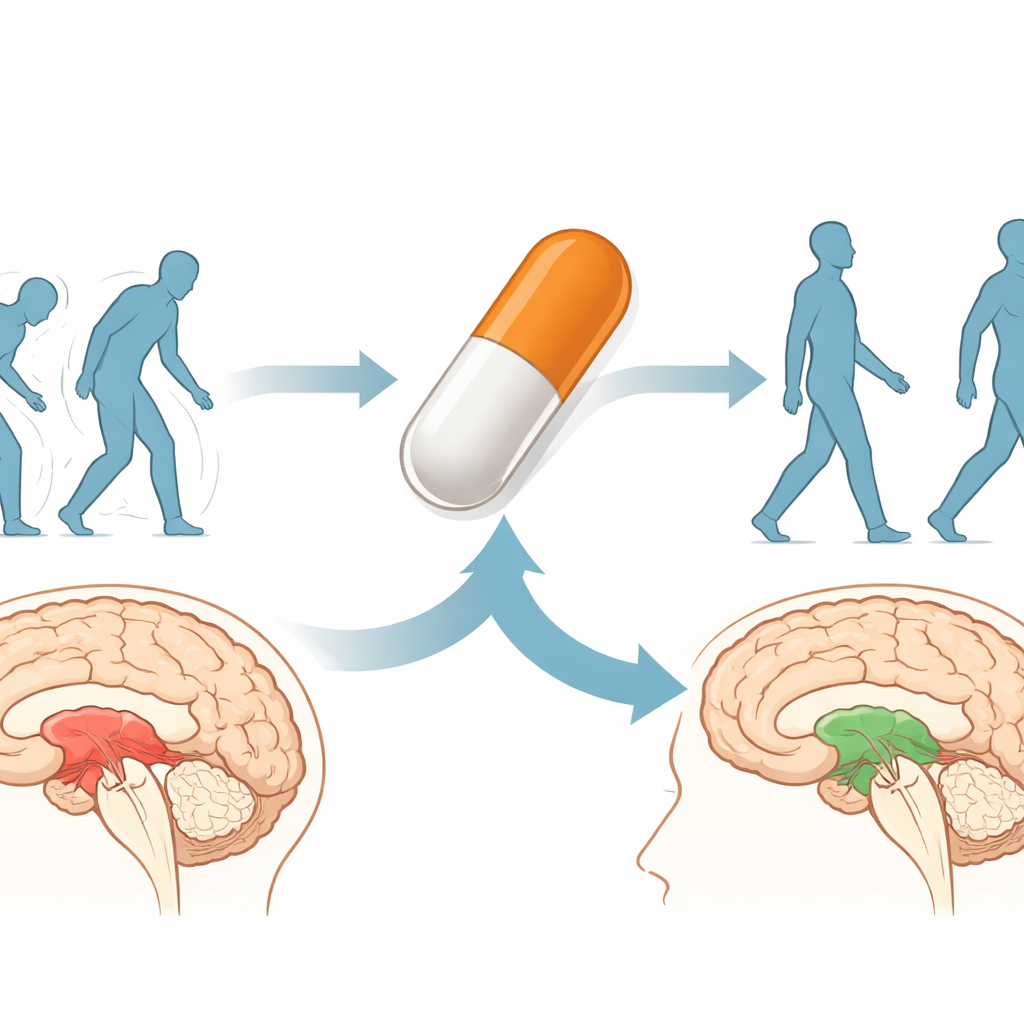
Ein Krebswirkstoffkandidat findet eine neue Rolle
GV1001 ist ein kurzes Peptid, das von der menschlichen Telomerase abgeleitet ist, einem Enzym, das in vielen Tumoren aktiv ist. Es wurde bereits gegen verschiedene Tumore und neuerdings bei Erkrankungen wie Prostatavergrößerung und Alzheimer untersucht und weist insgesamt eine gute Verträglichkeit auf. Frühere Arbeiten zeigten, dass GV1001 Nervenzellen vor oxidativem Schaden schützen, die energieproduzierenden Mitochondrien unterstützen und entzündliche Reaktionen im Gehirn dämpfen kann. Die aktuelle Studie fragt, ob diese breiten schützenden Wirkungen sowie mögliche neue Effekte GV1001 für Erkrankungen nützlich machen könnten, bei denen 4R-Tau die Hauptursache ist, wie etwa PSP.
Prüfung von Bewegung, Gedächtnis und Hirnveränderungen bei Mäusen
Die Forschenden verwendeten eine speziell gezüchtete Maus, die ein menschlich-ähnliches 4R-Tau produziert, das zur Aggregation neigt und im Laufe der Zeit zu Bewegungs- und Gedächtnisstörungen führt. Ab einem Alter von sieben Monaten erhielten diese Mäuse GV1001 dreimal wöchentlich unter die Haut für etwa fünf Monate. Im Vergleich zu unbehandelten Tieren blieben GV1001-behandelte Mäuse länger auf einem rotierenden Balken, liefen weiter und schneller in einer offenen Arena und zeigten eine bessere Erkennung neuer Objekte, was auf verbesserte motorische Fähigkeiten und Gedächtnis schließen lässt. Bei der Untersuchung der Gehirne fanden die Forschenden weniger Tau-Aggregate und weniger chemische Markierungen, die mit „überaktivem“ Tau assoziiert sind, in mehreren Regionen, darunter Cortex, Hippocampus und Substantia nigra — alles Bereiche, die für Bewegung und Kognition wichtig sind.
Blick in die Zellen und Beruhigung der Gehirnentzündung
Über Tau hinaus zeichnen sich PSP und verwandte Erkrankungen durch Verlust von Synapsen — den Kontaktpunkten zwischen Nervenzellen — sowie Überaktivierung von Stütz-Zellen namens Astrozyten und Mikroglia aus, die chronische Entzündung antreiben. Bei den behandelten Mäusen kehrten die Spiegel wichtiger synaptischer Proteine teilweise wieder in Richtung Normalwerte zurück, was darauf hindeutet, dass GV1001 neuronale Verbindungen schützt. Marker aktivierter Astrozyten und Mikroglia sanken sowohl in Mausgehirnen als auch in menschlichen Zelllinien, die zur Nachahmung einer Entzündung stimuliert wurden. Das Medikament verringerte außerdem die Konzentration von TSPO, einem Protein, das in Hirnscans zur Überwachung von Entzündung verwendet wird, sodass künftige Bildgebungsverfahren möglicherweise das Ansprechen auf GV1001 bei Patientinnen und Patienten verfolgen könnten.
Direktes Ansteuern der schädlichen 4R-Tau-Form
Um zu prüfen, ob GV1001 die 4R-Tau-Form spezifischer beeinflusst, erstellte das Team ein zellbasiertes PSP-Modell, indem es menschlich-abgeleitete, nervenähnliche Zellen differenzierte und sie Annonacin aussetzte, einem pflanzlichen Toxin, das Mitochondrien schädigt und 4R-Tau erhöht. Wie erwartet stieg durch Annonacin die Menge an 4R-Tau stark an, ohne das Gesamt-Tau zu verändern. Wurde GV1001 nach Einsetzen dieses Schadens hinzugefügt, fielen die überschüssigen 4R-Tau-Spiegel und das Verhältnis von 4R-Tau zu Gesamt-Tau wieder in Richtung Normalwerte, während sich das gesamte Tau weitgehend unverändert zeigte. Ähnliche selektive Reduktionen von 4R-Tau wurden in den Gehirnen der behandelten Mäuse beobachtet. Diese Befunde legen nahe, dass GV1001 mehr leistet als einen allgemeinen Zellschutz — es scheint gerade jene Tau-Form herunterzuregeln, die am engsten mit PSP verbunden ist.
Was das für zukünftige Behandlungen bedeuten könnte
In der Summe zeigen die Ergebnisse, dass GV1001 in Modellen, die zentrale Aspekte von PSP und anderen 4R-Tau-getriebenen Erkrankungen nachbilden, Bewegung und Gedächtnis verbessern, toxische Tau-Veränderungen reduzieren, Synapsen erhalten und Gehirnentzündungen dämpfen kann. Erste klinische Tests bei Menschen mit PSP deuten bereits auf ein langsameres Fortschreiten der Symptome und gute Verträglichkeit hin, obwohl deutlich größere und längere Studien erforderlich sind. Für Patientinnen, Patienten und Familien bietet diese Arbeit vorsichtigen Optimismus, dass ein ursprünglich für die Krebstherapie entwickeltes Medikament umgenutzt werden könnte, um den Verlauf einer schnell voranschreitenden Hirnerkrankung zu verlangsamen, indem es die zugrundeliegende Proteinfehlregulation adressiert.
Zitation: Jang, KB., Kang, D.M., Lee, MH. et al. GV1001 reduces pathological 4R tau and functional deficits in models relevant to progressive supranuclear palsy. Sci Rep 16, 8638 (2026). https://doi.org/10.1038/s41598-026-42195-7
Schlüsselwörter: progressive supranukleäre Blickparese, Tau-Protein, 4R-Tauopathie, Neuroinflammation, GV1001