Clear Sky Science · de
Multizentrische klinisch-pathologische Studie zu Läsionen des Spektrums des odontogenen Myxoms mittels quantitativer Pathologie
Warum das für Patientinnen, Patienten und Zahnärzte wichtig ist
Tief im Kieferknochen können seltene Tumoren über Monate oder Jahre unbemerkt wachsen, bevor sie entdeckt werden. Diese Wucherungen, genannt odontogene Myxome und Myxofibrome, sind keine Krebsarten, können jedoch an Größe zunehmen, Knochen schwächen und Operationen erschweren. Jahrzehntelang bewerteten Pathologen sie überwiegend mit bloßem Auge, was dazu führte, dass Krankenhäuser dasselbe Läsionsbild unterschiedlich beschrieben und klassifiziert haben. Diese Studie bringt leistungsfähige Bildanalyse‑Werkzeuge auf den Objektträger und zeigt, wie künstliche Intelligenz (KI) Ärzten helfen kann, diese Tumoren klarer und konsistenter zu erkennen.
Seltene Kiefertumoren mit täuschender Ähnlichkeit
Das odontogene Myxom und das odontogene Myxofibrom entstehen aus Geweben, die an der Zahnentwicklung beteiligt sind. Beide sind weiche, geleeartige Tumoren, die im Kieferknochen liegen. Unter dem Mikroskop enthalten sie eine Mischung aus lockeren, myxoid erscheinenden Bereichen und dichteren fibrösen Strängen. Klassischerweise versuchen Pathologen, sie durch eine Schätzung des Verhältnisses von fibrösem zu myxoidem Gewebe zu unterscheiden. Diese Tumoren sind jedoch selten, und es gibt keine allgemein akzeptierten Regeln dafür, wie viel fibröses Gewebe erforderlich ist, um eine Diagnose von der einen auf die andere Bezeichnung zu verlagern. Folglich können in verschiedenen Kliniken sehr ähnliche Läsionen unterschiedlich benannt werden, selbst wenn Patientinnen und Patienten vergleichbare Symptome und Bildbefunde zeigen.
Mikroskopische Schnitte in Zahlen verwandeln
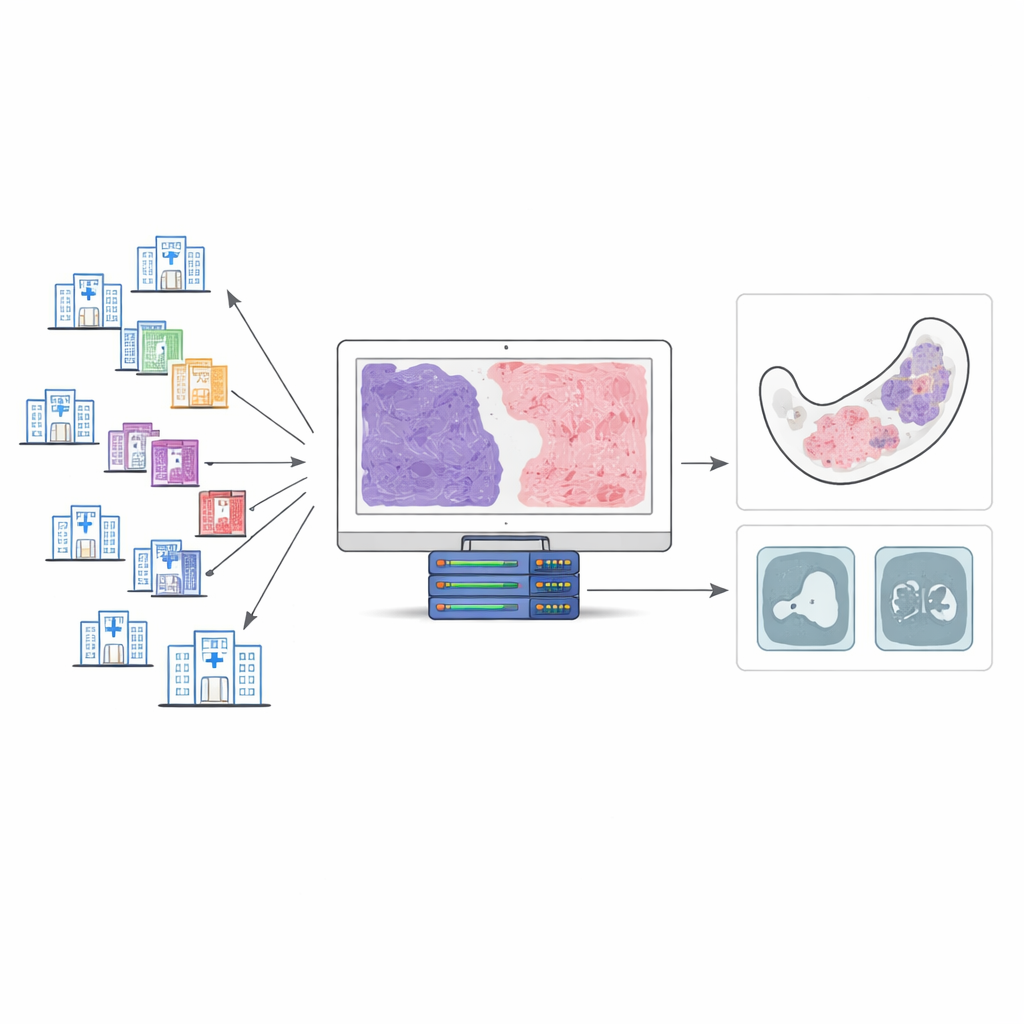
Das Forscherteam sammelte 143 Gewebeproben von Patientinnen und Patienten, die in 34 Krankenhäusern über zwei Jahrzehnte behandelt worden waren, und konzentrierte sich schließlich auf 100 Fälle, die strenge Qualitätskriterien erfüllten. Alle Proben wurden mit einer speziellen Färbung (Masson‑Trichrom) behandelt, die fibröses Gewebe vom umgebenden Tumor farblich unterscheidet. Zwei erfahrene Mund‑ und Kieferpathologen überprüften jeden Fall sorgfältig und schätzten den Anteil fibrösen Gewebes in 10‑Prozent‑Schritten. Diese Expertenbewertungen dienten als Referenz, um ein KI‑System zu trainieren, dieselbe Aufgabe automatisch und vollständig quantitativ durchzuführen.
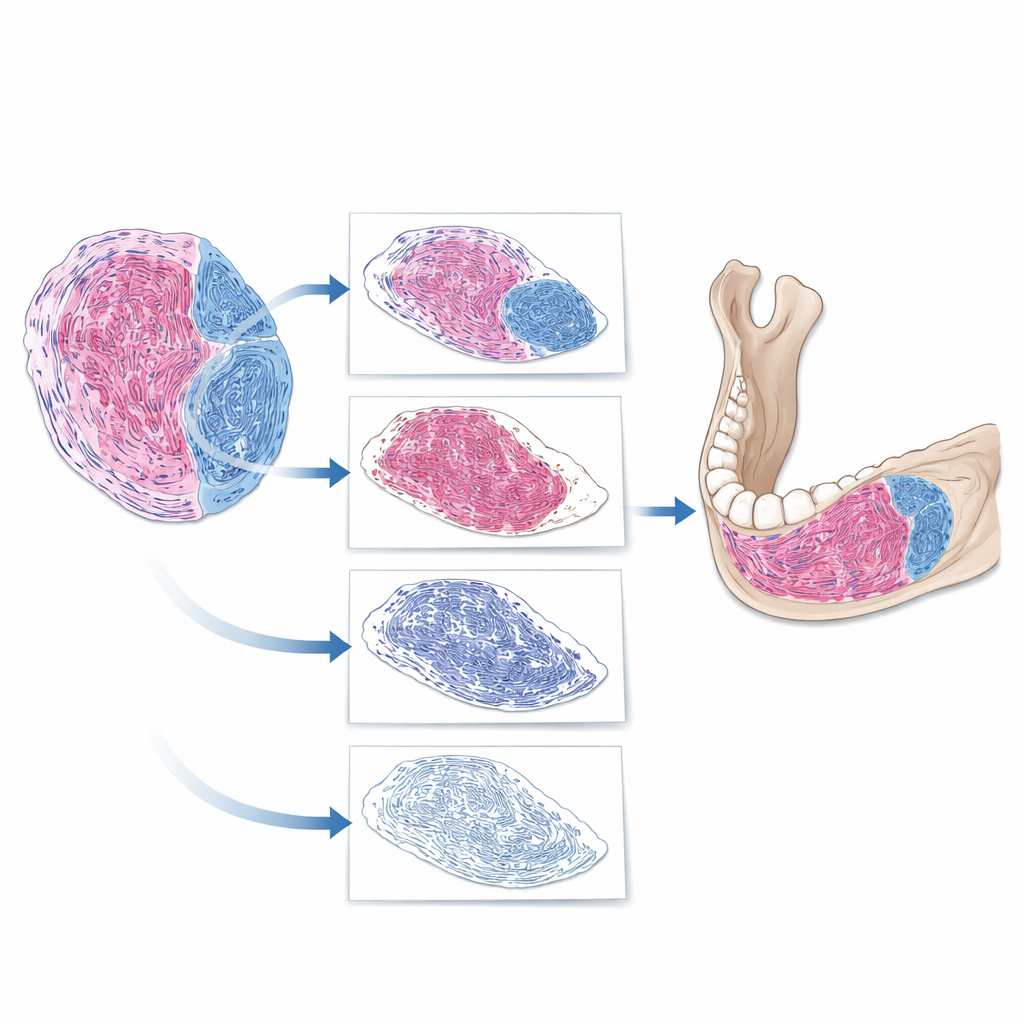
Wie die KI eine Tumorfolie "liest"
Das Team entwickelte eine schrittweise digitale Pipeline zur Analyse kompletter Objektträgerbilder. Zuerst trennte die Software echtes Gewebe vom leeren Hintergrund auf dem Objektträger. Anschließend isolierte sie den Tumor von nahen Strukturen wie Knochen und Zähnen. Schließlich entfernte sie innerhalb des Tumors die Zellkerne und konzentrierte sich auf das verbleibende Material, wobei Regionen identifiziert wurden, die die fibröse Färbung aufnahmen. Daraus berechnete die KI einen Anteil fibrösen Gewebes: die Fläche des fibrösen Gewebes geteilt durch die Gesamtfläche des Tumors. Beim Vergleich der KI‑generierten Werte mit den Experteneinschätzungen zeigte sich eine starke Übereinstimmung, mit meist nur etwa zehn Prozentpunkten Streuung in einzelnen Fällen. Das deutet darauf hin, dass die KI die Expertenbeurteilung zuverlässig abbilden kann, dabei aber präzise Messwerte statt grober Eindrücke liefert.
Was die fibröse Zusammensetzung über das Tumorbild verrät
Mithilfe dieser Messungen untersuchten die Forscher, wie der fibröse Gehalt mit klinischen und radiologischen Merkmalen zusammenhängt. Sie fanden, dass der Anteil fibrösen Gewebes zwischen den Einrichtungen stark variierte, was die Unterschiede in der ursprünglichen Benennung der Tumoren widerspiegelt. Beim Blick auf die Bildgebung fiel ein Muster besonders auf: Tumoren, die in den Scans als einzelnes Hohlraumgebilde erschienen (unilokuläre Läsionen), wiesen tendenziell einen höheren Anteil fibrösen Gewebes auf als solche mit mehreren kleinen Kammern (multilokuläre Läsionen). Das passt zu der Vorstellung, dass dichteres, fibröses Gewebe eher eine solide, einkammerige Masse bildet, während lockereres, flüssigkeitsreicheres Gewebe in mehrere Räume zerfallen kann.
Was das für zukünftige Diagnose und Behandlung bedeutet
Die Studie will Krankheiten nicht umbenennen oder Pathologen durch Maschinen ersetzen. Sie zeigt vielmehr, dass KI‑basierte quantitative Pathologie einen gemeinsamen Maßstab für seltene Kiefertumoren über viele Einrichtungen hinweg liefern kann. Indem sie die subtilen Texturen von Tumorgewebe in reproduzierbare Zahlen überführt, offenbart diese Methode, wie sehr Alltagsdiagnosen von subjektiver Einschätzung abhängen, und bietet einen Weg, diese Variabilität zu reduzieren. Für Patientinnen und Patienten könnte eine konsistentere Interpretation dieser Läsionen klarere Therapieentscheidungen unterstützen und den Vergleich von Ergebnissen zwischen Zentren verbessern. Wenn ähnliche Methoden auf andere seltene Tumoren ausgeweitet werden, könnte KI‑gestützte Mikroskopie still und leise die Sichtweise der Pathologie verändern — ihre Beurteilungen vergleichbarer und letztlich nützlicher machen, unabhängig davon, wo ein Patient behandelt wird.
Zitation: Harazono, Y., Fukawa, Y., Iwasaki, T. et al. Multicenter clinicopathological study of odontogenic myxoma spectrum lesions using quantitative pathology. Sci Rep 16, 11221 (2026). https://doi.org/10.1038/s41598-026-42019-8
Schlüsselwörter: odontogenes Myxom, Kiefer-Tumoren, digitale Pathologie, künstliche Intelligenz, Anteil fibrösen Gewebes