Clear Sky Science · de
Genetische Analyse zentraler Akteure der PI3K‑Signalübertragungskaskade bei kolorektalem Karzinom
Warum Ihre Gene für die Darmgesundheit wichtig sind
Das kolorektale Karzinom gehört zu den häufigsten und tödlichsten Krebserkrankungen weltweit, und die Fallzahlen steigen in vielen Ländern mit raschem Lebensstilwandel. Dennoch hat nicht jeder mit ähnlicher Ernährung oder ähnlichen Gewohnheiten dasselbe Risiko. Diese Studie stellt eine einfache, aber folgenschwere Frage: Erklären vererbte Unterschiede in zentralen Wachstumssteuerungsgenen, wer Darmkrebs entwickelt, wie aggressiv er verläuft und wie gut Standardmedikamente wirken — insbesondere in einer großen Patientengruppe aus Pakistan, einer bisher wenig untersuchten Population?
Eine geschäftige Kontrolllinie in unseren Zellen
Die Zellen im Darm erhalten fortlaufend Signale, die ihnen sagen, wann sie wachsen, sich teilen oder selbst zerstört werden sollen. Einer der aktivsten Kommunikationswege ist die PI3K–AKT–mTOR‑Kaskade — eine Abfolge molekularer Schalter, die Zellwachstum, Überleben, Gefäßbildung und Widerstand gegen Zelltod fördert. Ist dieser Weg überaktiv, können Zellen unkontrolliert zu proliferieren beginnen und Tumore bilden. Die Gene PIK3CA, AKT1 und mTOR liegen an wichtigen Kontrollpunkten dieses Pfades. Subtile vererbbare Änderungen in diesen Genen, sogenannte Einzelnukleotid‑Polymorphismen (SNPs), sowie stärkere Veränderungen, bekannt als „Hotspot“-Mutationen, können das Gleichgewicht zugunsten von Krebs verschieben oder die Reaktion von Tumoren auf Therapien verändern.
DNA‑Screening bei Patienten und gesunden Freiwilligen
Um dies zu untersuchen, führten Forschende eine Fall‑Kontroll‑Studie mit 495 Personen mit kolorektalem Karzinom und 495 krebsfreien, nach Alter und Geschlecht abgeglichenen Freiwilligen durch. Blutproben lieferten DNA, die auf sieben SNPs in PIK3CA, AKT1 und mTOR sowie auf zwei bekannte Hotspot‑Mutationen, E542K (in PIK3CA) und E17K (in AKT1), untersucht wurde. Mit gezielten PCR‑Methoden und DNA‑Sequenzierung verglich das Team die Häufigkeit der einzelnen genetischen Varianten bei Patienten und Kontrollen und verband diese Muster anschließend mit klinischen Merkmalen wie Alter, Familienanamnese, Darmerkrankungen, Tumorstadium und den eingesetzten Medikamentenschemata. 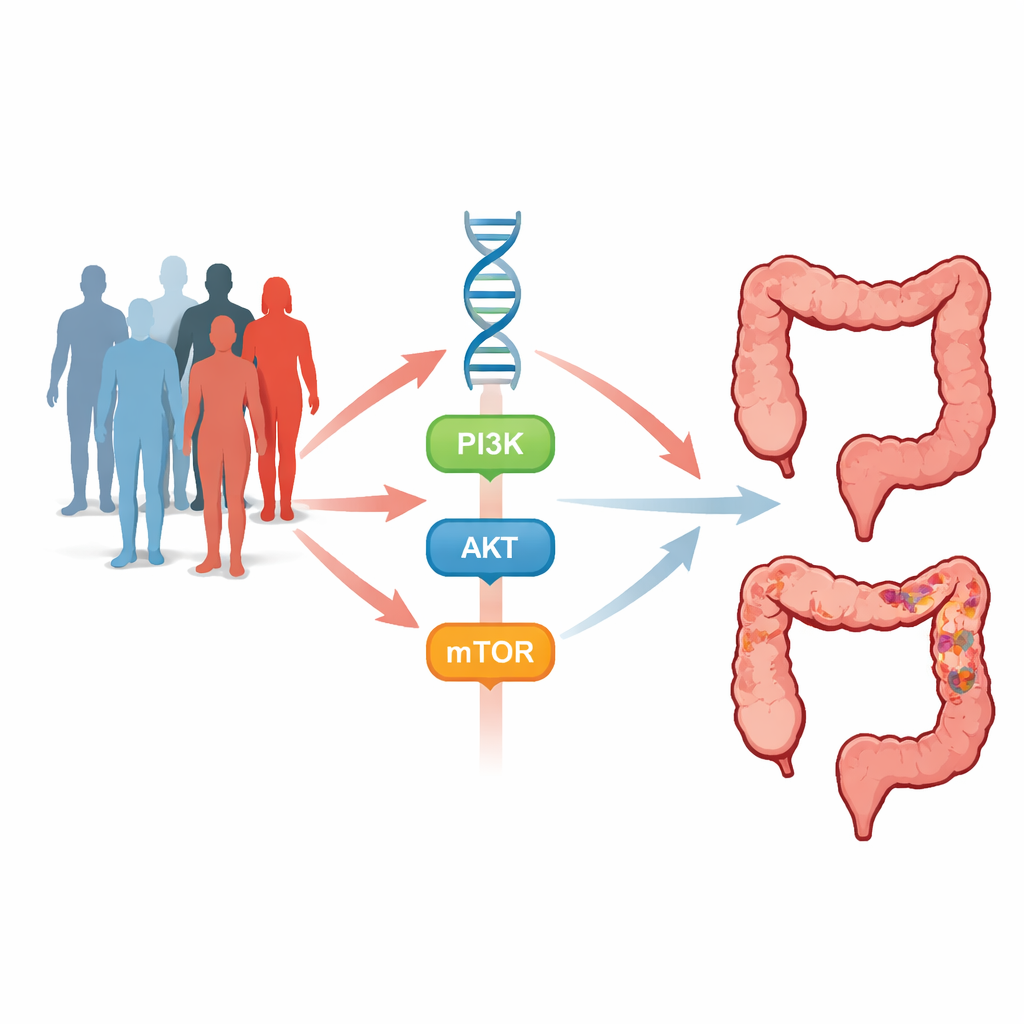
Risikobehaftete Varianten und wirkungsvolle Mutationen
Die Analyse zeigte, dass die meisten getesteten Varianten bei Menschen mit kolorektalem Karzinom deutlich häufiger vorkamen als bei gesunden Kontrollen, was stark dafür spricht, dass sie zum Erkrankungsrisiko beitragen. Mehrere Varianten in AKT1 und mTOR wiesen besonders hohe Häufigkeiten bei Patienten auf, während bestimmte „normale“ Versionen dieser Gene in den Kontrollen häufiger waren und damit auf eine schützende Rolle hindeuten. Die Hotspot‑Mutationen lieferten ein noch klareres Bild: Die E542K‑Veränderung in PIK3CA fand sich bei etwa 15 % der Patienten, die E17K‑Veränderung in AKT1 bei rund 29 %, jeweils deutlich häufiger als bei den Kontrollen. Computerbasierte Modellierungen deuteten darauf hin, dass diese Mutationen die Gesamtstruktur des Proteins nicht dramatisch verzerren, sondern den Signalweg eher in einen beständig „an“-Zustand verriegeln, was kontinuierliche Wachstumssignale fördert und die Tumorentwicklung begünstigt.
Von Genen zu Therapie und Überleben
Genetik wirkt nicht isoliert, daher untersuchten die Forschenden, wie diese Varianten mit realen Risikofaktoren und Therapien interagieren. Viele der SNPs standen in Verbindung mit Rauchen, entzündlichen Darmerkrankungen, Familienanamnese, Krebsart und -stadium sowie der Frage, ob Patienten Chemotherapie oder Strahlentherapie erhalten hatten. Bei der Nachverfolgung der Patienten über die Zeit zeigte sich, dass bestimmte Genvarianten mit besserer oder schlechterer Gesamtüberlebenszeit verknüpft waren. Beispielsweise lebten Personen mit den normalen Versionen mehrerer AKT1‑ und mTOR‑Varianten tendenziell länger als Träger der Hochrisiko‑Versionen. Die Studie verglich außerdem das Überleben unter gängigen Medikamentenkombinationen: Capecitabin, eine weitverbreitete orale Chemotherapie, ging mit den besten Überlebensschätzungen einher, und mehrere Varianten des Signalwegs schienen zu beeinflussen, wie gut unterschiedliche Schemata wirkten — ein Hinweis darauf, dass vererbte Genetik personalisierte Therapieentscheidungen leiten könnte.
Wie Veränderungen gemeinsam weitergegeben werden
Über einzelne Varianten hinaus untersuchten die Autorinnen und Autoren, wie Gruppen von Veränderungen dazu neigen, gemeinsam vererbt zu werden — ein Muster, das als Linkage Disequilibrium bezeichnet wird. Sie entdeckten einen Block benachbarter Varianten, der PIK3CA und AKT1 überspannte und bei Patienten häufiger zusammen auftrat als bei Kontrollen. Das deutet darauf hin, dass Kombinationen kleiner DNA‑Unterschiede entlang des PI3K‑Wegs gemeinsam das individuelle Grundrisiko und das Verhalten eines Tumors prägen können, statt dass eine einzelne Veränderung allein verantwortlich ist.
Was das für Patienten und Präzisionsmedizin bedeutet
Für Laien zusammengefasst bedeutet dies: Die Arbeit untermauert die Idee, dass „One size fits all“ ein ungeeignetes Modell für die Behandlung von Darmkrebs ist. In dieser pakistanischen Kohorte standen spezifische vererbte Varianten und Hotspot‑Mutationen in wachstumssteuernden Genen klar in Zusammenhang mit Krebsrisiko, Tumoreigenschaften und Überleben und schienen sogar die Behandlungsergebnisse unter Standardchemotherapien zu modulieren. Zwar müssen diese Befunde in größeren und vielfältigeren Gruppen bestätigt werden, doch sie weisen auf eine Zukunft hin, in der ein einfacher Bluttest auf PI3K–AKT–mTOR‑Varianten helfen könnte, Personen mit erhöhtem Risiko zu identifizieren, Patientinnen und Patienten zu kennzeichnen, die von bestimmten Wirkstoffen profitieren, und andere vor unwirksamen oder unnötig toxischen Behandlungen zu bewahren.
Zitation: Pervaiz, H., Masood, N., Malik, P.A. et al. Genetic analysis of key players in PI3K signaling cascade of colorectal carcinoma. Sci Rep 16, 11317 (2026). https://doi.org/10.1038/s41598-026-42006-z
Schlüsselwörter: Genetik von Darmkrebs, PI3K AKT mTOR Signalweg, Einzelnukleotid‑Polymorphismen, Präzisionsonkologie, Chemotherapieansprechen