Clear Sky Science · de
Visualisierung malignen Fortschreitens: in situ CD109-basierter räumlicher Immunfluoreszenz-Assay zeichnet die Transformation von papillärem zu anaplastischem Schilddrüsenkarzinom innerhalb des Tumormikroumfelds nach
Warum diese Studie zum Schilddrüsenkrebs wichtig ist
Das anaplastische Schilddrüsenkarzinom zählt zu den tödlichsten menschlichen Krebserkrankungen und kann einen üblicherweise heilbaren Schilddrüsentumor in eine schnell tödlich verlaufende Krankheit verwandeln. Dennoch ist noch nicht vollständig geklärt, wie ein weit verbreitetes, langsam wachsendes papilläres Schilddrüsenkarzinom plötzlich in diese aggressive Form übergeht. Diese Studie verfolgt diese Umwandlung direkt im Tumor eines Patienten und nutzt eine neue Bildgebungstechnik, um Schritt für Schritt zu beobachten, wie Krebszellen und ihre Umgebung sich verändern. Die Arbeit liefert ein detaillierteres Bild davon, wie das lokale Tumorumfeld Zellen in einen tödlicheren Zustand treiben kann, und deutet auf neue Wege hin, diese Transformation zu verlangsamen oder zu verhindern.
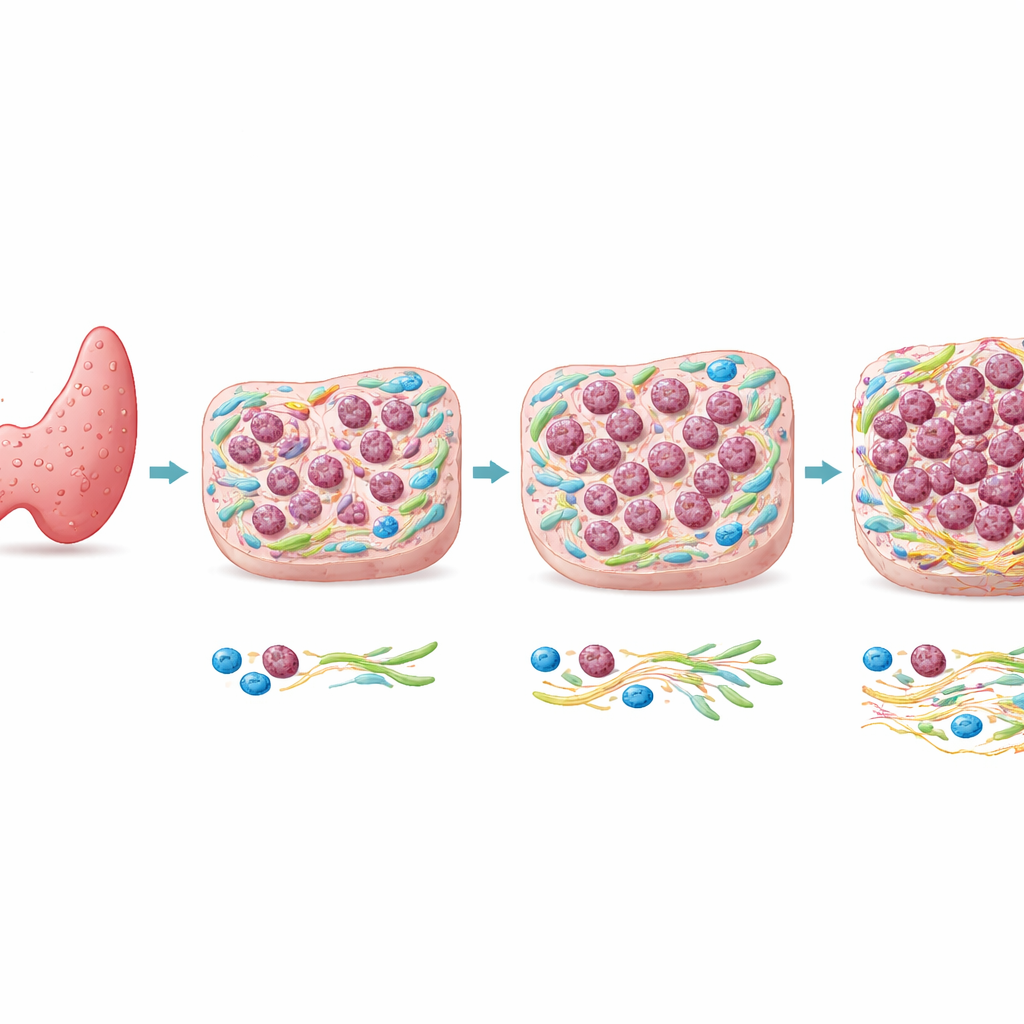
Von einem häufigen Tumor zu einem seltenen Killer
Die meisten Schilddrüsenkrebse sind papilläre Schilddrüsenkarzinome (PTC), die im Allgemeinen langsam wachsen und sehr gute Aussichten haben. Das anaplastische Schilddrüsenkarzinom (ATC) ist dagegen selten, aber häufig innerhalb weniger Monate tödlich. Genetische Studien haben gezeigt, dass ATC und benachbarte PTC im selben Patienten oft viele der gleichen DNA-Mutationen teilen, einschließlich Veränderungen in bekannten Krebsgenen. Diese Gemeinsamkeit legt nahe, dass Gene allein nicht erklären, warum nur bestimmte Bereiche eines Tumors anaplastisch werden. Die Autoren richteten ihren Fokus daher auf das, was in der Gewebeumgebung um die Zellen geschieht — das Tumormikroumfeld — um zu prüfen, ob lokale Bedingungen diese gefährliche Verschiebung fördern.
Eine neue Methode, Krebs vor Ort zu kartieren
Das Team entwickelte einen räumlichen Immunfluoreszenz-(SPI-)Assay, eine Form der Mehrfarben-Mikroskopie, die die Helligkeit bestimmter Proteine in kleinen, definierten Kacheln über einen Gewebeschnitt misst. Sie stellten die Methode auf CD109 aus, ein Oberflächenprotein, das sie als Marker für malignes Verhalten im Schilddrüsengewebe identifizierten, und CK8/18, ein Protein, das für gewöhnliche papillären Tumorzellen charakteristisch ist. Durch die Berechnung des Verhältnisses von CD109 zu CK8/18 in Hunderten kleiner Regionen erzeugten sie farbkodierte Karten, die klare PTC-Bereiche von klaren ATC-Bereichen trennten und vor allem Zwischenzonen aufzeigten, in denen beide Marker überlappten. Anstelle einer scharfen Grenze erschien der Übergang von papillärem zu anaplastischem Krebs als graduelles, fleckiges Kontinuum.
Fünf Zonen entlang eines Wandlungswegs
Um dieses Kontinuum besser zu verstehen, teilten die Forscher das Gewebe in fünf Regionen, von reinem PTC bis zu voll entwickeltem ATC. Sie untersuchten dann viele weitere Proteine, die Auskunft über Zellidentität, Wachstum, Bewegung und das stützende Gewebe geben. In diesen Regionen nahmen klassische epitheliale Merkmale wie E-Cadherin und CK8/18 stetig ab, während Marker, die mit Zellbeweglichkeit und Formänderung verknüpft sind, wie Vimentin, zunahmen. Proteine, die auf rasche Zellteilung hinweisen, stiegen in den stärker anaplastischen Zonen an. Gleichzeitig wurden die umliegenden Stützzellen — krebsassoziierte Fibroblasten — und Immunzellen, insbesondere bestimmte Makrophagen, zahlreicher und stärker aktiviert, und die von ihnen produzierten Proteine nahmen zu.
Wenn das Tumorgerüst feindlich wird
Eine auffällige Veränderung trat im Gerüst des Tumors, der extrazellulären Matrix, auf. In den anaplastischen Bereichen lagerten fibroblastähnliche Zellen mehr Kollagene vom Typ III und VI sowie ein Matrixprotein namens TGFBI ab; diese Fasern waren dicker, stärker vernetzt und in vielen Richtungen orientiert statt in glatten, parallelen Bahnen. Dieses umgestaltete Geflecht macht das Gewebe wahrscheinlich mechanisch steifer. In diesen steiferen Zonen war ein druckempfindliches Signalmolekül namens YAP sowohl in Krebs- als auch in Stützzellen stärker aktiv. Dieselben Bereiche zeigten mehr Anzeichen von DNA-Schäden und einer Form entzündlicher Zelltodprozesse sowie die Freisetzung von S100-Proteinen, die als Gefahrenzeichen wirken und die Entzündung weiter anheizen können. Die Autoren schlagen vor, dass diese Kombination aus Kompression, Zelltod und chronischer Entzündung das Überleben und die Ausbreitung bereits mutierter Krebszellen fördert, die Stress widerstehen und einen epithel–mesenchymalen-ähnlichen Übergang durchlaufen können.
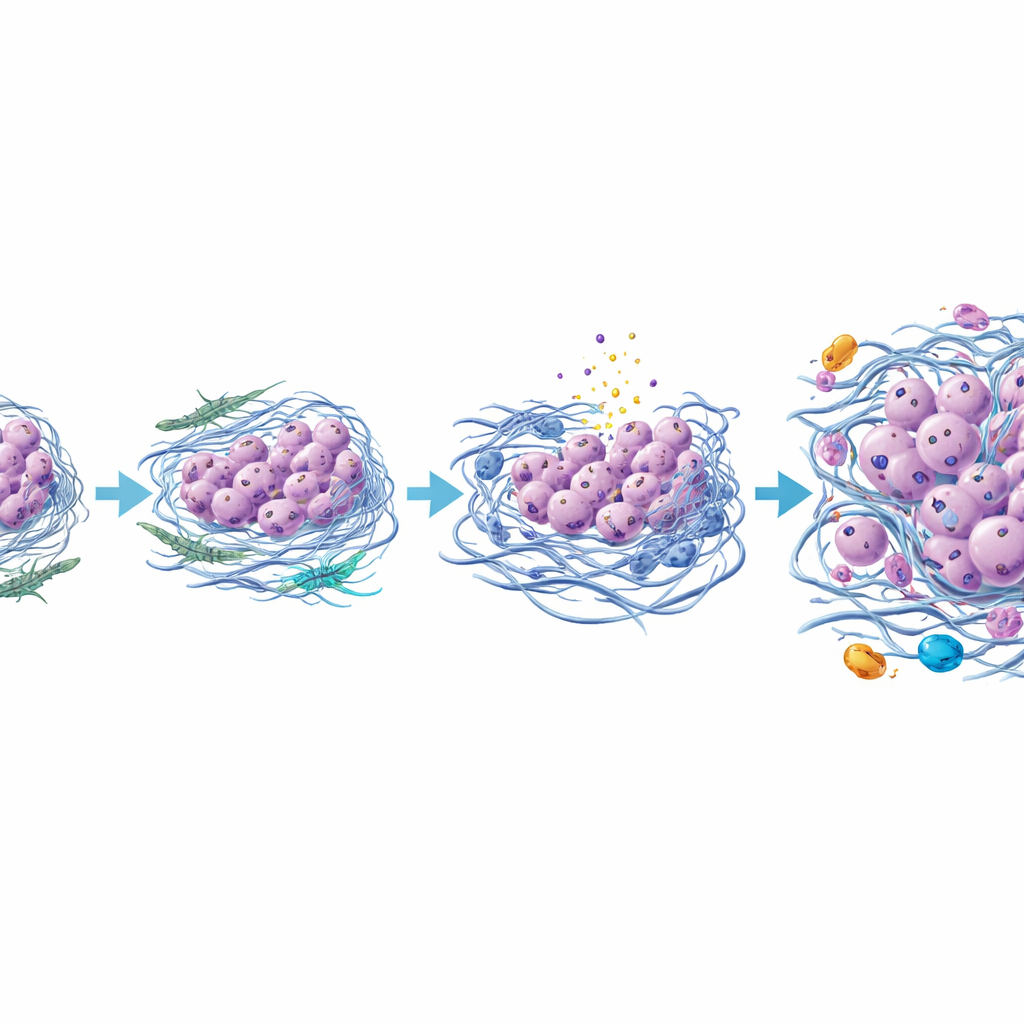
Ein neues Bild davon, wie ein Schilddrüsentumor tödlich wird
Setzt man diese Befunde zusammen, legt die Studie nahe, dass anaplastischer Schilddrüsenkrebs nicht nur durch zusätzliche Genmutationen entsteht, sondern durch ein umgestaltetes Umfeld rund um den Tumor. Wenn papilläre Tumorzellen und benachbarte Stützzellen interagieren, entwickeln sich einige Fibroblasten zu einem aggressiveren Typ, der die umgebende Matrix verdickt und versteift, verletzliche Zellen zerdrückt und entzündliche Immunzellen anlockt. Die überlebenden, widerstandsfähigeren Krebszellen verlieren allmählich ihre ursprünglichen Schilddrüsenmerkmale und nehmen eine beweglichere, invasive Identität an, bis schließlich ein anaplastischer Tumor entsteht. Auch wenn diese Arbeit auf einem gut untersuchten Einzelfall basiert und in weiteren Patienten bestätigt werden muss, führt sie ein leistungsfähiges Bildgebungswerkzeug und ein detailliertes Modell ein, wonach das Anvisieren der Stützzellen des Tumors, der Matrix oder der entzündlichen Signale helfen könnte, eine der gefürchtetsten Transformationen beim Schilddrüsenkrebs zu verhindern oder zu verzögern.
Zitation: Cohen, T., Suzuki, K., Matsuda, K. et al. Visualizing malignant progression: in situ CD109-based spatial immunofluorescence assay delineates papillary to anaplastic thyroid carcinoma transformation within the tumor microenvironment. Sci Rep 16, 8682 (2026). https://doi.org/10.1038/s41598-026-41927-z
Schlüsselwörter: anaplastisches Schilddrüsenkarzinom, papilläres Schilddrüsenkarzinom, Tumormikroumfeld, Steifigkeit der extrazellulären Matrix, räumliche Immunfluoreszenz