Clear Sky Science · de
Analyse von extrazellulären Vesikeln aus bronchialen Epithelzellen mit konventionellen, bildgebenden und nanoskaligen Durchflusszytometrie-Technologien
Warum winzige Bläschen in den Lungen wichtig sind
Unsere Lungen sind von Zellen ausgekleidet, die ständig mit dem Immunsystem kommunizieren, besonders wenn wir Staub, Schadstoffe oder Keime einatmen. Ein Großteil dieses „Gesprächs“ erfolgt über mikroskopisch kleine Bläschen, sogenannte extrazelluläre Vesikel — Paketchen aus Lipiden und Proteinen, die von Zellen freigesetzt werden. Diese Vesikel können Lungenerkrankungen verschlimmern oder dämpfen und könnten eines Tages als Frühwarnsignale für Zustände wie Asthma, chronisch obstruktive Lungenerkrankung (COPD) oder Fibrose dienen. Diese Studie untersucht, wie sich diese schwer fassbaren Partikel am besten mit verschiedenen Arten fortschrittlicher laserbasierter Instrumente messen lassen, mit dem Ziel, solche Messungen für die Forschung und mögliche künftige klinische Tests praktikabel zu machen.
Unsichtbare Botschaften von den Atemwegszellen
Extrazelluläre Vesikel (EVs) sind winzige, von einer Membran umschlossene Pakete, die von nahezu allen Zellen in Flüssigkeiten wie Blut, Urin und der dünnen Flüssigkeitsschicht der Luftwege freigesetzt werden. EVs aus menschlichen bronchialen Epithelzellen — den Zellen, die die Atemwege auskleiden — wurden bereits mit mehreren Lungenprozessen in Verbindung gebracht: Sie können beeinflussen, wie Allergien entstehen, bei der Bekämpfung von Lungeninfektionen helfen, die Struktur der Atemwege bei COPD prägen und sogar die Narbenbildung im Lungengewebe begrenzen. Da sie Fragmente von Proteinen, Lipiden und genetischem Material ihrer Ursprungzellen tragen, könnten EVs als Fingerabdrücke für Lungen-Gesundheit oder -Erkrankung dienen und möglicherweise selbst als Therapie eingesetzt werden. Die Herausforderung ist, dass sie extrem klein, stark heterogen und in geringen Mengen vorhanden sind, wodurch sie schwer sichtbar zu machen und genau zu zählen sind.
Weg vom langsamen und fragmentierten Testen
Traditionell haben Wissenschaftler mehrere getrennte Methoden zur Untersuchung von EVs verwendet. Ultrazentrifugation oder Größenausschlusschromatographie dienen zu ihrer Isolation; Nanopartikel-Tracking-Analyse misst ihre Bewegung, um Größe und Zahl abzuschätzen; und Elektronenmikroskope liefern detaillierte Bilder. Obwohl leistungsfähig, sind diese Ansätze langsam, arbeitsintensiv und nicht ideal für Routinetests oder den klinischen Einsatz. Vor allem sind sie schlecht darin, anzugeben, welche spezifischen Proteine jedes Vesikel trägt. Durchflusszytometrie — eine Technologie, die weit verbreitet zur Analyse von Blut- und Immunzellen eingesetzt wird — bietet eine straffere Alternative. Sie führt Partikel einzeln an Laser vorbei und misst deren Lichtstreuung (in Bezug auf Größe) und Fluoreszenz (durch Farbstoffe oder Antikörper). Moderne Gerätekonzepte versprechen, die Durchflusszytometrie bis hinunter zur Größenordnung der kleinsten Vesikel zu bringen, was die Möglichkeit eröffnet, Größe, Anzahl und Charakteristika von EVs in einem einzigen Durchgang zu erfassen.
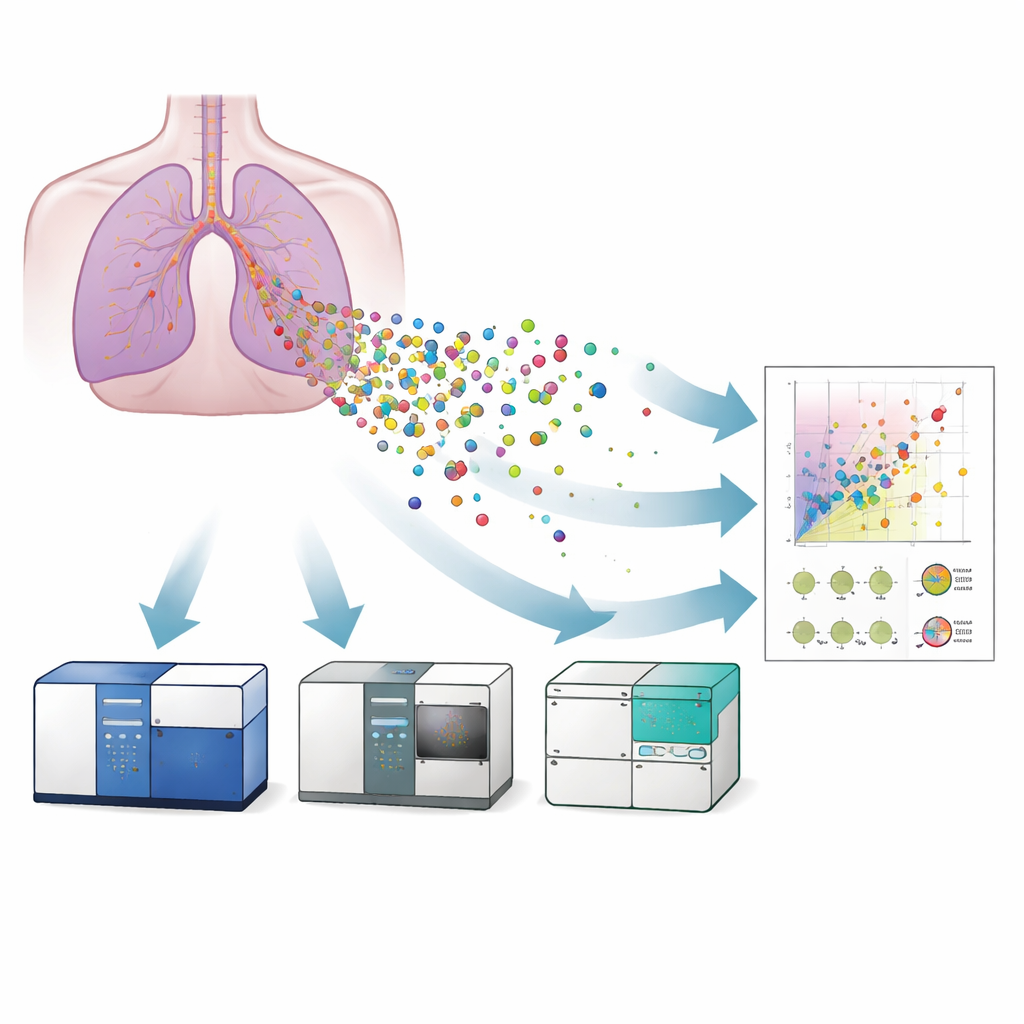
Drei Geräte, ein Ziel
Die Forschenden verglichen drei Varianten der Durchflusszytometrie zur Untersuchung von EVs, die aus einem im Labor gezüchteten Modell des menschlichen bronchialen Epithels freigesetzt wurden: einen konventionellen Durchflusszytometer, einen bildgebenden Durchflusszytometer und einen nanoskaligen Durchflusszytometer. Zunächst bestätigten sie das Vorhandensein und das typische Aussehen der Vesikel mittels Elektronenmikroskopie und Superauflösungs-Mikroskopie, die auch zeigten, dass die Vesikel Oberflächenproteine tragen, die als Tetraspanine (CD9, CD63, CD81) bekannt sind — Standardmarker zur Identifizierung von EVs. Anschließend verwendeten sie sorgfältig kalibrierte Referenzperlen und Liposom-Standards, um die Lichtsignale jedes Instruments in ungefähre Vesikelgrößen zu übersetzen. Der nanoskalige Durchflusszytometer konnte Vesikel bis etwa 40 Nanometer detektieren, das bildgebende Gerät bis etwa 55 Nanometer, während das konventionelle Gerät unter ungefähr 120 Nanometern Schwierigkeiten hatte. Das bedeutete, dass nur die empfindlicheren Systeme die kleinsten und potenziell medizinisch relevantesten Vesikel vollständig erfassen konnten.
Markierung und Zählung der Vesikel
Um sicherzustellen, dass sie intakte, biologisch aktive Vesikel und nicht nur Trümmer maßen, verwendete das Team ein Farbstoff namens Calcein-AM. Dieser Farbstoff leuchtet erst, wenn er über eine intakte Membran gelangt und von Enzymen im Vesikel verarbeitet wird. Sie passten die Farbstoffkonzentration sorgfältig an, sodass Vesikel stark markiert wurden, während das Hintergrundsignal minimiert blieb, und wählten eine Konzentration, die über Verdünnungsreihen klare, lineare Reaktionen erzeugte. Calcein wurde dann mit fluoreszierenden Antikörpern kombiniert, die an die Tetraspanine auf der Vesikeloberfläche binden, wodurch die Instrumente Vesikel mit unterschiedlichen Kombinationen dieser Marker trennen konnten. Die Gruppe bestimmte außerdem, wie empfindlich jedes Gerät gegenüber diesen fluoreszenten Markern war — wie viele Antikörpermoleküle auf einem Vesikel vorhanden sein mussten, damit es zuverlässig detektiert werden konnte. Die bildgebende Durchflusszytometrie bot im Allgemeinen niedrigere Nachweisgrenzen als der konventionelle Zytometer, wodurch sie besser für Partikel mit nur wenigen Markereiweißmolekülen geeignet ist.
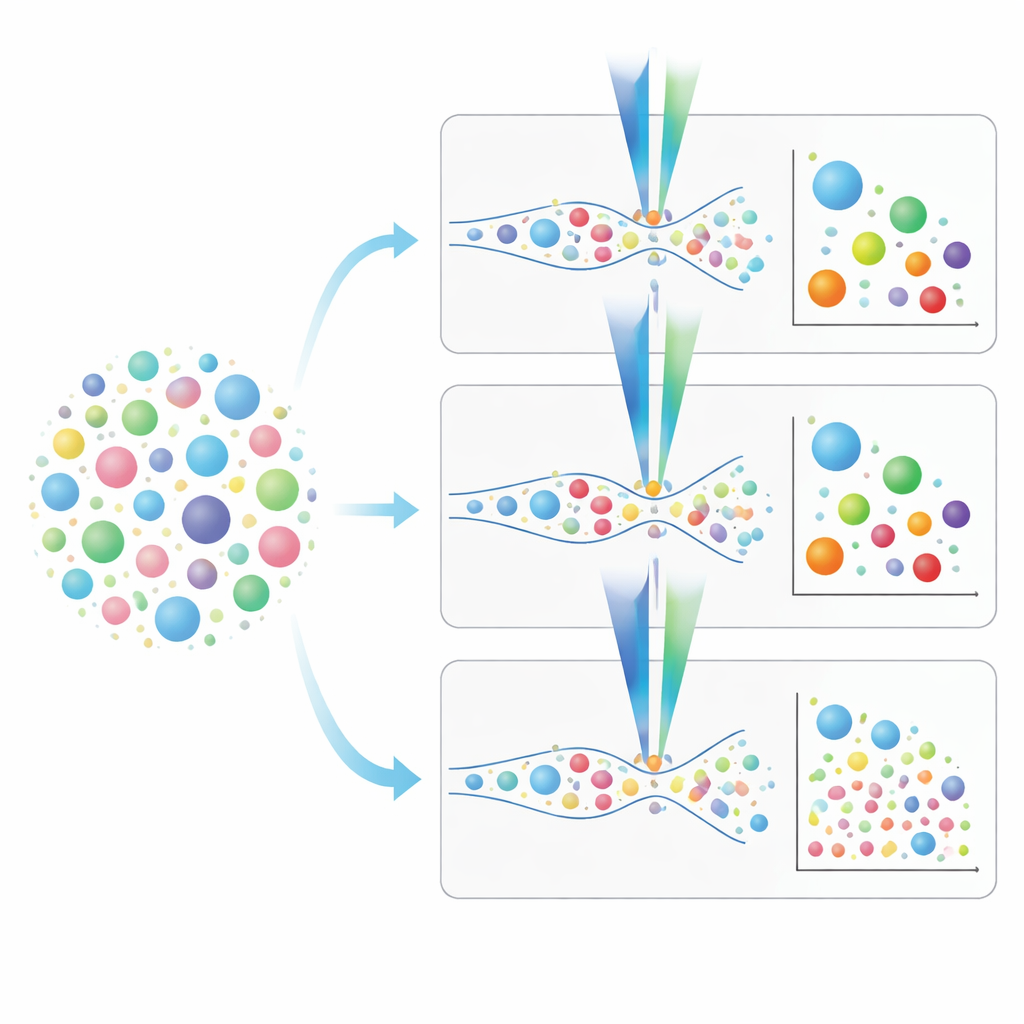
Das richtige Werkzeug für Studien zu Lungenvesikeln wählen
Aus diesem direkten Vergleich ergibt sich ein praxisorientiertes Bild. Konventionelle Durchflusszytometer sind schneller und können Proben ohne vorherige Isolation analysieren, sie übersehen jedoch viele der kleinsten Vesikel, die wichtige Krankheitssignale tragen könnten. Bildgebende und nanoskalige Durchflusszytometer, obwohl langsamer und im Fall des Nano-Geräts stärker auf vorherige Probenreinigung angewiesen, können viel kleinere Größen erfassen und eine reichhaltigere „Fingerabdruck“-Analyse der Vesikeloberflächenmarker unterstützen. Die Autoren skizzieren schrittweise Färbe- und Kalibrierungsstrategien, betonen die Bedeutung, die Nachweisgrenze jedes fluoreszenten Markers zu kennen, und zeigen, wie irreführende Signale von Farbstoffen vermieden werden können, die auch Fragmente oder Nicht-Vesikel-Partikel markieren. Einfach ausgedrückt liefern sie einen Fahrplan für Forschende, um zu entscheiden, welches Instrument und welches Protokoll am besten zu ihren Fragen zu Lungen-EVs passen, und tragen so dazu bei, die Anwendung dieser mikroskopischen Botenstoffe in Diagnose, Verständnis und letztlich Behandlung von Atemwegserkrankungen voranzubringen.
Zitation: Hopkins, G., Browne, W., Tucis, D. et al. Bronchial epithelial cell-derived extracellular vesicle analysis using conventional, imaging, and nanoscale flow cytometry technologies. Sci Rep 16, 11162 (2026). https://doi.org/10.1038/s41598-026-41848-x
Schlüsselwörter: extrazelluläre Vesikel, Lungenepithel, Durchflusszytometrie, Atemwegserkrankung, Biomarker-Analyse