Clear Sky Science · de
Kombination von tumorstammenden microRNAs mit klinischen Risikomodellen zur Vorhersage des HCC-Rezidivs nach Lebertransplantation: Eine Machbarkeitsstudie
Warum diese Forschung für Patientinnen, Patienten und Angehörige wichtig ist
Leberkrebs gehört weltweit zu den tödlichsten Krebsarten, und für manche Patientinnen und Patienten ist die einzige reale Heilungschance eine neue Leber. Selbst dann kann der Krebs jedoch im transplantierten Organ wieder auftreten, Leben verkürzen und knappe Spenderlebern belasten. Diese Studie untersucht, ob winzige Moleküle aus dem entfernten Tumor, sogenannte microRNAs, Ärzten helfen können, besser vorherzusagen, bei wem der Krebs nach der Transplantation am ehesten zurückkehrt, damit die Nachsorge gezielter an die jeweilige Person angepasst werden kann.
Ein genauerer Blick auf Leberkrebs nach Transplantation
Das hepatozelluläre Karzinom, die häufigste Form des primären Leberkrebses, entsteht oft bei Menschen mit langjähriger Leberschädigung durch Faktoren wie Alkohol, Virushepatitis oder Fettlebererkrankung. Bei kleinen Tumoren, die sich nicht sicher entfernen lassen, bietet die Lebertransplantation eine wirksame Doppelmaßnahme: Sie ersetzt die vernarbte Leber und entfernt gleichzeitig den Tumor. Da Spenderorgane jedoch begrenzt sind, stützen sich Transplantationszentren auf strenge Regeln, die hauptsächlich Größe und Anzahl der Tumoren berücksichtigen — die bekannten Milan- und UCSF-Kriterien —, um diejenigen zu identifizieren, die am meisten profitieren. Doch selbst wenn diese Kriterien eingehalten werden, tritt bei 8–20 % der Patientinnen und Patienten ein Rezidiv auf, was zeigt, dass Größenmessungen allein die Aggressivität eines Tumors nicht vollständig erfassen.
Winzige RNA-Moleküle mit großem Potenzial
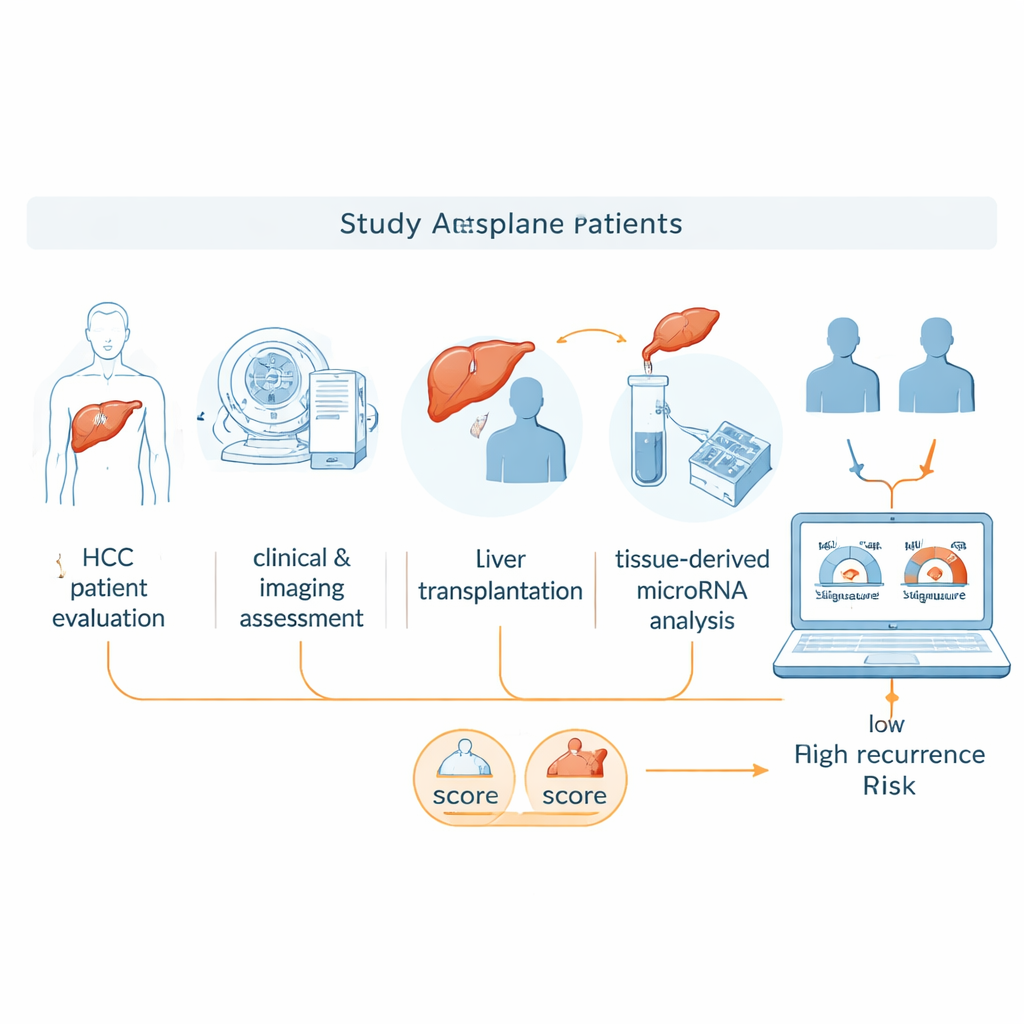
MicroRNAs sind kurze genetische Abschnitte, die selbst keine Proteine herstellen, aber steuern helfen, wie andere Gene ein- und ausgeschaltet werden. Verschiedene Tumoren weisen charakteristische microRNA-»Fingerabdrücke« auf, die Aufschluss darüber geben können, wie schnell ein Tumor wächst oder wie wahrscheinlich eine Ausbreitung ist. In dieser Machbarkeitsstudie prüften die Forschenden, ob microRNAs aus dem bei der Transplantation entfernten Lebertumor zusammen mit bestehenden klinischen Regeln die Vorhersage eines Krebsrezidivs verbessern können. Sie konzentrierten sich auf Gewebeproben, die in Paraffinblöcken konserviert worden waren — ein routinemäßiges Verfahren in Krankenhäusern —, um zu testen, ob eine solche molekulare Analyse in der Praxis umsetzbar wäre.
Wie die Studie durchgeführt wurde
Das Team wertete 20 Patientinnen und Patienten aus, die zwischen 2007 und 2021 wegen Leberkrebs eine Transplantation erhielten. Die Hälfte erlitt nach der Transplantation ein Rezidiv, die andere Hälfte blieb mindestens fünf Jahre rezidivfrei. Alle hatten vor der Operation die üblichen klinischen Untersuchungen und CT-Scans durchlaufen. Aus dem entfernten Tumor entnahmen die Forschenden RNA und untersuchten die Aktivität von etwa 3.600 microRNAs mit einem Microarray-Chip. Zunächst suchten sie nach microRNAs, deren Werte sich stark zwischen Rezidiv- und Nicht-Rezidiv-Gruppen unterschieden, und reduzierten dann die Kandidatenliste anhand statistischer Stärke und früherer Belege, die bestimmte microRNAs mit dem Verhalten von Leberkrebs in Verbindung bringen.
Ein Warnsignal aus drei microRNAs
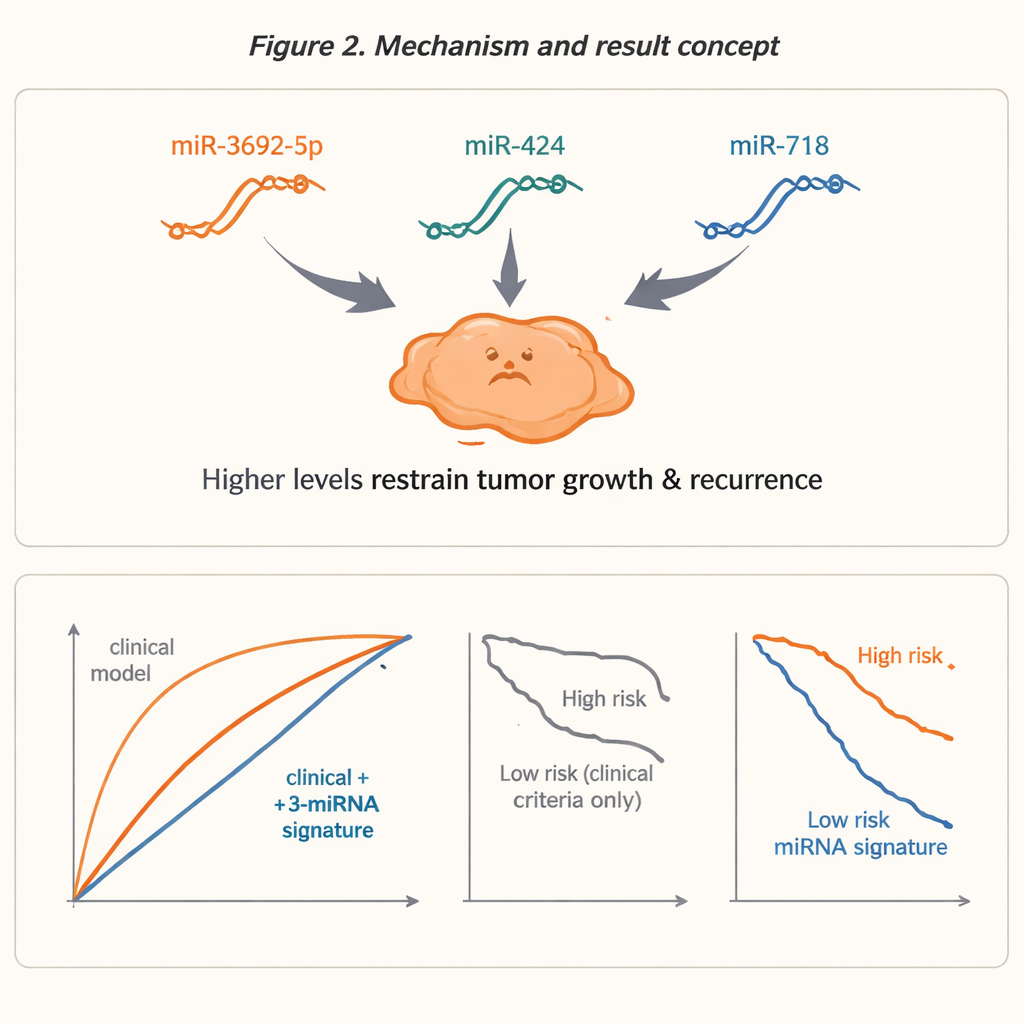
Dieser Prozess hob eine besonders aussagekräftige microRNA hervor, miR-3692-5p, die bei den Patientinnen und Patienten, deren Krebs später zurückkehrte, deutlich niedriger war. Zwei weitere microRNAs — miR-424 und miR-718 — wurden hinzugefügt, weil frühere Studien sie mit dem Verlauf von Leberkrebs verknüpft hatten und weil sie in der Rezidivgruppe ebenfalls nach unten verschoben waren. Zusammen bildeten diese drei eine »3-miRNA-Signatur«, die allein in dieser kleinen Gruppe bereits mit hoher Genauigkeit zwischen Rezidiv und Nicht-Rezidiv unterscheiden konnte. Als die Forschenden diese microRNA-Signatur auf vier gängige klinische Modelle aufsetzten — darunter die Milan- und UCSF-Kriterien sowie ein AFP-basiertes Bluttestmodell — schnitten die kombinierten Modelle deutlich besser ab als die klinischen Regeln allein bei der Vorhersage, wer rückfällig werden würde.
Wie bessere Vorhersagen in der Praxis aussehen
Zur Beurteilung der Leistung nutzte das Team gängige statistische Werkzeuge, die messen, wie gut ein Test Hoch- und Niedrigrisiko-Patientinnen und -Patienten trennt. Die klinischen Modelle allein unterschieden diese Gruppen nur mäßig. Nach Hinzufügen der drei microRNAs stieg die Vorhersagekraft stark an, mit Genauigkeitsmaßen, die sich 0,94–0,96 näherten auf einer Skala, bei der 1,0 einen perfekten Test darstellt. Die verbesserten Modelle stuften etwa die Hälfte der Patientinnen und Patienten in eine andere Risikokategorie ein, was darauf hindeutet, dass viele Menschen unter den ausschließlich auf Größe basierenden Regeln möglicherweise falsch klassifiziert werden. Wichtig ist, dass Patienten, die von den kombinierten Modellen als Hochrisiko eingestuft wurden, eine deutlich kürzere rezidivfreie Überlebenszeit hatten — etwa 17 Monate gegenüber 38,5 Monaten in einem Beispiel —, was zeigt, dass diese molekularen Signale sinnvoll mit realen Ergebnissen korrelieren.
Was das für die zukünftige Versorgung bedeutet
Für Nicht-Fachleute lautet die Quintessenz, dass die Untersuchung der inneren »Steuersignale« eines Tumors, hier erfasst durch drei spezifische microRNAs, mehr über seine wahre Natur verraten kann als Größe oder Anzahl allein. Da es sich um eine kleine, explorative Studie handelt, sind Bestätigungen in größeren, multizentrischen Kohorten und in leichter zugänglichen Proben wie Blut nötig. Die Arbeit zeigt jedoch, dass eine solche Testung technisch auf Routinegewebe machbar ist. Bei Validierung könnte dieser Ansatz Transplantationsteams helfen, Nachsorgescans und Therapien gezielter auszurichten, indem die intensivste Überwachung und präventive Maßnahmen denen vorbehalten werden, deren Tumoren ein molekulares Warnsignal für ein wahrscheinliches Rezidiv zeigen — und zugleich niedrigere Risiken vor unnötigen Untersuchungen bewahrt werden.
Zitation: Lederer, T., Lehr, K., Bobe, S. et al. Combining tissue-derived microRNAs with clinical risk models for prediction of HCC recurrence after liver transplantation: A proof-of-concept study. Sci Rep 16, 7742 (2026). https://doi.org/10.1038/s41598-026-41688-9
Schlüsselwörter: Leberkrebs, Lebertransplantation, microRNA-Biomarker, Krebsrezidivrisiko, Präzisionsonkologie