Clear Sky Science · de
DUSP29 reguliert nicht die Interaktionen zwischen Melanom und Myoblasten in einem Skelettmuskel-Kokultur‑Modell
Warum die Resistenz der Muskeln gegen Krebsausbreitung wichtig ist
Wenn sich Krebs im Körper ausbreitet, siedelt er sich oft an Orten wie Lunge, Leber oder Knochen an. Merkwürdigerweise sind unsere Skelettmuskeln — die zusammen etwa die Hälfte unseres Körpergewichts ausmachen — selten Schauplatz solcher gefährlicher Ablagerungen. Dieses Rätsel beschäftigt Mediziner und Wissenschaftler seit mehr als einem Jahrhundert. Die hier zusammengefasste Studie stellt eine gezielte Frage innerhalb dieses größeren Puzzles: Schränken Muskelzellen selbst sowie ein in Muskeln besonders reichlich vorhandenes Protein namens DUSP29 Krebszellen direkt ein, oder beruht der Schutz der Muskeln ganz auf etwas anderem?
Ein seltener Landeplatz für umherwandernde Krebszellen
Ärzte beobachten viel weniger Metastasen im Skelettmuskel als in vielen anderen Organen, selbst bei Menschen mit weit verbreiteter Krebserkrankung. Eine Idee ist, dass Muskelzellen für eindringende Tumorzellen eine unwirtliche Nachbarschaft schaffen, möglicherweise durch chemische Signale oder indem sie Krebszellen zu Verhaltensänderungen zwingen. Frühere Arbeiten an Mäusen deuteten darauf hin, dass Hautkrebszellen (Melanom), die neben unreifen Muskelzellen wachsen, etwas von ihrem Pigment verlieren und sogar beginnen, Muskelähnlichkeit anzunehmen. Aufbauend darauf richteten die Autoren ihr Augenmerk auf ein spezifisches Protein, DUSP29, das in Muskeln deutlich höher exprimiert wird als anderswo und zu einer Enzymfamilie gehört, die Wachstums‑ und Überlebenswege steuert, die Krebs häufig kapert.
Muskel‑Tumor‑Begegnungen im Reagenzglas testen
Um diese Ideen zu untersuchen, entwickelten die Forschenden ein kontrolliertes Labor‑Modell mit zwei gut untersuchten Maus‑Zelllinien: Melanomzellen (B16F10) und Muskelvorläuferzellen, sog. Myoblasten (C2C12). Sie mischten diese beiden Zelltypen in gemeinsamen Kulturschalen in unterschiedlichen Verhältnissen, von gleichen Zellzahlen bis hin zu Situationen, in denen Myoblasten Tumorzellen deutlich überwogen. In einigen Experimenten standen die Zellen in direktem Kontakt; in anderen wurden Melanomzellen nur in das flüssige Nährmedium überführt, das aus Myoblastenkulturen stammte, um etwaige lösliche Faktoren der Muskelzellen zu erfassen. Über mehrere Tage maßen die Forscher, wie viele Zellen lebten und sich teilten, mittels eines standardisierten farbumschlagenden Tests, und sie überprüften Anzeichen für programmierter Zellsterblichkeit mittels Durchflusszytometrie, einer Technik, die lebende, sterbende und tote Zellen unterscheiden kann.
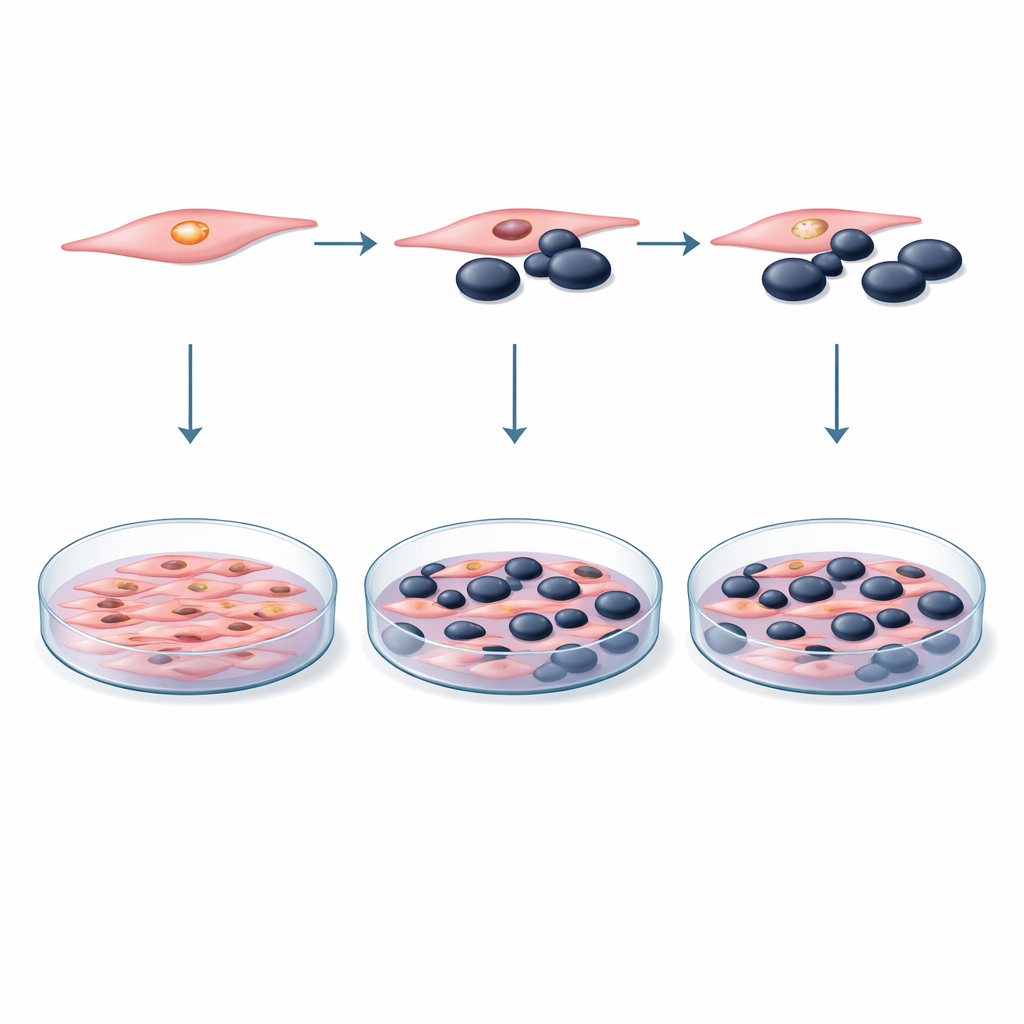
DUSP29 genauer unter der Lupe
Der zweite Teil der Studie konzentrierte sich auf DUSP29 selbst. Zunächst bestätigten die Wissenschaftler, dass Myoblasten die genetische Botschaft dieses Proteins in nennenswerten Mengen produzieren. Anschließend nutzten sie small interfering RNA (siRNA) — kurze genetische Fragmente, die wie gezielte „Ausschaltknöpfe“ wirken — um die DUSP29‑Spiegel in den Muskelzellen stark zu reduzieren. Sorgfältige Kontrollen zeigten, dass die Transfektionschemikalien und Kontroll‑siRNAs die Zellen für sich genommen nicht schädigten. Mit heruntergeregeltem DUSP29 wurden die modifizierten Myoblasten erneut zusammen mit Melanomzellen kultiviert oder ihr Nährmedium wurde auf Melanomkulturen aufgebracht. Die gleichen Tests zur Zellüberlebensrate und zum Zelltod wurden zu mehreren Zeitpunkten wiederholt, um zu prüfen, ob das Ausschalten dieses muskelreichen Proteins das Gleichgewicht zugunsten oder zulasten der Tumorzellen verschiebt.
Wenn Nichtstun das wichtige Ergebnis ist
In all diesen Experimenten war das Ergebnis durch das Fehlen dramatischer Effekte auffällig. Ob Melanomzellen allein oder neben Myoblasten kultiviert wurden, mit oder ohne direkten Kontakt — ihre Überlebensrate blieb im Rahmen normaler experimenteller Schwankungen im Wesentlichen unverändert. Die Ko‑Kultur löste weder zusätzlichen Zelltod bei Melanomzellen aus, noch förderte sie deren Wachstum. Auch das Herunterregulieren von DUSP29 in den Myoblasten veränderte nicht die Lebensfähigkeit der Melanomzellen, obwohl die Genaktivität in den Muskelzellen deutlich reduziert worden war. Anders gesagt: Unter diesen kurzzeitigen, vereinfachten Bedingungen lenkten weder myoblastische Nachbarn noch das Vorhandensein bzw. Fehlen von DUSP29 die Melanomzellen messbar in Richtung Überleben oder Vernichtung.
Was das für das Muskel‑Krebs‑Rätsel bedeutet
Die Ergebnisse deuten darauf hin, dass der relative Schutz des Skelettmuskels vor Metastasen wahrscheinlich nicht aus einer einfachen direkten Wechselwirkung zwischen Melanomzellen und benachbarten Myoblasten oder aus DUSP29 allein in dieser frühen Interaktion resultiert. Vielmehr entsteht die Resistenz der Muskeln vermutlich durch eine komplexere Mischung von Faktoren — ihre dichte Struktur, die mechanischen Kräfte der Kontraktion, einzigartige Stoffwechseleigenschaften und eine Reihe weiterer Signalmoleküle, die in diesem dish‑basierten System nicht abgebildet werden. Indem diese Arbeit klar zeigt, wo ein plausibler Mechanismus nicht wirkt, hilft sie, die Suche danach einzugrenzen, wie Muskeln die meisten metastatischen Krebszellen fernhalten, und weist zukünftige Studien auf realistischere Gewebemodelle, unterschiedliche Tumortypen und die breitere Umgebung hin, in der Muskel‑ und Krebszellen aufeinandertreffen.
Zitation: Ön, S., İlhan, H.A., Günenç, D. et al. DUSP29 does not regulate melanoma–myoblast interactions in a skeletal muscle co-culture model. Sci Rep 16, 8372 (2026). https://doi.org/10.1038/s41598-026-41300-0
Schlüsselwörter: Skelettmuskel‑Metastase, Melanom, Tumor‑Muskel‑Interaktionen, DUSP29, Tumormikroumgebung