Clear Sky Science · de
Bewertung der Langlese-Metagenomik für die Diagnostik von Blutstrominfektionen: eine Pilotstudie aus einem tertiären Krankenhaus in Thailand
Warum schnellere Tests bei Blutinfektionen wichtig sind
Wenn Bakterien in den Blutkreislauf gelangen, zählt jede Stunde. Ärztinnen und Ärzte müssen rasch das passende Antibiotikum wählen, doch die heute üblichen Labortests können mehrere Tage dauern, bis der Erreger identifiziert und seine Wirkstoffresistenzen bekannt sind. Diese Studie aus einem großen Krankenhaus in Thailand untersucht einen neuen Ansatz, um das zu beschleunigen: die gleichzeitige Auslese des genetischen Materials aller Mikroben in einer Blutprobe mit einem tragbaren DNA-Sequenzer. Ziel ist es, statt mehrtägigen Wartens innerhalb einer einzigen Schicht ein detailliertes Bild der Infektion zu liefern.
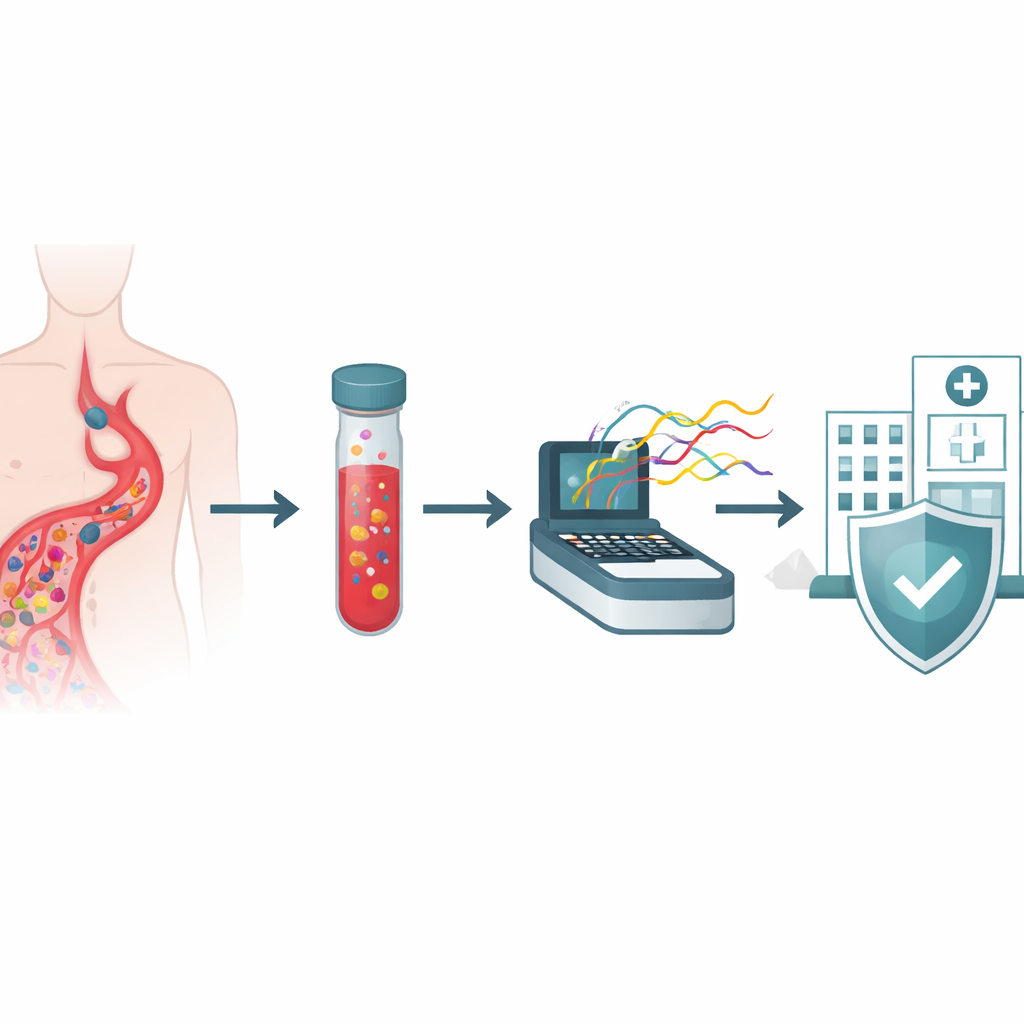
Ein neuer Weg, Keime im Blut zu lesen
Die Forschenden konzentrierten sich auf Patientinnen und Patienten, bei denen bereits in den standardmäßigen Blutkulturflaschen bakterielles Wachstum nachgewiesen worden war, wie es weltweit in Krankenhäusern üblich ist. Anstatt jedes Bakterium auf getrennten Agarplatten anzuziehen und eine Reihe chemischer Tests durchzuführen, entnahmen sie Flüssigkeit direkt aus 40 positiven Kulturflaschen und isolierten die gesamte mikrobielle DNA. Diese DNA wurde anschließend auf einem Oxford-Nanopore-Sequenzer analysiert, einem Gerät, das lange DNA-Stränge durch winzige Poren zieht und ihre Sequenz in Echtzeit liest. Da die Methode nicht vom separaten Anzüchten einzelner Organismen abhängt, kann sie prinzipiell viele Arten, ihre Resistenzmerkmale und ihre krankheitsfördernden Eigenschaften in einem einzigen, schlanken Arbeitsablauf erfassen.
Was man bei Blutstrominfektionen in Thailand fand
Die konventionelle Untersuchung derselben 40 Proben ergab 45 bakterielle Isolate, was widerspiegelt, dass einige Patientinnen und Patienten mit mehr als einer Spezies infiziert waren. Das im Klinikum übliche Arbeitssystem VITEK zeigte, dass zwei bekannte Darmbakterien, Escherichia coli und Klebsiella pneumoniae, fast 40 % dieser Infektionen verursachten und viele dieser Stämme gegen mehrere Wirkstoffe resistent waren. Der Nanopore-Ansatz stimmte weitgehend mit diesem Bild überein: Er identifizierte 43 verschiedene bakterielle Genome und bestätigte die Dominanz von Angehörigen der Enterobacterales. Außerdem entdeckte er einige seltene oder falsch klassifizierte Spezies, etwa das Umweltbakterium Ralstonia mannitolilytica und das Magen-Darm-Bakterium Campylobacter jejuni, die Routineverfahren übersehen hatten oder nur unscharf erfasst wurden. In einigen Mischinfektionen hatte die Sequenzierung jedoch Schwierigkeiten, eng verwandte Mikroben vollständig zu trennen, wenn eine Art deutlich seltener vertreten war als die andere.
Blick auf Resistenz- und Tarnungsmechanismen
Weil die neue Methode lange DNA-Stücke liest, kann sie mehr als nur die Bakterien benennen: Sie zeigt die genetische Maschinerie, die ihnen hilft, Antibiotika zu widerstehen und Krankheit zu verursachen. Das Team durchsuchte die Genome nach bekannten Resistenzgenen und nach „Virulenz“-Genen, die Keimen helfen, an Geweben zu haften, schützende Biofilme zu bilden, Eisen zu stehlen oder Toxine zu produzieren. E. coli und K. pneumoniae trugen viele solcher Gene, darunter solche, die wichtige Antibiotikaklassen wie Beta-Laktame und Aminoglykoside unwirksam machen. Die Sequenzierung hob auch mächtige Resistenzpakete in klinisch belasteten Arten wie Acinetobacter baumannii und Pseudomonas aeruginosa hervor, deren Genome reich an Wirkstoffpumpen und anderen Abwehrmechanismen waren. Gleichzeitig verfügten einige seltenere Blutkeime über vergleichsweise überschaubare Arsenale, was auf ein geringeres, aber dennoch relevantes Risiko hindeutet. 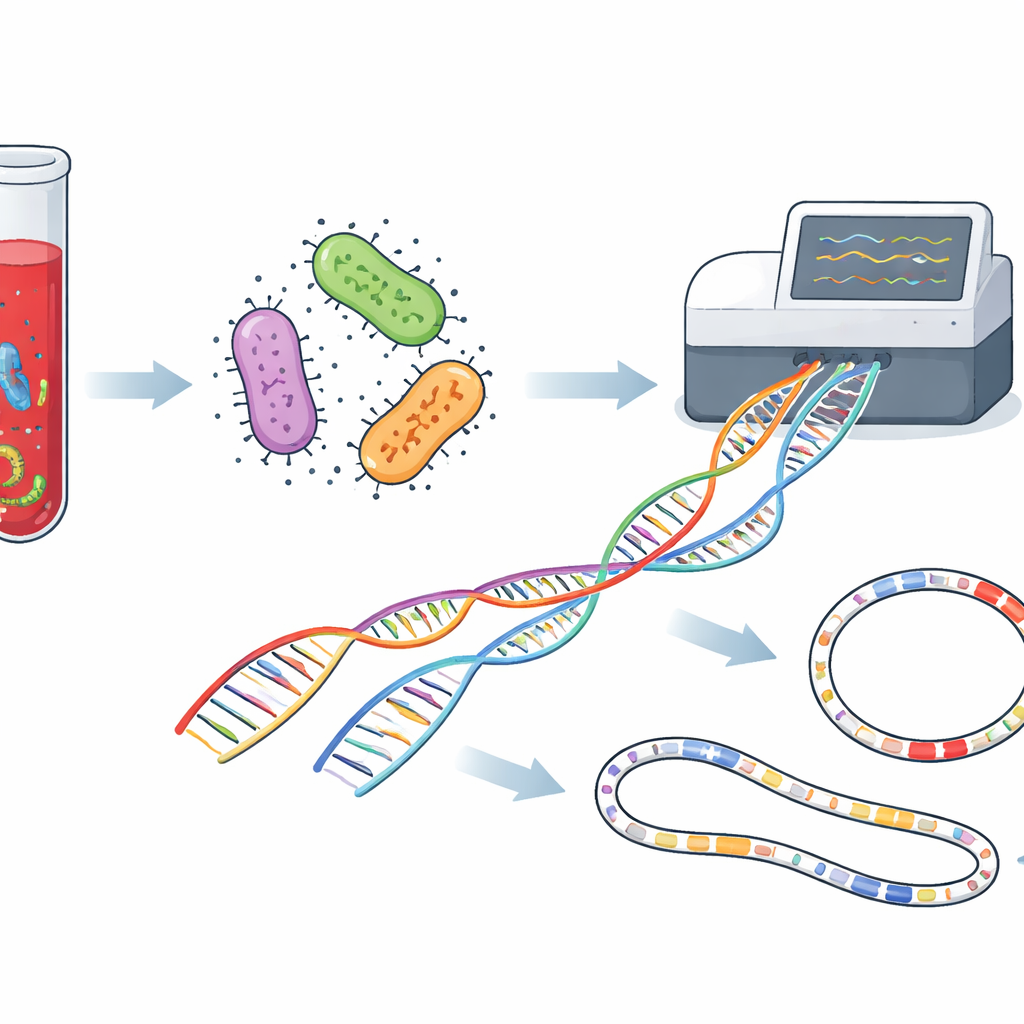
Resistenzen auf mobilen DNA-Elementen verfolgen
Eine weitere Stärke der Langlese-Sequenzierung ist die Fähigkeit, ganze bakterielle Chromosomen zusammen mit zirkulären DNA-Molekülen namens Plasmiden zusammenzusetzen, die zwischen Bakterien springen und Resistenzgene verbreiten können. In dieser Studie katalogisierten die Forschenden Dutzende Plasmidtypen. Einige waren stark mit bestimmten Spezies verknüpft, andere wurden über mehrere Bakterienarten hinweg geteilt, was auf einen fortlaufenden Genaustausch in der Krankenhausumgebung hindeutet. Viele trugen bekannte Treiber von Therapieversagen, wie erweitere Spektrum Beta-Laktamasen und Carbapenemasen — Enzyme, die einige der wichtigsten Antibiotika wirkungslos machen. Das Kartieren dieser mobilen Elemente hilft den Infektionskontrollteams zu verstehen, wie gefährliche Eigenschaften sich im Zeitverlauf durch ein Krankenhaus bewegen.
Schnellere Antworten für Ärzte und Kliniken
Die zeitliche Dimension ist der Bereich, in dem der neue Ansatz den deutlichsten Vorteil zeigt. Standardabläufe benötigen oft fünf bis sieben Tage, von dem Moment an, in dem eine Blutkultur positiv wird, bis vollständige Identifikations- und Empfindlichkeitsbefunde vorliegen. Im Gegensatz dazu lieferte die Nanopore-Konfiguration in dieser Pilotstudie frühe Artenidentifikationen innerhalb von zwei bis vier Stunden nach Beginn des Laufs und markierte wichtige Resistenzgene innerhalb von sechs bis acht Stunden. Längere Sequenzläufe verbesserten zwar die Vollständigkeit der Genome, änderten aber nicht die wesentlichen klinischen Schlussfolgerungen. Obwohl es sich um eine kleine, frühe Studie handelte, die noch keine Verknüpfung der Ergebnisse mit Patientenergebnissen oder Kostenmessungen vornahm, deutet sie darauf hin, dass die Integration der Langlese-Metagenomik in Krankenhauslabore schneller und reichhaltiger Informationen liefern könnte, um die Behandlung zu steuern, die Antibiotikastewardship zu unterstützen und die regionale Überwachung resistenter Infektionen zu stärken.
Was das für die Patientenversorgung bedeutet
Für die Allgemeinheit lässt sich festhalten: Ärztinnen und Ärzte könnten bald noch am selben Tag, an dem eine Kultur positiv wird, eine genetische „Momentaufnahme“ einer Blutinfektion zur Verfügung haben, statt nahezu eine Woche zu warten. Diese Momentaufnahme nennt nicht nur den Erreger, sondern zeigt auch viele seiner Schwachstellen und seine Fähigkeit, Resistenz an andere weiterzugeben. Während weitere Studien mit größeren Patientengruppen, strengeren Kontaminationskontrollen und Kostenanalysen nötig sind, zeigt diese thailändische Pilotstudie, dass taschengroße DNA-Sequenzer uns näher an eine schnelle, genominformierte Versorgung lebensbedrohlicher Blutinfektionen bringen können.
Zitation: Yaikhan, T., Wongsurawat, T., Jenjaroenpan, P. et al. Evaluating long-read metagenomics for bloodstream infection diagnostics: a pilot study from a Thai Tertiary Hospital. Sci Rep 16, 9330 (2026). https://doi.org/10.1038/s41598-026-41247-2
Schlüsselwörter: Blutstrominfektion, antimikrobielle Resistenz, metagenomische Sequenzierung, Nanopore-Technologie, klinische Mikrobiologie