Clear Sky Science · de
Auftreten eines neu reassortierten hochpathogenen aviären Influenza-A(H5N2)-Virus, das mit schwerer Pneumonie bei einer jungen Erwachsenen in Verbindung steht
Warum dieser neue Vogelgrippe-Fall wichtig ist
Meistens betrifft die Vogelgrippe Landwirtinnen und Wildtierfachleute, nicht die allgemeine Bevölkerung. Dieser Artikel beschreibt die erstmals dokumentierte menschliche Infektion mit einer neuen Art von Vogelgrippevirus namens H5N2, das bei Vögeln schwere Erkrankungen verursachen kann und in diesem Fall eine schwere Pneumonie bei einer jungen Frau in Mexiko auslöste. Zu verstehen, wie dieses Virus entstanden ist, wie es die Patientin betroffen hat und wie es sich ausbreiten könnte, hilft Ärztinnen, Ärzten und Gesundheitsbehörden, künftige Gefahren zu erkennen, bevor sie zu größeren Ausbrüchen werden.
Eine seltene und schwere Erkrankung bei einer Person
Die Geschichte beginnt Ende 2025, als eine junge Erwachsene nach mehr als einer Woche mit Fieber, Halsschmerzen, Husten, Atemnot und blutigem Auswurf in ein Atemwegskrankenhaus in Mexiko‑Stadt eingeliefert wurde. Sie war adipös, hatte aber keine schweren chronischen Erkrankungen und keinen bestätigten engen Kontakt zu Geflügel, Tauben oder anderen Tieren. Bei Aufnahme waren ihre Sauerstoffwerte gefährlich niedrig, und Röntgen‑/CT‑Bilder zeigten verschattete, fleckige Bereiche und Hinweise auf Blutungen in beiden Lungen, was mit einer schweren Pneumonie übereinstimmte, die die winzigen für den Gasaustausch verantwortlichen Lungenbläschen schädigte.
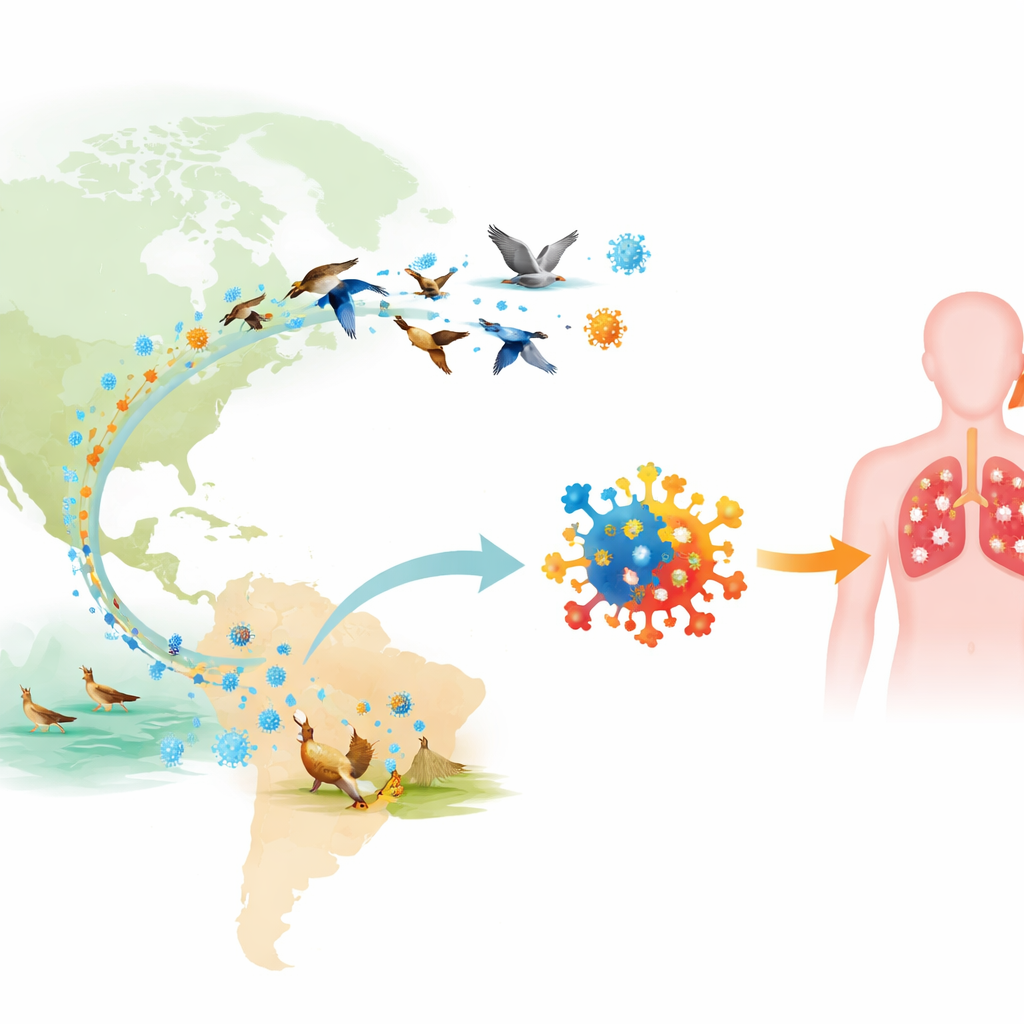
Die Spur eines ungewöhnlichen Virus verfolgen
Erste Labortests ergaben, dass die Patientin mit Influenza A infiziert war, der großen Familie, zu der sowohl saisonale als auch aviäre Grippe gehören. Standardtests konnten den Erreger jedoch keinem bekannten saisonalen Subtyp zuordnen, was den Verdacht auf eine ungewöhnliche Stämmen erhob. Spezialisiertere Untersuchungen von Material aus tiefen Atemwegen bestätigten, dass es zur H5‑Familie der Vogelviren gehörte. Die Patientin kam unter Infektionsschutzmaßnahmen, erhielt das antivirale Medikament Oseltamivir und zusätzlich Sauerstoff. In den folgenden Tagen besserte sich ihr Zustand stetig, und sie wurde schließlich ohne Komplikationen entlassen, während die Gesundheitsbehörden mit der Untersuchung der Infektionsquelle begannen.
Wie sich verschiedene Vogelgrippen zu etwas Neuem vermischten
Um genau zu bestimmen, womit sie es zu tun hatten, sequenzierten Forschende das vollständige genetische Material des Viruses aus der Patientin. Influenzaviren tragen ihre Gene auf acht getrennten Segmenten, die ausgetauscht werden können, wenn zwei verschiedene Viren dasselbe Tier infizieren. Die Analyse zeigte, dass das Virus der Patientin ein genetisches Flickwerk war: Einige Segmente stimmten mit hochpathogenen H5N1‑Viren überein, die weitverbreitet bei Wildvögeln kursieren und in Nordamerika große Geflügelausbrüche verursacht haben, während andere Segmente mit einem seit Langem in mexikanischem Geflügel zirkulierenden, weniger aggressiven H5N2‑Virus übereinstimmten. Dieser Mischvorgang, Reassortment genannt, hatte eine neue Variante von H5N2 hervorgebracht, die Merkmale beider Elterntypen vereint.
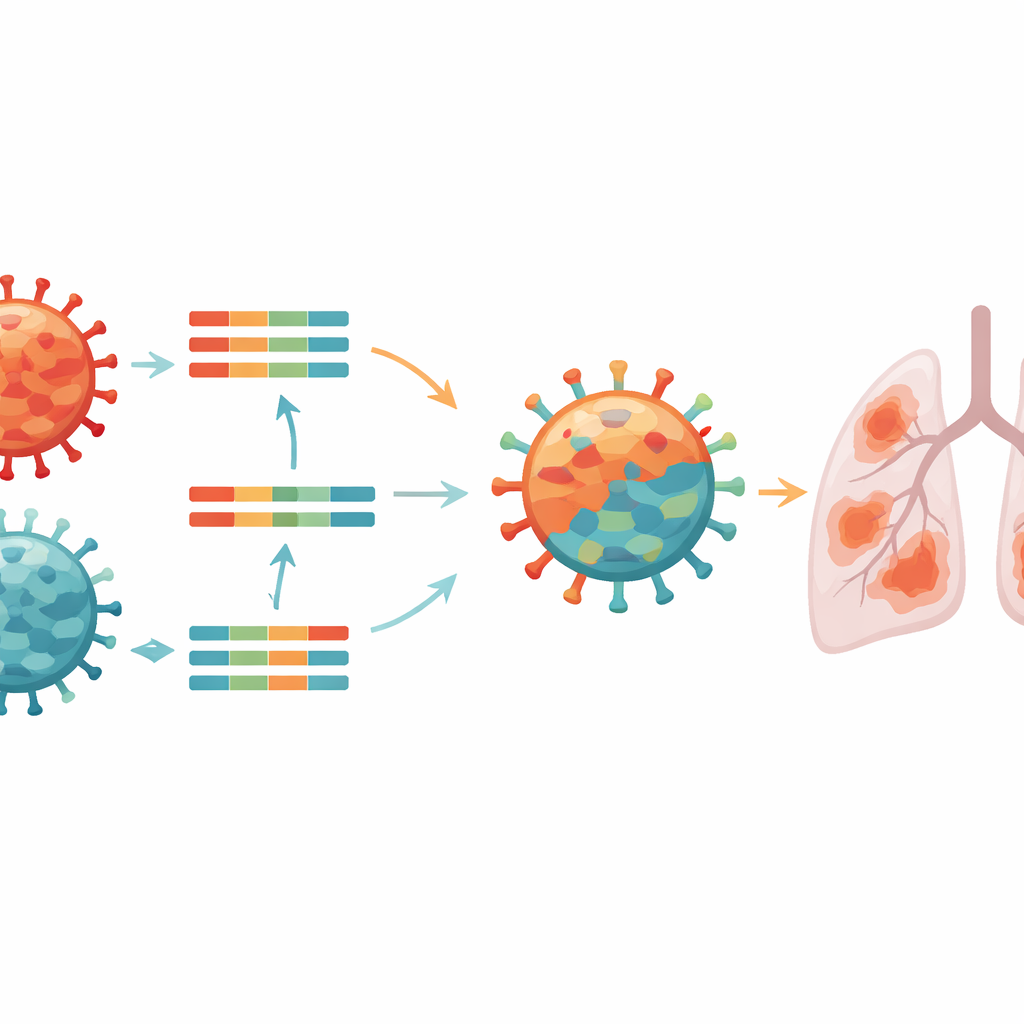
Genetische Hinweise auf Risiko für Menschen und Tiere
Durch den Vergleich der Gene dieses Virus mit Tausenden anderen Vogelgrippeproben aus Nordamerika und Mexiko konnten die Forschenden es in detaillierten Stammbaumkarten einordnen und einem zuvor nicht gesehenen genetischen Muster zuweisen, das sie vorläufig B3.14 nannten. Sie suchten auch nach spezifischen Veränderungen, die das Virus beim Infizieren von Säugetieren oder beim Resistenzverhalten gegen Medikamente begünstigen könnten. Das Virus trug weiterhin ein molekulares Muster, das typisch für hochpathogene Vogelstämme ist, und wies keine bekannten Änderungen auf, die gängige antivirale Medikamente unwirksam machen. Es enthielt jedoch mehrere Modifikationen, die in anderen Studien mit besserer Vermehrung in Säugetierzellen und mit Veränderungen in der Bindung an Rezeptoren der Atemwege in Verbindung gebracht wurden, was Besorgnis erregt, dass es etwas besser geeignet sein könnte, Menschen oder andere Säugetiere zu infizieren als frühere Verwandte.
Was dieser einzelne Fall über künftige Gefahren aussagt
Trotz der Schwere der Erkrankung der Frau ergaben Folgeuntersuchungen bei mehr als 40 engen menschlichen Kontaktpersonen keine weiteren Infektionen, und es gab keine Hinweise auf eine Übertragung von Mensch zu Mensch. Proben eines Huhns, zweier Tauben und eines Hundes aus dem Haushalt der Patientin enthielten verwandte H5‑Viren, was unterstreicht, dass die wahrscheinliche Quelle die fortlaufende Zirkulation gemischter Vogelgrippe‑Stämme in lokalen Tieren war und nicht die Ausbreitung zwischen Menschen. Die Autorinnen und Autoren schließen, dass dies die erste dokumentierte menschliche Infektion mit einem hochpathogenen H5N2‑Virus dieser neuen genetischen Zusammensetzung ist und ein Warnsignal dafür, wie schnell Vogel‑ und Tierviren ihre Gene neu mischen und die Speziesgrenze überschreiten können. Sie plädieren dafür, die genetische Überwachung in Wildvögeln, Geflügel und Säugetieren fortzusetzen – verbunden mit rascher Diagnostik und Behandlung beim Menschen –, um solche gefährlichen Neuzugänge frühzeitig zu erfassen und Impfstoff‑ sowie antivirale Strategien zu steuern, bevor sie sich weiter ausbreiten können.
Zitation: Vázquez-Pérez, J.A., Becerril-Vargas, E., Ramírez‐González, J.E. et al. Emergence of a novel reassorted high pathogenicity avian influenza A(H5N2) virus associated with severe pneumonia in a young adult. Sci Rep 16, 8841 (2026). https://doi.org/10.1038/s41598-026-41122-0
Schlüsselwörter: Vogelgrippe, H5N2, Reassortant‑Virus, Pneumonie, Zoonotische Infektion