Clear Sky Science · de
In-situ-Wachstum heterogener Au-Partikel auf MoS2-Nanoschichten für die SERS-Detektion von brustkrebsassoziierten miR-210-3p und miR-9-3p
Kleine Krebs‑Signale in deutliche Warnhinweise verwandeln
Ärztinnen und Ärzte wissen seit langem, dass Tumorzellen winzige Fragmente genetischen Materials in den Blutkreislauf abgeben, doch diese leisen Hinweise auf Krankheit zuverlässig nachzuweisen, war schwierig. Diese Studie stellt einen neuen nanoskaligen Sensor vor, der eine spezielle Kombination aus Gold und dem zweidimensionalen Material Molybdändisulfid (MoS2) nutzt, um diese schwachen Signale zu verstärken. Ziel ist es, das Auffinden brustkrebsbezogener MicroRNAs — kurze RNA-Stücke, die mit dem Wachstum und der Ausbreitung von Tumoren verknüpft sind — zu erleichtern, und das mit einer schonenden, lichtbasierten Methode, die eines Tages frühere und präzisere Diagnosen unterstützen könnte.
Warum diese winzigen Moleküle wichtig sind
MicroRNAs sind extrem kurze Abschnitte des genetischen Codes, die die Zellfunktionen steuern helfen. Bei Krebs kommen manche MicroRNAs ungewöhnlich häufig oder selten vor, wodurch sie zu starken Biomarkern für Diagnose und Prognose werden. Die Schwierigkeit besteht darin, dass sie in sehr niedrigen Konzentrationen vorliegen und oft in komplexen biologischen Flüssigkeiten wie Blut oder Zelllysaten verteilt sind. Konventionelle Methoden wie PCR und Sequenzierung können sie zwar nachweisen, erfordern jedoch spezialisierte Labore, geschultes Personal und zeitaufwändige Arbeitsabläufe. Die Forscherinnen und Forscher wollten eine direkt arbeitende Messplattform entwickeln, die prinzipiell einfacher zu betreiben ist, zugleich aber sehr hohe Empfindlichkeit und die Fähigkeit bietet, mehrere MicroRNA-Ziele gleichzeitig zu unterscheiden.
Aufbau eines lichtverstärkenden Nanosheets
Um dies zu erreichen, konstruierten das Team ein Hybridmaterial aus dünnen MoS2-Nanoschichten, die mit Goldnanopartikeln dekoriert sind. MoS2 ist ein blattförmiges Material von nur wenigen Atomen Dicke, das eine große Oberfläche zum Anheften von Molekülen bietet und eine starke Wechselwirkung mit Metallen zeigt. Anstatt vorgefertigte Goldpartikel zu verwenden, wuchsen sie das Gold direkt auf der MoS2-Oberfläche in Lösung heran. Dieses in-situ-Wachstum erzeugte eine bewusst heterogene Landschaft aus Goldpartikeln — überwiegend Kugeln, aber auch Dreiecke und unregelmäßige Formen —, verteilt über die Flächen und Kanten der MoS2-Blätter. Mikroskopie und Spektroskopie bestätigten, dass Gold und MoS2 einen stabilen Verbund bildeten, wobei Gold an defektreichen Stellen der Blätter fest verankert war. Diese unregelmäßige, „raue“ Architektur ist entscheidend, weil sie viele winzige Lücken und scharfe Strukturen schafft, in denen Licht stark konzentriert werden kann.
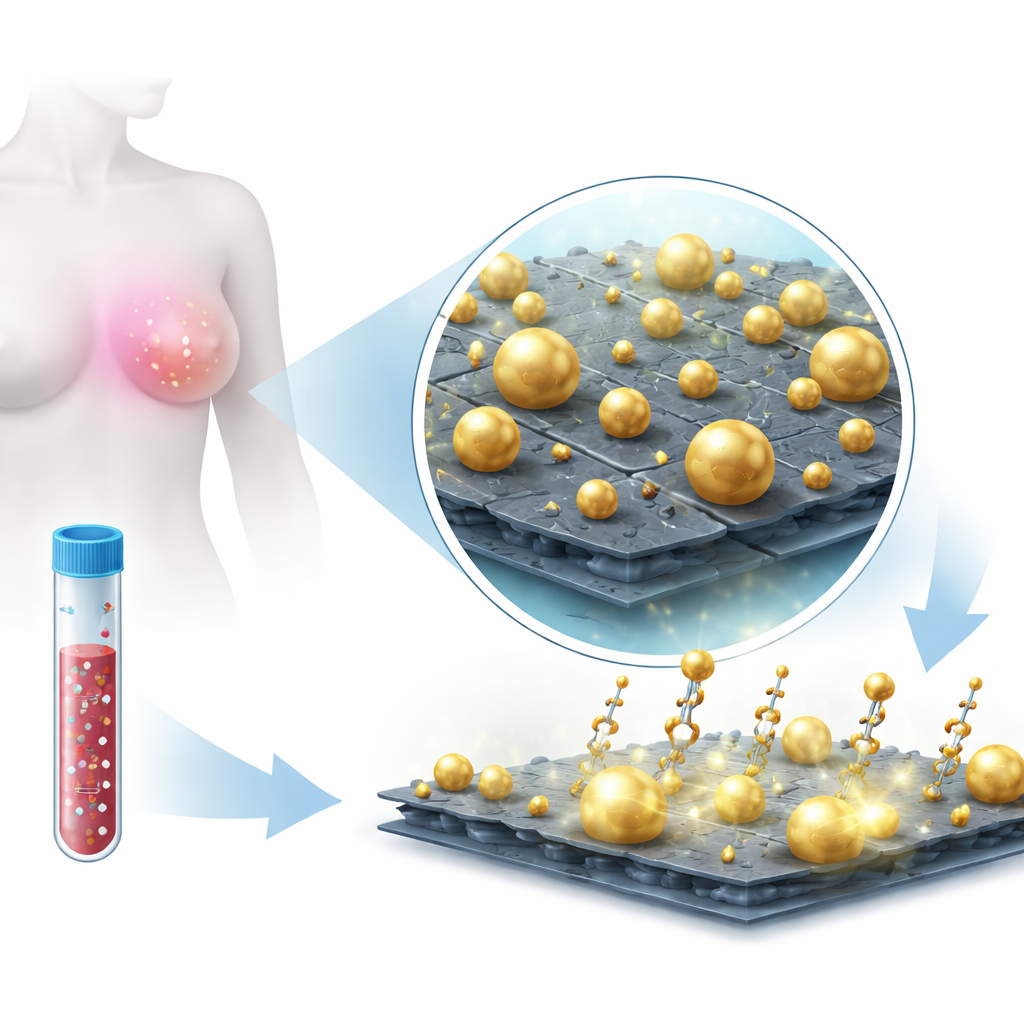
Licht nutzen, um molekulare Fingerabdrücke zu lesen
Die Plattform arbeitet mit Oberflächenverstärkter Raman-Streuung (SERS), einer Technik, bei der Laserlicht an Molekülen gestreut wird und ein spektrales „Fingerabdruck“-Signal zurückgibt. Für sich genommen ist eine MicroRNA zu klein und zu leise, um so einfach erkannt zu werden. Die Forscher verwendeten stattdessen kurze DNA-ähnliche Sonden, sogenannte locked nucleic acids (LNAs), die sich an spezifische MicroRNA-Sequenzen binden, die mit Brustkrebs assoziiert sind — namentlich miR-210-3p und miR-9-3p. Diese Sonden trugen helle Farbstoffmoleküle (Cy3 und Cy5.5), die starke Raman-Fingerabdrücke erzeugen, wenn sie in der Nähe der goldbeschichteten MoS2-Oberfläche gehalten werden. Bindet eine Ziel‑MicroRNA an ihre passende LNA‑Sonde, wird der Farbstoff in die Gold‑„Hotspots“ positioniert, wo das lokale Lichtfeld durch das Zusammenspiel der Metallnanopartikel und der MoS2‑Schicht stark verstärkt wird. Durch Bestrahlung mit einem energiearmen NIR‑Laser konnte das Team klare Raman‑Spektren mit charakteristischen Peaks aufzeichnen, die anzeigen, wie viel MicroRNA vorhanden ist.
Von synthetischen Targets zu echten Krebszellen
Nach Bestätigung von Struktur und Stabilität ihres Nanoverbunds prüften die Forschenden das System mit synthetischen MicroRNA‑Sequenzen zur Kalibrierung und Validierung. Sie stellten fest, dass unterschiedliche spektrale Peaks jeder Farbstoffmarke empfindlich und linear über weite Konzentrationsbereiche reagierten, wodurch sich Nachweisgrenzen bis in den Bereich weniger Billionstel Mol (Pikomolar) berechnen ließen. Wichtig war, dass sie sich nicht auf einen einzelnen Peak verließen, sondern eine Mehrpeak‑Analyse nutzten, um die Zuverlässigkeit insbesondere in komplexen Proben zu erhöhen. Die Plattform wurde anschließend mit MicroRNAs aus einer aggressiven Brustkrebszelllinie getestet. Unabhängige PCR‑Messungen zeigten, dass eine MicroRNA, miR-210-3p, in diesen Zellen deutlich häufiger vorkam als miR-9-3p. Mit demselben SERS‑Aufbau konnte der MoS2–Gold‑Sensor zellabgeleitete miR-210-3p bzw. miR-9-3p bis etwa 0,1 Nanomolar bzw. 0,018 Nanomolar nachweisen, wobei die empfindliche RNA durch schonende Beleuchtung erhalten blieb.
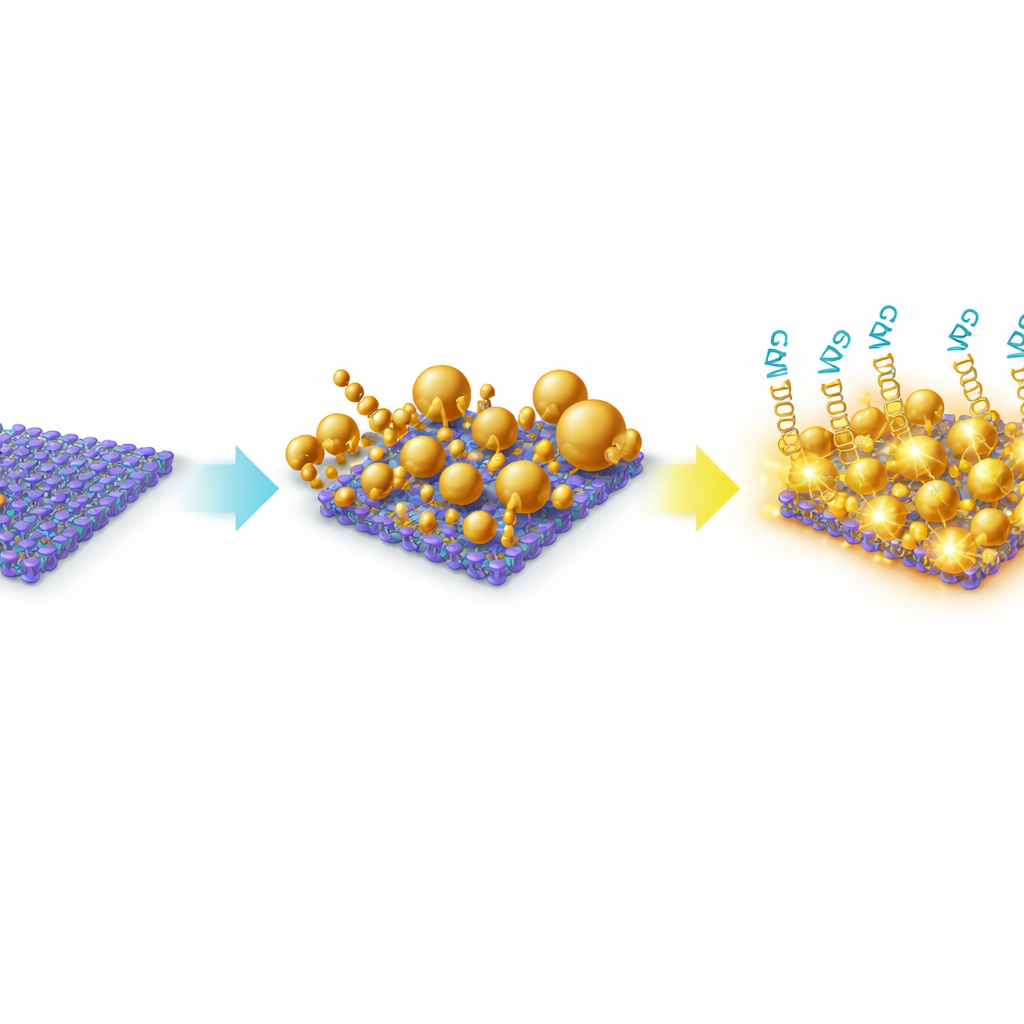
Was das für zukünftige Krebs‑Tests bedeuten könnte
Obwohl diese Arbeit noch im Laborstadium steckt, skizziert sie einen klaren Weg, wie eine sorgfältig entwickelte Nanosurface zu einem praktischen Diagnosewerkzeug werden könnte. Durch das gezielte Wachstum von Gold in unterschiedlichen Formen und Größen auf MoS2 schufen die Forschenden ein dichtes Netzwerk lichtverstärkender Hotspots, das das Vorhandensein spezifischer MicroRNAs über ihre Farbstoff‑Markierungen auslesen kann. Die moderate, aber gut kontrollierte Signalverstärkung kombiniert mit Mehrpeak‑Analysen erlaubt quantitative Nachweise über einen breiten Konzentrationsbereich sowohl in reinen als auch in biologisch komplexen Proben. Langfristig könnte dieser Ansatz kompakte, multiplexe Tests ermöglichen, die mehrere krebsassoziierte MicroRNAs gleichzeitig überwachen, Ärzten ein detaillierteres Bild des Tumorstatus aus kleinen Proben liefern und so potenziell personalisierte Therapieentscheidungen unterstützen.
Zitation: Zablon, F.M., Pathiraja, G., Dellinger, K. et al. In-situ growth of heterogeneous Au on MoS2 nanosheets for SERS detection of breast cancer-derived miR-210-3p and miR-9-3p. Sci Rep 16, 8902 (2026). https://doi.org/10.1038/s41598-026-41084-3
Schlüsselwörter: Biomarker bei Brustkrebs, Detektion von MicroRNA, SERS-Nanosensoren, Gold-Nanopartikel-Komposite, MoS2-basierte Biosensorik