Clear Sky Science · de
Farbstandardisierung in der Histopathologie: Methodenvergleich mit Multizenter-Datensatz
Schärfere Gewebebilder für Ärztinnen, Ärzte und Computer
Wenn Pathologinnen und Pathologen Gewebeproben unter dem Mikroskop betrachten, verlassen sie sich auf feine Schattierungen von Rosa und Violett, um zu entscheiden, ob Zellen gesund oder krebsartig sind. Heute können diese Farben jedoch stark von einem Krankenhauslabor zum anderen variieren, was nicht nur die menschliche Diagnostik erschwert, sondern auch KI-Werkzeuge, die mit diesen Bildern trainiert wurden, stört. Diese Studie hatte zum Ziel, das Ausmaß dieses Farbproblems zu messen und zu prüfen, welche computergestützten Techniken am besten funktionieren, um Präparate so anzugleichen, dass wichtige Details erhalten bleiben.
Warum die Farbe von Labor zu Labor variiert
Die Arbeit konzentriert sich auf das in der Pathologie am häufigsten verwendete Farbpaar Hämatoxylin und Eosin, das Zellkerne bläulich-violett und das umliegende Gewebe rosa färbt. Kleine Unterschiede in der Fixierung, Verarbeitung und Färbung von Gewebe sowie in der Art, wie Scanner Bilder erfassen, können diese Farben drastisch verschieben. Um diesen Effekt kontrolliert zu untersuchen, entnahmen die Autorinnen und Autoren drei winzige Gewebeproben — Haut, Niere und Dickdarm — aus denselben Spenderblöcken und schickten identische unstained Schnitte an 66 Labore in 11 Ländern. Jedes Labor verwendete sein Routine-Färbeprotokoll, danach wurden die fertigen Objektträger digitalisiert. Da das biologische Material nahezu identisch war, spiegelten Unterschiede im Erscheinungsbild hauptsächlich wider, wie jedes Labor das Gewebe gefärbt und bildlich erfasst hatte.
Aufbau eines einzigartigen Testfelds für Farbkorrektur
Die resultierende Bildsammlung zeigte auffällige Variationen: Objektträger aus demselben Gewebeblock reichten von blass bis fast schwarz oder drifteten von kühlen zu sehr warmen Farbtönen. Das Team quantifizierte diese Unterschiede zunächst, indem es die mittleren Rot- und Blauwerte in jedem Bild maß. Sie wählten dann pro Gewebeart einen gut ausbalancierten Referenzträger aus und wandten acht verschiedene Methoden der Farbnormierung auf die übrigen Bilder an. Vier Methoden waren ältere, mathematische Ansätze, die globale Farbstatistiken anpassen oder Färbekomponenten trennen und neu skalieren. Vier weitere basierten auf modernen „generativen“ KI-Verfahren, die mittels neuronaler Netze lernen, Bilder von einem Farbstil in einen anderen zu transformieren.
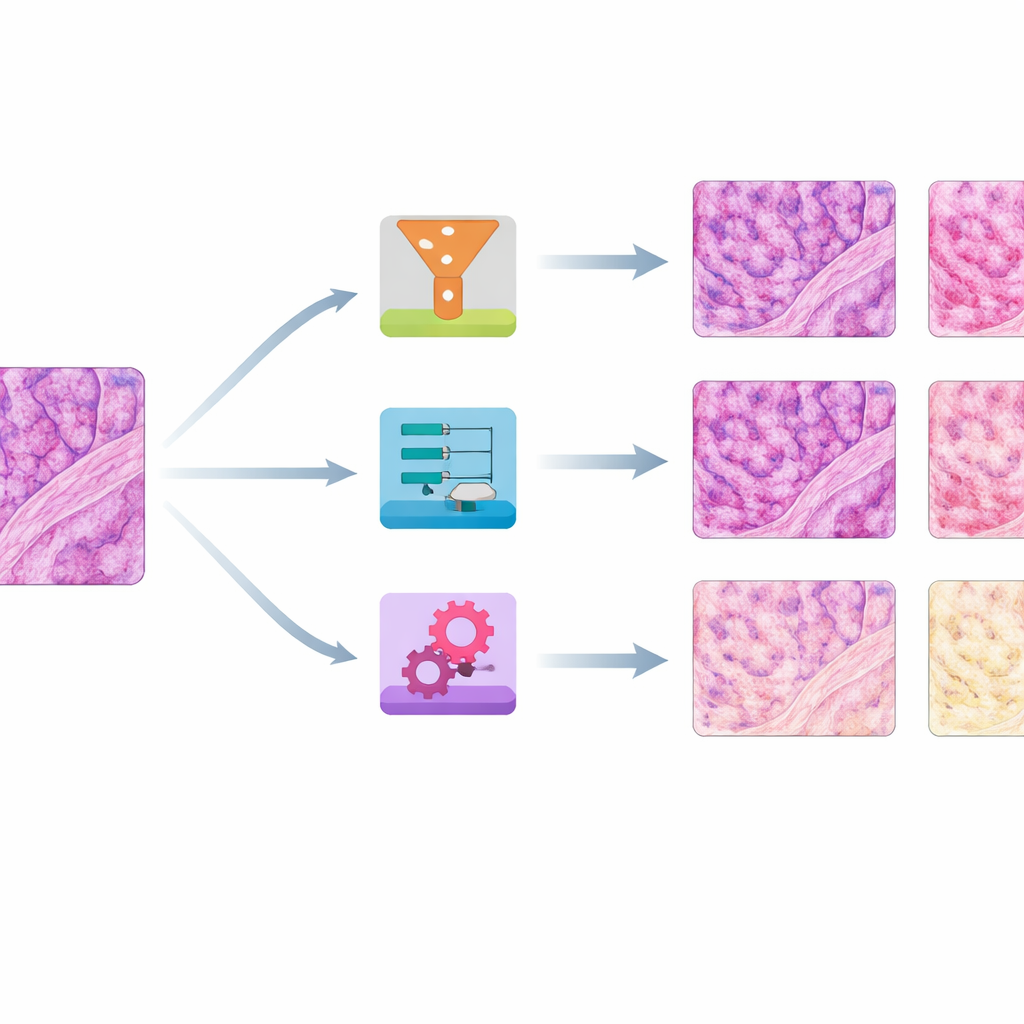
Welche Methoden bei Farbe und Struktur am besten abschnitten
Zur Bewertung stellten die Autorinnen und Autoren zwei Hauptfragen: Wie eng stimmten die korrigierten Bilder mit den Referenzfarben überein, und wie gut blieben feine Gewebestrukturen erhalten? Sie verwendeten mehrere numerische Kennzahlen, die Farbdichteverteilungen vergleichen, eine hochstufige Bildähnlichkeitsmetrik aus der Computer-Vision und einen Strukturindex, der empfindlich gegenüber Unschärfen oder Verzerrungen ist. Über Haut, Niere und Dickdarm hinweg lieferte eine einfache Methode namens Histogram Matching — im Wesentlichen das Umformen der Farbdaten jedes Bildes, um die Referenz zu imitieren — durchgängig die engste Farbangleichung bei gleichzeitig weitgehend intakter Struktur. Ein weiterer traditioneller Ansatz, die Reinhard-Normalisierung, war oft nahezu ebenso gut. Die Methode von Vahadane zeichnete sich beim Strukturenschutz aus, neigte jedoch dazu, alles in einen rosa Ton zu drücken und das blaue Kernfärbemittel zu unterdrücken.
Wie die Bilder für Expertinnen, Experten und KI wirkten
Erfahrene Pathologinnen und Pathologen begutachteten normalisierte Dickdarmproben, um zu sehen, wie sich die Methoden auf die praktische Interpretierbarkeit auswirkten. Sie prüften, ob wichtige Schichten und Zelltypen weiterhin gut zu unterscheiden waren, ob stark über- oder unterfärbte Originale verbessert wurden und ob ungewöhnliche digitale Artefakte auftauchten. Keine einzelne Methode löste jedes Problem, aber Histogram Matching erzeugte allgemein gleichmäßige, referenzähnliche Farben ohne offensichtliche Artefakte, besonders bei stark überfärbten Proben. Einige KI-basierte Methoden, insbesondere bestimmte Varianten von CycleGAN und Pix2pix, lieferten realistisch wirkende Ergebnisse, führten aber gelegentlich zu subtilen künstlichen Strukturen oder Farbfehlern in Blutzellen und Hintergrundbereichen. Das Team zeigte außerdem, dass Normalisierung beeinflusste, wie ein moderner Zell-Erkennungsalgorithmus Kerne zählte und wie ein großes „Foundation“-Modell die Präparate darstellte — ein Hinweis darauf, dass Farbkorrektur das Verhalten nachgeschalteter KI-Systeme stark beeinflussen kann.
Was das für die zukünftige digitale Diagnose bedeutet
Insgesamt zeigt die Studie, dass Farbunterschiede zwischen Laboren groß genug sind, um sowohl für menschliche Gutachter als auch für automatisierte Systeme relevant zu sein, und dass eine Vereinheitlichung der Bilder ein wichtiger Schritt hin zu zuverlässiger, geteilter digitaler Pathologie ist. Überraschenderweise übertrafen in diesem sorgfältig kontrollierten Datensatz mit sehr ähnlichem Gewebeinhalt einfache globale Methoden wie Histogram Matching häufig komplexere Deep-Learning-Techniken, die deutlich mehr Trainingsdaten benötigen als ein einziger Referenzträger pro Labor. Die Autorinnen und Autoren stellen ihren 66-Zentren-Datensatz offen zur Verfügung, damit andere neue Methoden benchmarken und Trainingsdaten besser gestalten können, sodass sie die reale Variation widerspiegeln. Für Patientinnen und Patienten könnte Fortschritt in diesem Bereich bedeuten, dass KI-Systeme zuverlässig zwischen Krankenhäusern „funktionieren“ und konsistentere Diagnosen liefern, unabhängig davon, wo eine Biopsie bearbeitet wird.
Zitation: Khan, U., Härkönen, J., Friman, M. et al. Staining normalization in histopathology: Method benchmarking using multicenter dataset. Sci Rep 16, 11097 (2026). https://doi.org/10.1038/s41598-026-40943-3
Schlüsselwörter: digitale Pathologie, Farbnormalisierung, Histologie-Bildgebung, medizinische KI, Farbvariation