Clear Sky Science · de
Pan‑kancer Gefrierschnitt‑Klassifikation mittels eines Soft‑Mixture‑of‑Experts Vision Transformer unter schwacher Aufsicht
Warum das im Operationssaal wichtig ist
Wenn Chirurgen einen verdächtigen Tumor entfernen, haben sie oft nur Minuten Zeit, um herauszufinden, ob sämtliches Krebsgewebe entfernt wurde. Pathologen arbeiten unter Zeitdruck, um einen schnell gefrorenen Gewebeschnitt zu untersuchen und eine Antwort zu geben, während der Patient noch am Tisch liegt. Dieser hochgradig belastende Prozess kann durch unscharfe Schnitte, unauffällige Tumoren und einfache Zeitlimitierungen erschwert werden. Die hier beschriebene Studie untersucht, wie ein System der künstlichen Intelligenz (KI) Pathologen helfen kann, schnell und zuverlässig harmloses von gefährlichem Gewebe über viele Organe hinweg zu unterscheiden — und zwar mit Geräten, die für den Krankenhausalltag realistisch sind.
Ein schneller Test mit eingebauten Herausforderungen
Die Gefrierschnitt‑Analyse ist ein Grundpfeiler der modernen Chirurgie: Ein dünnes Gewebestück wird eingefroren, geschnitten, gefärbt und unter dem Mikroskop betrachtet, um zu beurteilen, ob es gut‑ oder bösartig ist und ob die Resektionsränder sauber sind. Im Gegensatz zu Dauerpräparaten leiden Gefrierschnitte häufig unter Rissen, Falten und ungleichmäßiger Färbung. Bei Grenzfällen können Pathologen unterschiedlicher Meinung sein, und die Zeit drängt stets. Diese Probleme sind besonders gravierend in kleineren oder stark frequentierten Krankenhäusern, wo nur wenige Spezialisten viele Krebsarten abdecken müssen. Die Autoren argumentieren, dass ein robustes computerbasiertes Assistenzsystem Gefrierschnitt‑Entscheidungen konsistenter, schneller und breiter verfügbar machen könnte.
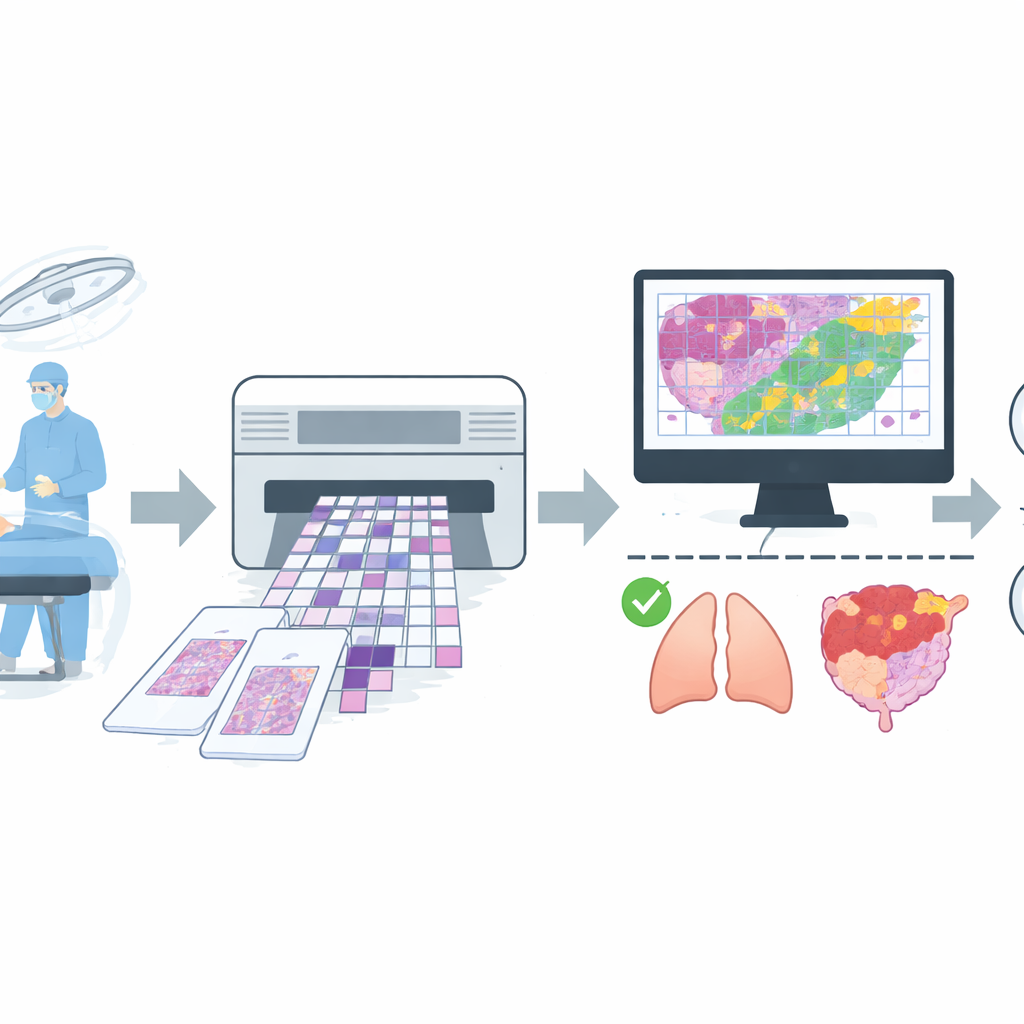
Aufbau eines breit gefächerten realen Bildbestands
Um einen solchen Assistenten zu trainieren, stellte das Team eine große Sammlung digitaler Bilder aus Routineeingriffen eines großen Krankenhauses zusammen. Sie sammelten 4.754 Whole‑Slide‑Bilder von Gefrierschnitten aus mehr als 2.600 Patienten und wendeten dann strenge Qualitätskriterien an, um Schnitte mit schweren Artefakten oder unsicheren Diagnosen zu entfernen. Der endgültige Datensatz enthielt 4.667 Schnitte, jeweils einfach als gut‑ oder bösartig etikettiert, basierend auf der Übereinstimmung zwischen der schnellen Gefrierschnitt‑Beurteilung und dem späteren, sorgfältigeren Bericht der Dauerpräparate. Die Schnitte deckten häufige Lokalisationen wie Lunge, Brust, Schilddrüse, Lymphknoten und weibliche Fortpflanzungsorgane ab, zudem eine gemischte Gruppe weniger häufiger Orte wie Magen, Leber und Haut. Die Daten wurden in getrennte Gruppen für Training, Feinabstimmung und abschließende Tests aufgeteilt, wobei darauf geachtet wurde, dass Bilder desselben Patienten nie in mehr als einer Gruppe erschienen.
Wie die KI aus schwachen Hinweisen lernt
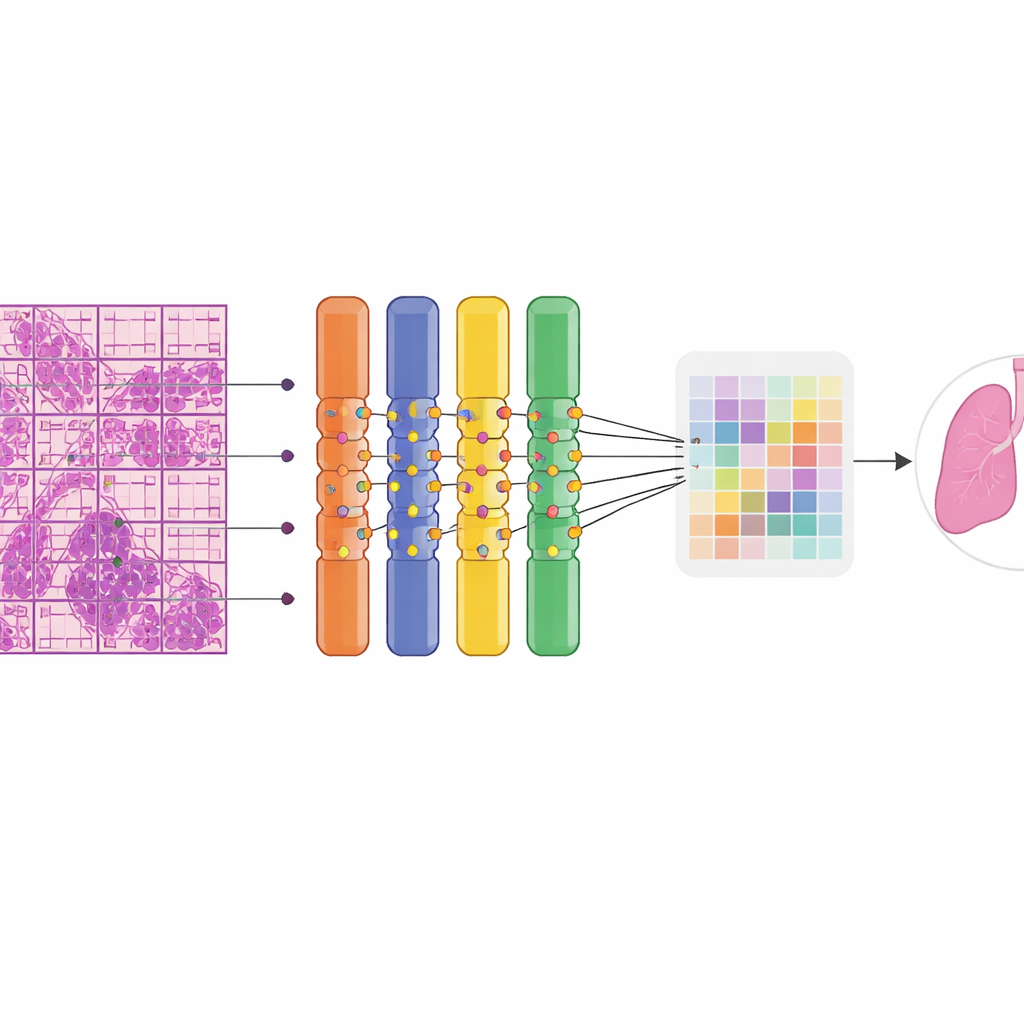
Die Forschenden bauten ihr Modell auf einer Klasse neuronaler Netze auf, die als Vision Transformer bekannt ist und sich besonders für das Erkennen von Mustern in großen Bildern eignet. Jedes riesige Gewebebild wurde automatisch in viele kleinere Kacheln und Patches zerlegt, damit es auf standardmäßiger Grafikhardware verarbeitet werden kann. Eine zentrale Innovation war der Ersatz eines Teils des Netzes durch eine „soft mixture of experts“, einen Satz vieler kleiner Spezial‑Zweige, die sich jeweils auf unterschiedliche visuelle Muster konzentrieren. Anstatt Experten an‑ und auszuschalten, vermischt das System deren Beiträge fließend, was das Training stabilisiert und die Nutzung begrenzter Daten verbessert. Da Pathologen keine Umrisse um Tumoren zeichneten, musste das Modell aus schwacher Aufsicht lernen: Es wusste nur, ob ein ganzer Schnitt gut‑ oder bösartig war. Eine Multiple‑Instance‑Learning‑Strategie förderte die verdächtigsten Patches innerhalb eines bösartigen Schnitts als positive Beispiele, sodass das Netzwerk schrittweise auf die informativeren Regionen fokussieren konnte.
Wie gut das System in der Praxis funktioniert
Getestet an 669 bislang ungesehenen Schnitten unterschied die KI gut‑ von bösartigem Gewebe mit hoher Genauigkeit. Sie klassifizierte insgesamt etwa 90 % der Fälle korrekt und zeigte eine ausgezeichnete Trennfähigkeit der beiden Gruppen über Wahrscheinlichkeitsschwellen hinweg. Die Sensitivität — die Wahrscheinlichkeit, einen tatsächlich bösartigen Schnitt zu erkennen — lag bei rund vier von fünf, während die Spezifität — die Wahrscheinlichkeit, einen gutartigen Schnitt korrekt als gutartig einzustufen — noch höher war. Wichtig ist, dass die Leistung organübergreifend stabil blieb: Sie erkannte im Testset alle bösartigen Lungen‑ und Brustfälle fehlerfrei und lieferte auch gute Ergebnisse bei selteneren Gruppen wie Adnex‑Tumoren der Frau und den gemischten „anderen“ Organen. Farblich überlagerte Heatmaps zeigten, dass sich die Aufmerksamkeit des Modells auf Regionen konzentrierte, die Fachpathologen als Tumor anerkennen, einschließlich metastatischer Herde in Lymphknoten, während normale Strukturen weitgehend ignoriert wurden. Das System lief effizient und benötigte weniger als 5 GB Speicher, wodurch es für gängige Grafikkarten und nicht nur für teure Rechencluster geeignet ist.
Begrenzungen, Fehlgriffe und Verbesserungsmöglichkeiten
Die Autoren untersuchten auch, wo die KI schwächelte. Falsch‑negative Ergebnisse betrafen häufig extrem spärliche Krebszellen, unscharfe Scanbereiche oder starke Entzündungen, die maligne Inseln verschleierten. Falsch‑positive Befunde traten eher bei benignen Zuständen auf, die unter dem Mikroskop Krebs nachahmen, etwa reaktive Überwüchse oder verzerrtes Gefrierschnittgewebe. Da routinemäßige chirurgische Abläufe keine detaillierten Umrisse der Tumorregionen enthalten, konnte das Team nicht exakt quantifizieren, wie gut die Heatmaps mit Expertenmarkierungen übereinstimmen, und stützte sich stattdessen auf qualitative Begutachtung. Einige Organarten, etwa Zunge oder bestimmte Weichteiltumoren, blieben unterrepräsentiert, was darauf hinweist, dass größere, multizentrische Sammlungen nötig sein werden, um die Reichweite des Systems zu erweitern.
Was das für Patienten und Krankenhäuser bedeuten könnte
Insgesamt zeigt die Studie, dass ein sorgfältig gestaltetes KI‑System eine genaue und interpretierbare Unterstützung bei einer Kernaufgabe der chirurgischen Pathologie bieten kann: in Echtzeit zu entscheiden, ob Gewebe über viele Organtypen hinweg gut‑ oder bösartig ist. Indem es nur Schnittebene‑Labels verwendet, auf weit verbreiteter Hardware läuft und verdächtige Bereiche zur menschlichen Überprüfung hervorhebt, bietet das Modell einen praxisnahen Weg zu konsistenteren Gefrierschnitt‑Entscheidungen. Für Patienten könnte das bedeuten, dass Operationen besser informiert in einem einzigen Eingriff erfolgen; für Krankenhäuser, insbesondere solche mit begrenztem Expertenpersonal, deutet es auf eine Zukunft, in der fortschrittliche digitale Werkzeuge helfen, qualitativ hochwertige Krebsversorgung gerechter bereitzustellen.
Zitation: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
Schlüsselwörter: Gefrierschnitt, digitale Pathologie, Krebsdiagnose, Vision Transformer, schwach überwachtes Lernen