Clear Sky Science · de
Erklärbare KI für die Überwachung gastrointestinaler Läsionen und präzise zielgerichtete Medikamentenabgabe
Intelligentere Scans, sicherere Behandlungen
Viele Menschen fürchten Krebsmedikamente wegen ihrer starken Nebenwirkungen. Diese Forschung skizziert eine Zukunft, in der winzige schluckbare Kameras, intelligente Algorithmen und mikroskopische Wirkstoffträger zusammenarbeiten, sodass starke Arzneien nur dort ankommen, wo sie wirklich benötigt werden. Indem die Schleife zwischen dem Erkennen eines Problems im Darm und der sofortigen Behandlung geschlossen wird, wollen die Autorinnen und Autoren die gastrointestinale Versorgung genauer, weniger invasiv und deutlich sicherer machen.
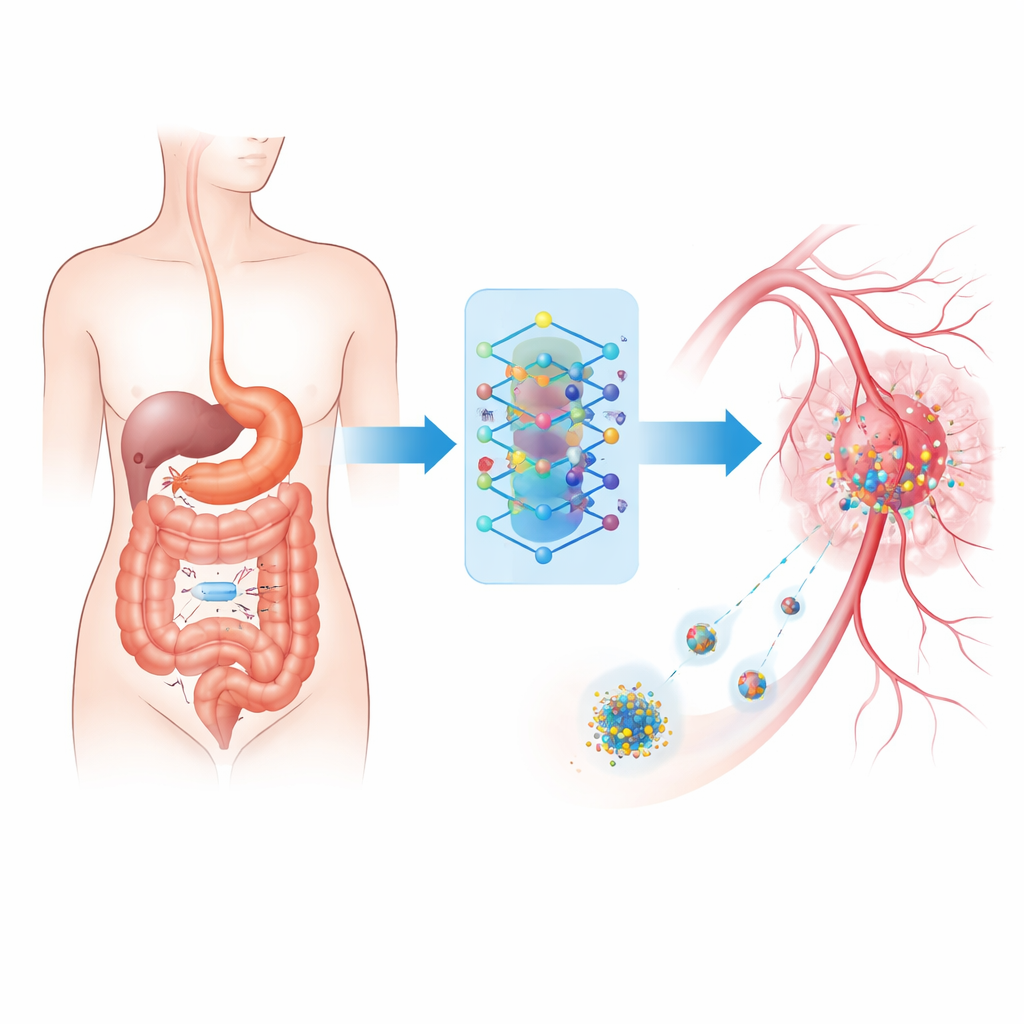
Kleine Kamera auf Reisen
Im Zentrum des Systems steht ein drahtloses, verschluckbares Bildgebungsgerät – eine vitamingroße Kapsel, die auf natürliche Weise durch den Verdauungstrakt wandert und dabei Zehntausende Bilder aufnimmt. Anstatt allein auf eine Ärztin oder einen Arzt zu bauen, die diese Bilderflut manuell auswerten, sendet die Kapsel die Aufnahmen an eine außerhalb des Körpers getragene Einheit. Dort sortiert ein kompakter Rechner mit fortschrittlicher Mustererkennungssoftware normales Gewebe von verdächtigen Läsionen, die krebsartig oder stark entzündet sein könnten. Dieses Setup ähnelt der bereits in Kliniken eingesetzten Kapselendoskopie, ist jedoch so erweitert, dass es in Echtzeit arbeitet und direkt mit Behandlungstools verbunden werden kann.
Künstliche Intelligenz als Entscheidungsträger
Die tragbare Einheit führt ein sorgfältig trainiertes Bildanalysemodell aus, das auf modernen Computer‑Vision‑Techniken beruht. Es lernte, 25 verschiedene gastrointestinale Zustände zu erkennen – von Polypen und Geschwüren bis hin zu starken Entzündungen – mithilfe einer großen öffentlichen Sammlung von Endoskopie‑ und Gewebebildern. Um mit der Tatsache umzugehen, dass einige Krankheiten viel seltener sind als andere, trainierten die Autorinnen und Autoren das System in zwei Stufen: Zuerst, um die allgemeinen visuellen Fingerabdrücke jeder Erkrankung zu lernen, und dann, um es so zu verfeinern, dass gefährliche, aber seltene Befunde nicht übersehen werden. In Tests klassifizierte dieser Ansatz Bilder in mehr als neun von zehn Fällen korrekt und schnitt insbesondere bei krebsbezogenen Kategorien sehr gut ab.
Ins Innere der „Black Box“ blicken
Da medizinisches Personal automatisierten Diagnosen, die eine Medikamentendosis beeinflussen könnten, vertrauen muss, nutzten die Autorinnen und Autoren erklärbare KI‑Techniken, um aufzuzeigen, welche Teile jedes Bildes die Entscheidung des Modells beeinflussen. Heatmap‑artige Überlagerungen heben die genauen Regionen hervor, die das System für wichtig hielt. Diese Erklärungs‑Maps wurden nicht nur visuell geprüft; sie wurden mit quantitativen Tests bewertet, die maßen, wie sehr sich das Vertrauen des Modells änderte, wenn hervorgehobene Bereiche entfernt oder hinzugefügt wurden, wie stabil die Erklärungen über wiederholte Trainingsläufe hinweg waren und wie gut sie mit von Expertinnen und Experten gezeichneten Läsionsumrissen übereinstimmten. Unter mehreren getesteten Methoden erzeugte eine namens LayerCAM die treuesten und konsistentesten Erklärungen und half so Ärztinnen und Ärzten zu verifizieren, dass das System an der richtigen Stelle „hinblickt“.
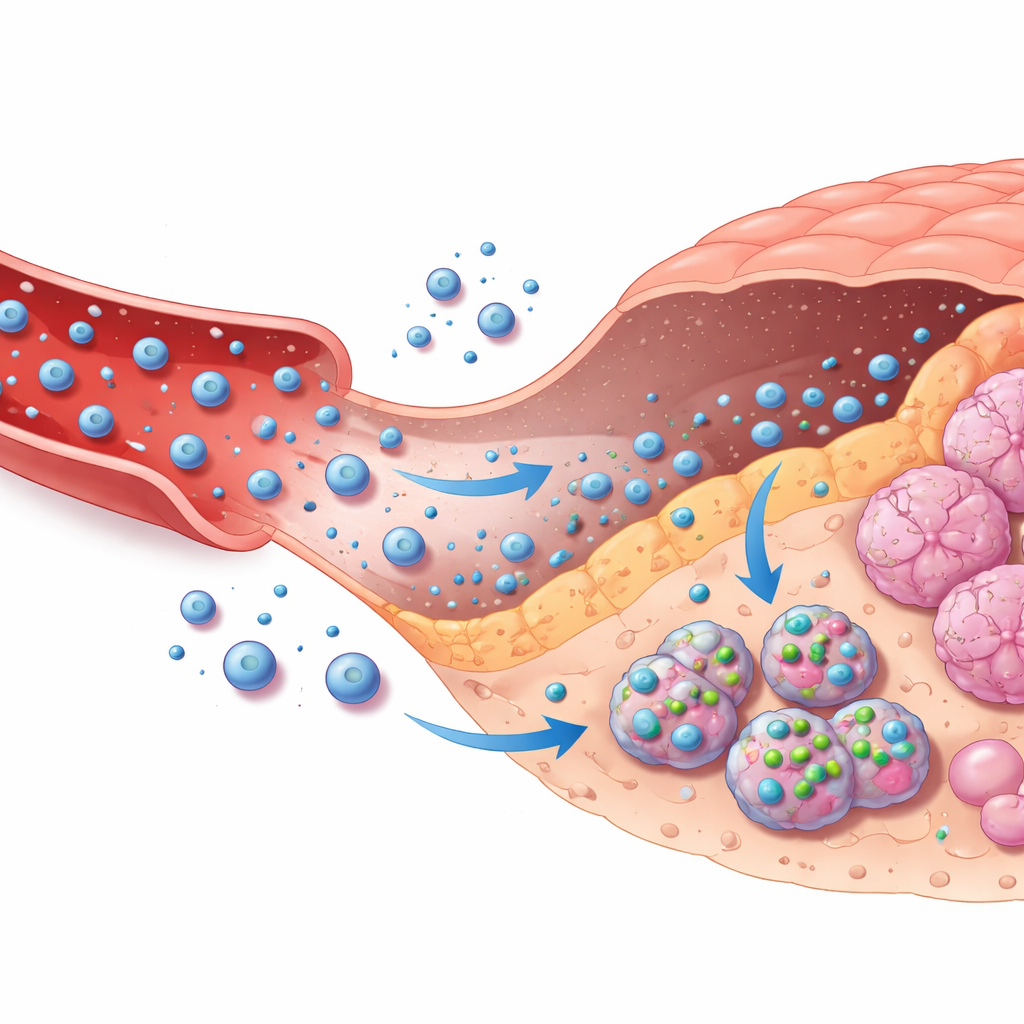
Wegweisung von Wirkstoffträgern durch den Körper
Die zweite Hälfte des Rahmens verbindet diese bildbasierten Entscheidungen mit einer zielgerichteten Chemotherapieabgabe. Die Autorinnen und Autoren modellieren, wie ein verbreitetes Krebsmedikament, Doxorubicin, von einer externen Pumpe durch die Blutbahn transportiert wird, in Tumorgewebe austritt, in Tumorzellen eindringt und schließlich eliminiert wird. Dies wird in einem Mehrkompartiment‑mathematischen Modell erfasst, das Wirkstoffspiegel im Blut, im umgebenden Gewebe und innerhalb der Zellen nachverfolgt. Basierend auf dem Vertrauen der KI in eine bösartige Läsion und der Einschätzung ihrer Schwere wählt ein einfaches Regelsystem zwischen keiner Behandlung, moderater Behandlung oder intensiver Behandlung, passt an, wie schnell mit Wirkstoff beladene Nanopartikel ihren Inhalt freisetzen und wie lange die Infusion dauert. Eine Sicherheitsschicht überprüft kontinuierlich die vorhergesagten Wirkstoffspiegel innerhalb der Zellen und reduziert automatisch die Dosierung, wenn eine sichere Obergrenze erreicht wird, selbst wenn die KI zu selbstsicher ist.
Privatsphäre schützen und Missbrauch verhindern
Da derselbe Kanal, der Bilder überträgt, auch Behandlungskommandos transportieren kann, ist Sicherheit entscheidend. Die Autorinnen und Autoren stellen ein leichtgewichtiges Datenschutzschema vor, das biomedizinische Signale vor ihrer Weiterleitung durch das Nano‑Netzwerk des Körpers mittels einer chaotischen mathematischen Abbildung verschlüsselt, sodass abgefangene Daten sehr schwer zu interpretieren sind. Darüber hinaus authentifiziert das tragbare Gateway Geräte und prüft, ob Steuersignale erwarteten physikalischen Mustern entsprechen, um gefälschte Befehle zu blockieren. Simulationen zeigen, wie unterschiedliche Datenschutzeinstellungen einen kleinen Verlust an Erkennungsgenauigkeit gegen stärkeren Schutz abwägen und identifizieren Betriebszustände, die die klinische Leistungsfähigkeit hoch halten und gleichzeitig Datenlecks stark einschränken. Zusammen mit strengen Dosislimits, Notabschaltregeln und Sicherheitsprotokollen sollen diese Maßnahmen das System gegen Unfälle und Angriffe widerstandsfähig machen.
Was das für Patientinnen und Patienten bedeuten könnte
Kurz gesagt skizziert diese Arbeit, wie eine „sehen‑und‑behandeln“‑Schleife im Körper funktionieren könnte: Eine verschluckbare Kamera findet verdächtige Stellen, eine intelligente Assistenz interpretiert das Gesehene mit transparenten Begründungen, und ein kontrolliertes Wirkstoffabgabesystem reagiert mit sorgfältig begrenzten Dosen, die auf krankes Gewebe fokussiert sind. Die Studie ist noch theoretisch und basiert auf Simulationen, zeigt aber, dass ein solches Closed‑Loop‑Design therapeutische Ziele erreichen und gleichzeitig strenge Sicherheitsgrenzen einhalten kann, selbst wenn die KI Fehler macht oder die Bedingungen von Person zu Person variieren. Wenn es in der Praxis realisiert wird, könnte ein solches System die grobe Chemotherapie in ein weitaus präziseres und personalisiertes Instrument zur Behandlung gastrointestinaler Erkrankungen verwandeln.
Zitation: Kamal, I.R., El-Zoghdy, S.F. & Soliman, R.F. Explainable AI for gastrointestinal lesion surveillance and precision targeted drug delivery. Sci Rep 16, 9807 (2026). https://doi.org/10.1038/s41598-026-40882-z
Schlüsselwörter: gastrointestinale Bildgebung, erklärbare KI, zielgerichtete Medikamentenabgabe, Nanomedizin, Kapselendoskopie