Clear Sky Science · de
Zielgerichtete Aktivierung von Nrf2 mittels sulforaphan-beladener Exosomen milderte azoospermische Zustände im Rattenmodell
Warum das für die Männergesundheit wichtig ist
Azoospermie, das vollständige Fehlen von Spermien im Ejakulat, ist eine der schwersten und am schwierigsten zu behandelnden Formen männlicher Unfruchtbarkeit. Viele Männer entwickeln diesen Zustand nach einer Chemotherapie, die das Hodengewebe schädigt. Aktuelle Therapien können die Spermienproduktion oft nicht wieder anstoßen, sodass assistierte Reproduktion die einzige verbleibende Option ist. Diese Studie untersucht eine eher natürliche Reparaturstrategie: winzige biologische Bläschen, sogenannte Exosomen, zu nutzen, um eine aus Brokkoli stammende Verbindung direkt in geschädigte Hoden zu transportieren und diese zur erneuten Spermienbildung anzuregen.
Schäden durch Krebstherapie
Chemotherapeutika wie Busulfan sind starke Krebsbekämpfer, können aber auch die Keimzellen in den Hoden, die Spermien produzieren, vernichten. Im hier verwendeten Rattenmodell führte eine einzige Injektion von Busulfan in die Hoden zu einem starken Abfall von Spermienzahl und -beweglichkeit, zu einem Anstieg missgebildeter Spermien und zu einer Verringerung des Hodengewichts. Mikroskopische Untersuchungen zeigten, dass die normale geschichtete Struktur der spermienproduzierenden Tubuli zusammengebrochen war, viele Zellen tot oder fehlend und narbenähnliches Gewebe dazwischen entstanden war. Auch die Testosteronwerte sanken, was darauf hindeutet, dass die Hormonproduktion ebenfalls beeinträchtigt war.
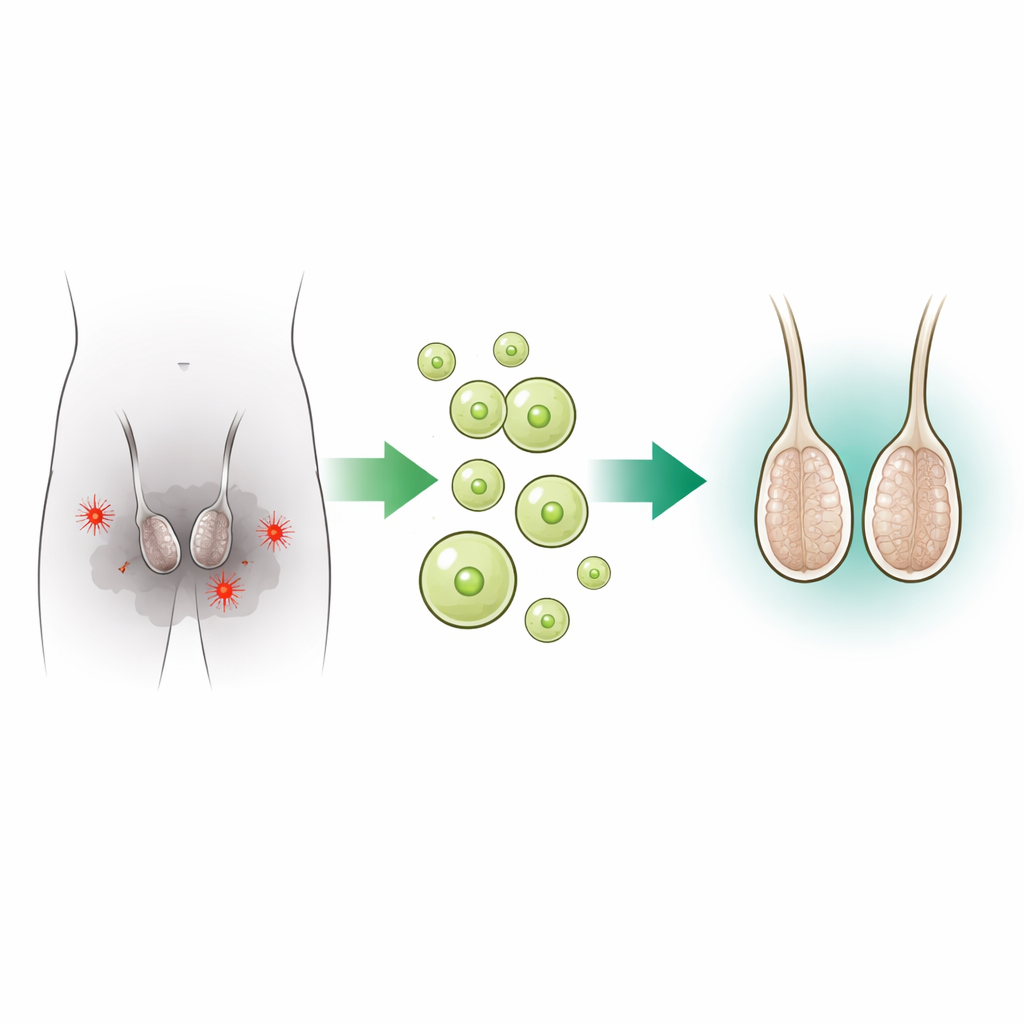
Exosomen als winzige Lieferkapseln
Um diesen Schäden zu begegnen, griffen die Forschenden zu Exosomen, natürlichen nano‑großen Paketen, die Zellen nutzen, um Moleküle auszutauschen. Sie isolierten Exosomen aus gespendetem menschlichem Serum und bestätigten deren Größe und Form mit mehreren Methoden. Anschließend beluden sie diese Vesikel mit Sulforaphan, einer Pflanzenverbindung, die vor allem in Brokkoli und anderen Kreuzblütlern reichlich vorkommt. Sulforaphan ist ein starker Aktivator von Nrf2, einem Protein, das Zellen hilft, antioxidative Abwehrmechanismen zu aktivieren und mit Stress umzugehen. Durch das Verpacken von Sulforaphan in Exosomen und die direkte Injektion in Rattenhoden hoffte das Team, die lokale Wirkung zu verstärken und gleichzeitig die Instabilität und schlechte Bioverfügbarkeit von freiem Sulforaphan zu umgehen.
Spermien wiederherstellen und Gewebe aufbauen
Die Ratten wurden in fünf Gruppen eingeteilt: gesunde Kontrollen, unbehandelte azoospermische Tiere und drei Behandlungsgruppen, die entweder Sulforaphan allein, leere Exosomen allein oder Sulforaphan‑beladene Exosomen erhielten. Zwei Monate nach einer einzigen Injektion hob sich die Kombinationstherapie deutlich hervor. Ratten, die Sulforaphan‑beladene Exosomen erhalten hatten, zeigten deutlich höhere Spermienzahlen und -beweglichkeit, weniger fehlgebildete Spermien und einen höheren Hodengewichtsindex als unbehandelte Tiere oder solche, die nur eine der Komponenten erhielten. Unter dem Mikroskop zeigten ihre Hoden eine nahezu normale Anordnung von Keimzellen in allen Entwicklungsstadien, von stammzellähnlichen Vorläufern bis zu reifen Spermien, und deutlich weniger faserige Narbenbildung. Die Expression wichtiger Keimzellgene, DAZL und VASA, die durch Busulfan stark reduziert worden war, kehrte nur in der Kombinationsgruppe zu Werten ähnlich denen der gesunden Kontrollen zurück.
Stress‑ und Aufräum‑Systeme der Zelle zurücksetzen
Die Studie untersuchte außerdem, wie die Behandlung interne Stressreaktionswege beeinflusste. Nach Busulfan‑Schaden zeigten die Hoden Anzeichen eines oxidativen Ungleichgewichts: Das Nrf2‑Gen, das antioxidative Abwehrwege koordiniert, war ungewöhnlich erhöht, und Gene, die an der zellulären "Aufräumarbeit" über Autophagie beteiligt sind, waren ebenfalls überaktiv. Eine solche andauernde Aktivierung kann eher auf ungelöste Schäden als auf Schutz hinweisen. Sulforaphan‑beladene Exosomen brachten Nrf2 und die autophagiebezogenen Gene LC3, Beclin1 und p62 wieder in Richtung Normalwerte, während sie gleichzeitig die Aktivität antioxidativer Abwehrmechanismen wie der Glutathionperoxidase und die allgemeine antioxidative Kapazität steigerten. Sulforaphan oder Exosomen allein veränderten diese Marker zwar in die richtige Richtung, normalisierten sie aber nicht so vollständig. Auch die Testosteronwerte verbesserten sich am stärksten in der Kombinationsgruppe, was auf eine bessere Erholung der hormonproduzierenden Zellen hindeutet.
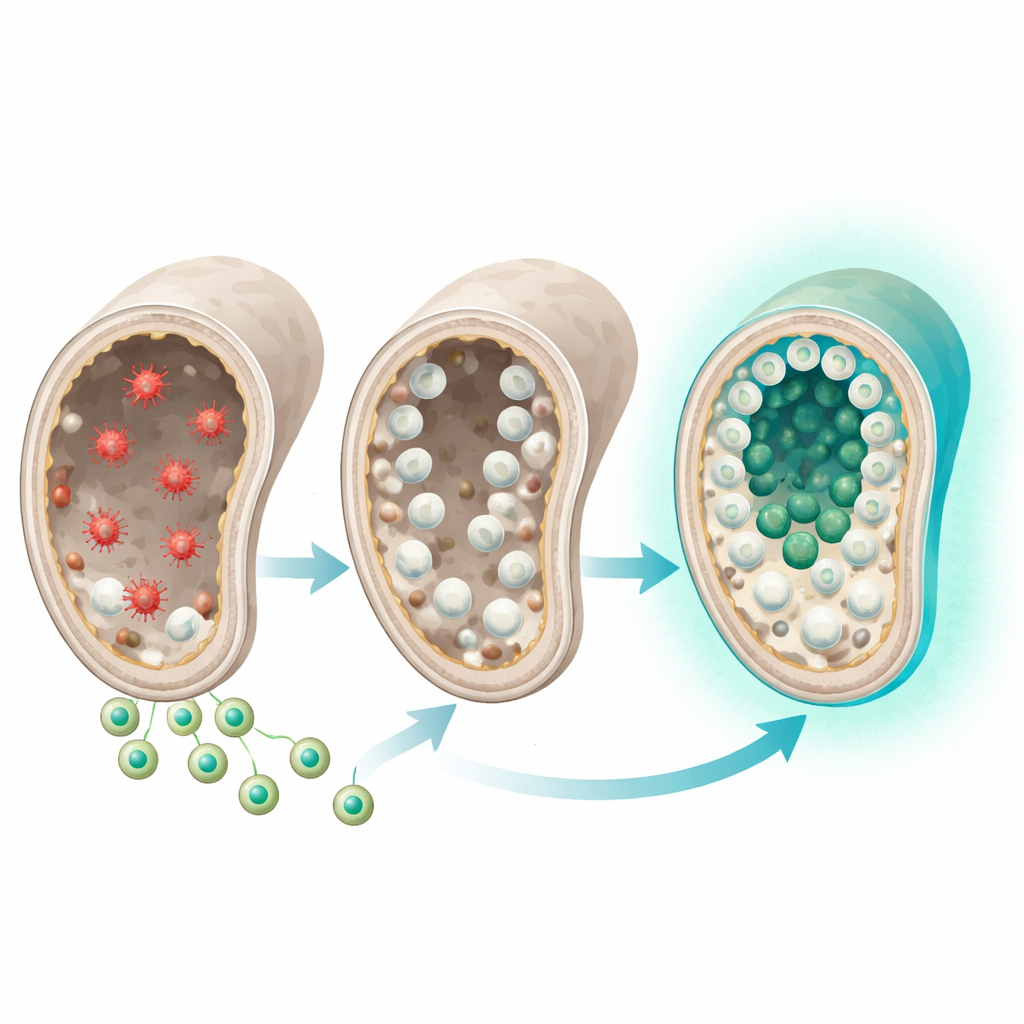
Ein neuer Weg zur Wiederherstellung der Fruchtbarkeit
Insgesamt deuten die Ergebnisse darauf hin, dass sulforaphan‑beladene Exosomen geschädigte Hoden aus einem chronischen Stresszustand heraus und in Richtung eines ausgewogenen Selbstreparaturprozesses steuern können. Indem sie antioxidantische und Aufräumwege fein justieren, ermöglichte diese gezielte Therapie den Keimzell‑Stammzellpopulationen, sich zu erholen und in einem Rattenmodell der chemotherapieinduzierten Azoospermie wieder reife Spermien zu produzieren. Zwar bleibt noch viel zu tun — etwa Langzeitsicherheitstests, Dosisoptimierung und die Bestätigung, dass Nachkommen gesund sind — doch dieser Ansatz deutet auf eine Zukunft hin, in der manche Formen männlicher Unfruchtbarkeit nicht nur durch das Auffinden seltener verbleibender Spermien behandelt werden, sondern dadurch, dass die Hoden ihre natürliche spermienproduzierende Funktion regenerieren können.
Zitation: Ahmadian, S., Fajri, M., Roelen, B.A. et al. Targeted activation of Nrf2 via sulforaphane-loaded exosomes attenuated azoospermic condition in the rat model. Sci Rep 16, 9752 (2026). https://doi.org/10.1038/s41598-026-40709-x
Schlüsselwörter: Azoospermie, männliche Unfruchtbarkeit, Exosomentherapie, Sulforaphan, oxidativer Stress