Clear Sky Science · de
Ein aus Spleißen stammendes MicroRNA aus Amelogenin Exon4 reguliert die Schmelzbildung durch Kontrolle von Exon4-Spleißen und Amelogenin-Expression
Warum eine winzige RNA für feste Zähne wichtig ist
Zahnschmelz ist die härteste Substanz im menschlichen Körper, kann aber überraschend anfällig sein, wenn seine Ausbildung gestört ist. Diese Studie zeigt, wie ein sehr kleines Stück genetischen Materials, eine MicroRNA namens miR‑exon4, Zellen, die Zähne bilden, dabei hilft, richtig gehärteten Schmelz aufzubauen. Indem sie aufzeigt, dass diese MicroRNA sowohl das wichtigste Schmelzprotein als auch das Timing der Mineralablagerung fein reguliert, verknüpft die Arbeit subtilen RNA‑Prozessierungsvorgang in Zellen mit sichtbaren Schmelzdefekten, ähnlich denen einer erblichen Erkrankung namens Amelogenesis imperfecta.
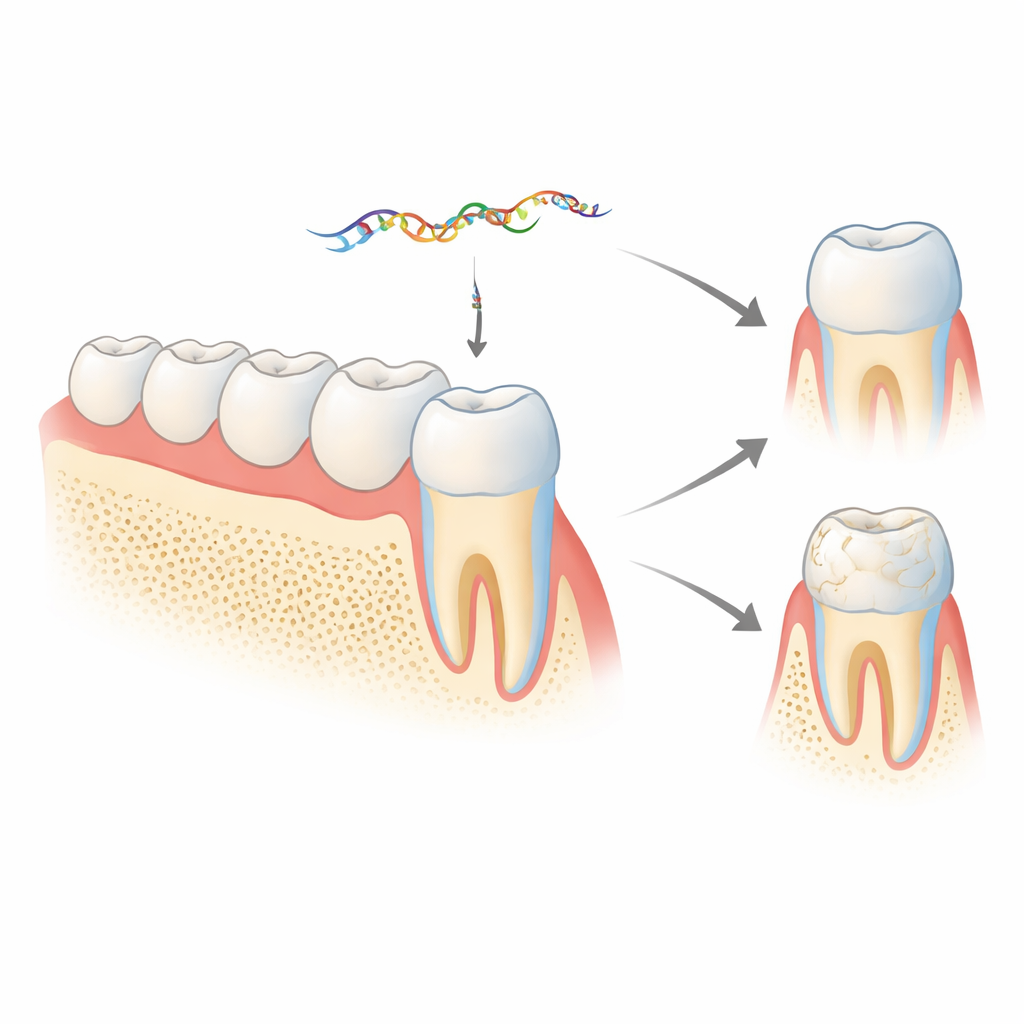
Eine versteckte Botschaft in einem Schmelzgen
Schmelz wird überwiegend aus einem Protein namens Amelogenin aufgebaut, das von Zellen, den Ameloblasten, produziert wird. Das Amelogenin‑Gen (Amelx bei Mäusen) kann auf verschiedene Weise gespleißt werden, wodurch mehrere Proteinvarianten entstehen, die in unterschiedlichen Stadien der Zahnentwicklung benötigt werden. Ein kurzes Segment, Exon 4 genannt, wird üblicherweise aus der endgültigen proteinkodierenden Nachricht entfernt. Frühere Arbeiten dieser Gruppe zeigten, dass das verworfene Exon 4 kein Abfallprodukt ist: Es wird zu einer MicroRNA, miR‑exon4, verarbeitet, die andere für Knochen und Schmelz wichtige Gene regulieren kann. Die neue Studie untersucht, was in lebenden Tieren passiert, wenn diese MicroRNA reduziert oder blockiert wird und ob sie außerdem rückkoppelt, um zu steuern, wie Amelogenin selbst zusammengesetzt wird.
Eine Regulationskette in Zahn bildenden Zellen
Die Forscher bestätigten zunächst in Mauszähnen, dass miR‑exon4 an einer Regulationskette beteiligt ist, die sie zuvor in im Labor gezüchteten Zellen kartiert hatten. In normalen Schmelzorganen hält miR‑exon4 zwei vorgelagerte Gene, Nfia und Prkch, in Schach. Werden diese niedrig gehalten, steigen die Werte eines wichtigen Transkriptionsfaktors, RUNX2. Anhand von Mäusen, denen entweder das Amelogenin‑Gen fehlte, die zusätzlich miR‑exon4 erhielten, oder mit einem miR‑exon4‑Blocker behandelt wurden, zeigte das Team, dass die Verminderung von miR‑exon4 Nfia und Prkch erhöht und RUNX2 verringert, während das Zufügen von miR‑exon4 den gegenteiligen Effekt hat. Dies bestätigt, dass der miR‑exon4–Nfia/Prkch–RUNX2‑Pfad in vivo in sich entwickelnden Zähnen wirkt.
Von gestörten Signalen zu schwächerem Schmelz
Um zu sehen, wie sich diese molekularen Veränderungen auf den tatsächlichen Schmelz auswirken, hemmten die Wissenschaftler miR‑exon4 bei neugeborenen Mäusen für eine Woche während der aktiven Zahnformation. Dreidimensionale Röntgenaufnahmen zeigten, dass die behandelten Tiere einen deutlichen Rückgang hoch mineralisierten Schmelzes sowohl an Schneidezähnen als auch an Backenzähnen aufwiesen. Heatmaps und gefärbte Schnitte zeigten, dass der Beginn der Mineralablagerung entlang der Schmelzschicht verzögert war und die frühe Mineralisierungsphase verkürzt wurde, was zu raueren Oberflächen und unscharfen Grenzen zwischen Schmelz und darunter liegenden Geweben führte. Gleichzeitig fielen die RUNX2‑Proteinspiegel in Ameloblasten, während Amelogenin‑Protein — einschließlich Varianten, die Exon 4 enthalten — zunahm. Dieses Muster spiegelt frühere Modelle wider, in denen eine Überproduktion einer langen Amelogenin‑Form mit Exon 4 zu Schmelzdefekten führt, und legt nahe, dass ein Übermaß dieser Isoform, ausgelöst durch den Verlust von miR‑exon4, die normale Mineralisierung direkt stören kann.
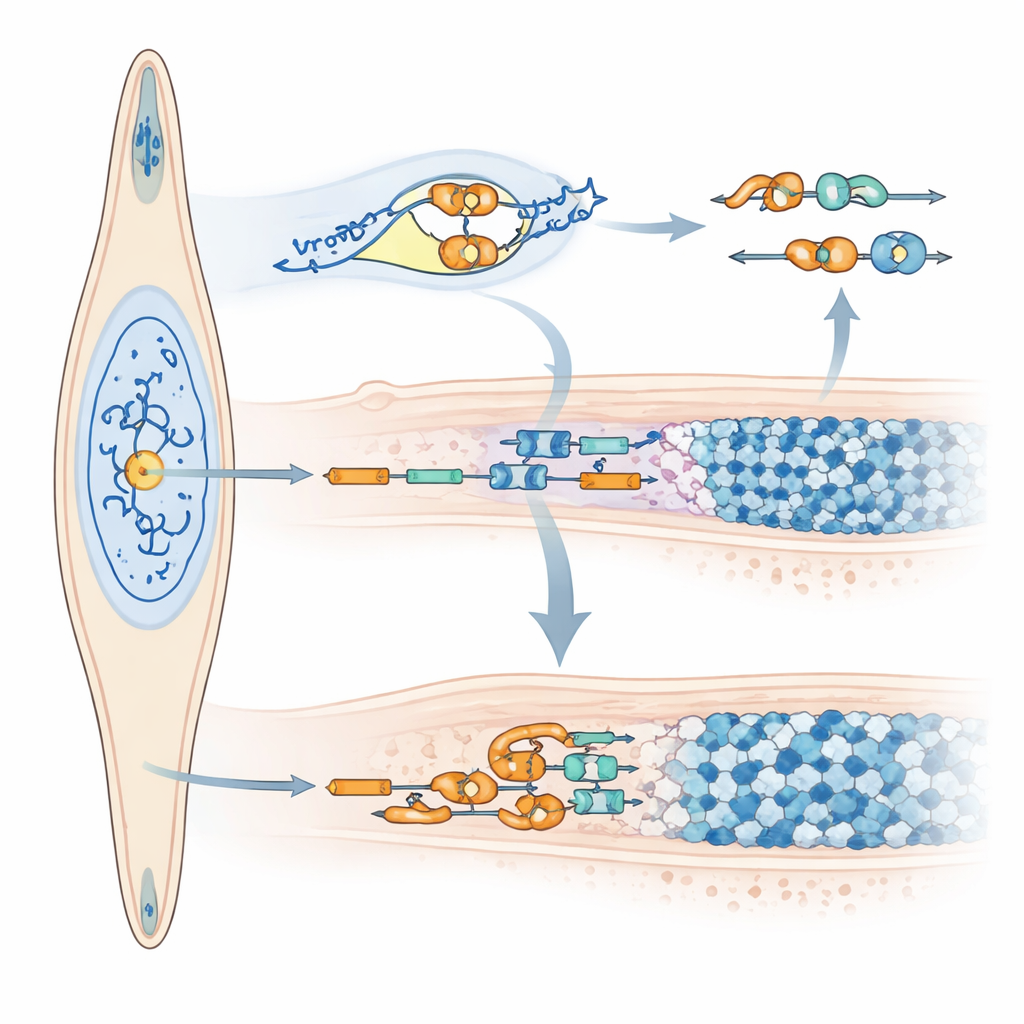
Wie die MicroRNA die Schmelz‑Botschaft umformt
Über die Veränderung der Amelogenin‑Menge hinaus beeinflusst miR‑exon4 auch, wie die Amelogenin‑Nachricht geschnitten und gespleißt wird. Kurzfristiges Blockieren von miR‑exon4 verringerte RNA‑Moleküle, die noch Exon 4 enthielten, ohne die Gesamtmenge an Amelogenin zu verändern, was darauf hindeutet, dass Exon 4 häufiger herausgeschnitten wurde. Das Team brachte diese Verschiebung mit Veränderungen in mehreren Spleißregulatorgenen (SRSFs) in Verbindung, von denen einige bei reduzierten miR‑exon4‑Werten anstiegen und andere sanken. In Zellmodellen, die eine speziell konstruierte Version des Amelogenin‑Gens tragen und weniger miR‑exon4 produzieren, wurde Exon 4 ebenfalls häufiger übersprungen. Entscheidend wurde die MicroRNA selbst im Zellkern gefunden, wo das Spleißen stattfindet, und biochemische Tests zeigten, dass sie am Amelogenin‑VorläuferRNA an einem spezifischen Kontrollpunkt im benachbarten Intron assoziiert. Diese Befunde stützen eine doppelte Rolle von miR‑exon4: indirekt die Exonauswahl durch Anpassung der Spleißfaktoren zu beeinflussen und direkt in der Nähe von Exon 4 zu binden, um zu steuern, ob es beibehalten oder entfernt wird.
Was das für die Schmelzgesundheit bedeutet
Insgesamt zeichnet die Studie miR‑exon4 als kleine, aber zentrale Koordinatorin der Schmelzbildung. Wenn sie in der richtigen Menge vorhanden ist, unterstützt sie die angemessene RUNX2‑Aktivität, hält die Amelogeninproduktion im Gleichgewicht und sorgt dafür, dass Exon 4 in den richtigen Stadien eingeschlossen oder ausgeschlossen wird. Ist miR‑exon4 fehlend oder vermindert, verschiebt sich dieses Gleichgewicht: Signalwege werden gestört, Exon 4 wird falsch gehandhabt, Amelogenin‑Isoformen werden verfälscht und die frühe Schmelzmineralisierung wird geschwächt. Diese Einsichten helfen zu erklären, wie bestimmte Mutationen im Amelogenin‑Gen vererbte Schmelzstörungen verursachen können, und heben nukleäre MicroRNAs als wichtige Akteure bei der Gestaltung des härtesten Gewebes im Körper hervor.
Zitation: Shemirani, R., Duong, T., Kim, R. et al. A splicing-derived microRNA from amelogenin exon4 regulates enamel formation via control of exon4 splicing and amelogenin expression. Sci Rep 16, 11044 (2026). https://doi.org/10.1038/s41598-026-40706-0
Schlüsselwörter: Zahnschmelz, Amelogenin, microRNA, RNA-Spleißen, Amelogenesis imperfecta