Clear Sky Science · de
ABE9 mit SpRY-Cas9-Nickase verbunden ermöglicht präzise Erstellung von nebenwirkungsfreien Mausmodellen
Scharfere Werkzeuge zum Aufbau besserer Krankheitsmodelle
Viele schwere Erkrankungen werden durch einzelne Buchstabenfehler in unserer DNA verursacht. Um diese Zustände zu verstehen und schließlich zu behandeln, erzeugen Wissenschaftler häufig Mäuse, die dieselben Mutationen wie menschliche Patienten tragen. Das präzise Umschreiben von DNA ist jedoch überraschend schwierig: Ältere Methoden können das Genom verletzen, zusätzliche Mutationen einführen und experimentelle Ergebnisse verschleiern. Diese Studie stellt ein verfeinertes Geneditier-Werkzeug vor, genannt ABE9-SpRY, das dazu entwickelt wurde, genau einen DNA-Buchstaben zu verändern, während benachbarte Buchstaben – und der Rest des Genoms – weitgehend unberührt bleiben.
Von groben Schnitten zu sanften DNA-Korrekturen
Traditionelle CRISPR-Cas9-Editing funktioniert wie eine molekulare Schere, die beide Stränge der DNA durchschneidet. Zellen reparieren diese Brüche unvollkommen und hinterlassen oft kleine Einfügungen oder Deletionen, die Gene auf unvorhersehbare Weise stören. Das ist nützlich, um Gene auszuschalten, aber nicht, um eine präzise krankheitsverursachende Mutation nachzubilden. Baseneditoren schneiden die DNA dagegen nicht. Stattdessen veranlassen sie chemisch, dass ein DNA-Buchstabe in einen anderen umgewandelt wird – hier A zu G – während die Doppelhelix intakt bleibt. Dieser Ansatz reduziert großflächige Deletionen und Umlagerungen erheblich, aber frühere Adenin-Baseneditoren litten dennoch an drei Hauptproblemen: Sie bearbeiteten manchmal benachbarte „Bystander“-Buchstaben, sie konnten nur Stellen neben spezifischen kurzen Sequenzmarkern erreichen und sie verursachten gelegentlich Änderungen an unbeabsichtigten Orten im Genom.
Entwicklung eines selektiveren molekularen Stifts
Die Forschenden hatten sich vorgenommen, alle drei Einschränkungen gleichzeitig anzugehen. Sie begannen mit ABE9, einer neueren Variante des Baseneditors, die ihre Aktivität auf einen sehr schmalen DNA-Abschnitt konzentriert und das „Editierfenster“ so weit verkleinert, dass deutlich weniger benachbarte Buchstaben versehentlich verändert werden. Anschließend fusionierten sie ABE9 mit einem konstruierten Cas9-Nickase namens SpRY. Im Unterschied zu Standard-Cas9, das einen strikten „NGG“-Marker neben der Zielstelle benötigt, kann SpRY eine deutlich breitere Palette von DNA-Sequenzen erkennen. Dadurch lassen sich krankheitsrelevante Positionen im Genom erreichen, die zuvor unzugänglich waren. Das resultierende Fusionswerkzeug ABE9-SpRY soll sowohl sehr präzise als auch wesentlich flexibler bei den erreichbaren Zielstellen sein.
Test des neuen Editors in Zellen und Embryonen
Um zu prüfen, ob ABE9-SpRY seinen Ansprüchen gerecht wird, verglich das Team ihn mit einem weit verbreiteten, aggressiveren Editor namens ABE8e-SpRY. Sie zielten auf vier krankheitsrelevante Positionen in Genen, die Ionenkanäle kodieren (TPC1, TPC2 und TRPM4), welche wichtige Rollen in Herz- und Leberfunktion spielen. In im Labor gezüchteten Maus-Nervenzellen bearbeitete ABE8e-SpRY den Zielbuchstaben effizienter, veränderte aber auch viele benachbarte Basen. ABE9-SpRY hingegen erzeugte insgesamt weniger Editierungen, lieferte jedoch einen deutlich höheren Anteil an „sauberen“ Ergebnissen – Sequenzen, in denen nur der beabsichtigte Buchstabe verändert wurde, ohne zusätzliche Mutationen in der lokalen Region. Dasselbe Muster zeigte sich in Maus-Embryonen. Als die Forschenden Editierkomponenten in befruchtete Eier injizierten, konvertierte ABE8e-SpRY oft nahezu alle Kopien des Zielgens, jedoch mit zahlreichen Bystander-Änderungen. ABE9-SpRY editierte insgesamt weniger Kopien, aber dort, wo es wirkte, war die DNA-Sequenz typischerweise exakt wie geplant korrigiert.
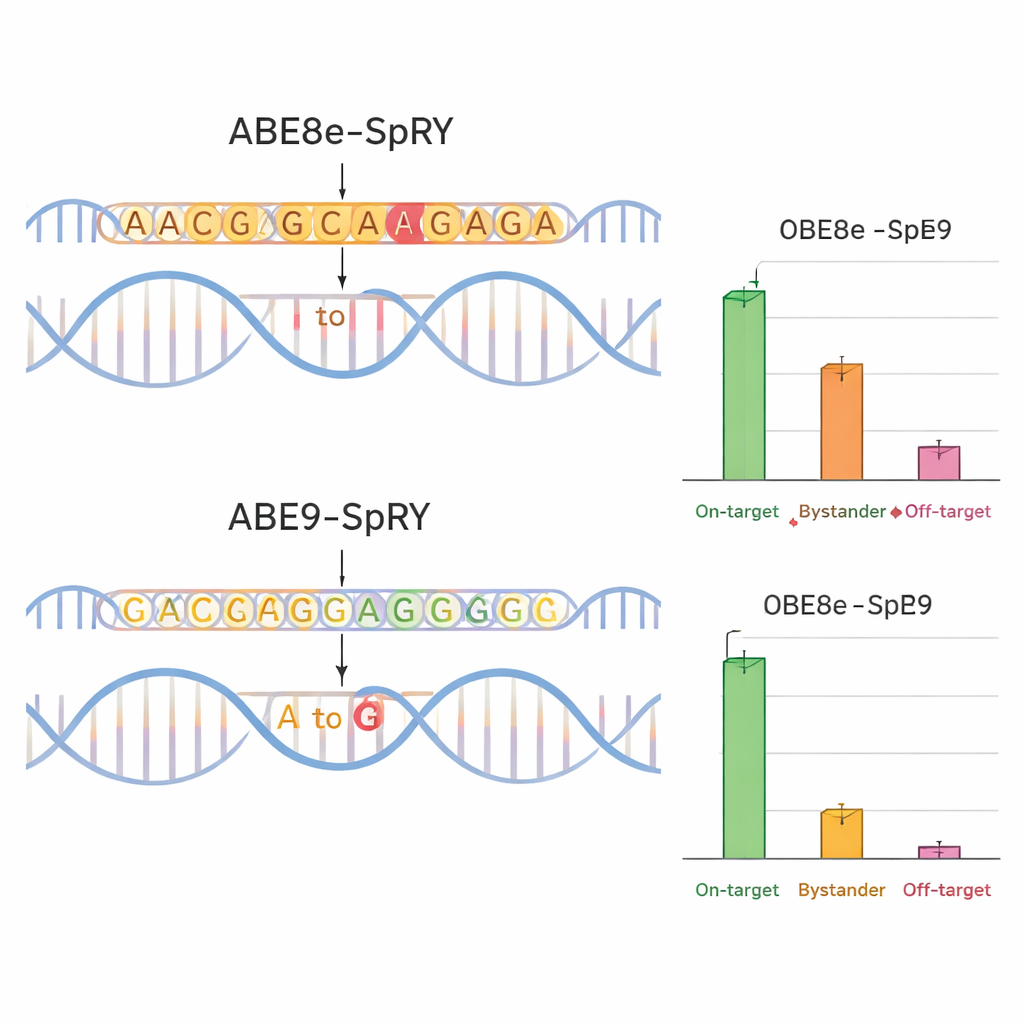
Sauberere Editierungen, weniger Nebenwirkungen
Präzision betrifft nicht nur die lokale DNA-Umgebung. Das Team untersuchte auch, ob ihr Editor entfernte Regionen des Genoms veränderte. Mit computergestützten Vorhersagen und gezieltem Sequenzieren maßen sie Off‑Target-Veränderungen an wahrscheinlich ähnlichen Stellen in Maus-Embryonen. ABE8e-SpRY führte häufig unbeabsichtigte A-zu-G-Änderungen an diesen Positionen ein, mitunter auf überraschend hohem Niveau. ABE9-SpRY zeigte deutlich weniger solche Ereignisse, mit nur seltenen Off‑Target-Editierungen und keiner nachweisbaren Aktivität in einem speziellen Test für Cas9-unabhängige DNA-Schädigung. Wichtig ist ferner, dass ABE9-SpRY, wenn es allein – nicht in gepoolten Tests – verwendet wurde, um zwei spezifische Mutationen in Mäusen einzuführen, viele Gründer-Tiere erzeugte, in denen die gewünschte Editierung in hoher Frequenz vorhanden war und zuverlässig an die Nachkommen weitergegeben wurde, wiederum mit minimalen Bystander-Änderungen oder kleinen Einfügungen und Deletionen.
Präzisions-Editing in menschlichen Stammzellen
Da patientenspezifische Stammzellen zunehmend genutzt werden, um Krankheiten zu untersuchen und Medikamente zu testen, probierten die Forschenden ABE9-SpRY auch in humanen induzierten pluripotenten Stammzellen aus. Sie zielten auf die menschliche Version des TPC1-Gens an einer Position, die einer der Mausstellen entspricht. Mit einem fluoreszenten Reporter zur Anreicherung editierter Zellen fanden sie, dass ABE8e-SpRY höhere rohe Editierraten erzielte, jedoch erneut mehrere benachbarte Basen veränderte. ABE9-SpRY editierte insgesamt weniger Allele, aber der Anteil perfekt editierter Abschnitte – eine beabsichtigte Änderung und sonst nichts – war deutlich höher, mit weniger störenden Einfügungen oder Deletionen. In der Arbeit mit Stammzellen, wo einzelne Klone für detaillierte Studien expandiert werden, ist eine solche „saubere“ Editierung in der Regel wertvoller als rohe Effizienz.
Warum das für die zukünftige Krankheitsforschung wichtig ist
Für Wissenschaftler, die verstehen wollen, wie eine einzelne DNA-Buchstabenänderung zu Krankheit führt, können zusätzliche unbeabsichtigte Mutationen tief irreführend sein. Diese Studie zeigt, dass ABE9-SpRY, obwohl es in Bezug auf rohe Editiergeschwindigkeit etwas weniger leistungsstark ist, Einzelbuchstabenänderungen in die Genome von Mäusen und menschlichen Stammzellen mit bemerkenswerter Genauigkeit und großer Zielflexibilität einfügen kann. Das macht es zu einem vielversprechenden Arbeitstier zum Aufbau getreuer Tier- und Zellmodelle menschlicher genetischer Störungen, insbesondere in Situationen, in denen schon eine einzelne Fremdmutation die Biologie verfälschen oder eine potenzielle Therapie entgleisen könnte.
Zitation: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
Schlüsselwörter: Adenin-Baseneditierung, CRISPR-Krankheitsmodelle, Mausgenetik, Nebenwirkungs-Effekte, Genbearbeitung von hiPSC