Clear Sky Science · de
Bei Pankreatitis assoziierte Chymotrypsin C (CTRC)-Variante p.R240Q beeinträchtigt selektiv den Abbau von Trypsinogen durch Störung langreichweitiger elektrostatischer Wechselwirkungen
Warum das für die Pankreasgesundheit wichtig ist
Chronische Pankreatitis ist eine schmerzhafte, lang andauernde Entzündung der Bauchspeicheldrüse, die zu Diabetes, Verdauungsproblemen und einer starken Einbuße der Lebensqualität führen kann. Diese Studie untersucht, warum manche Menschen anfälliger sind, weil sie kleine vererbte Veränderungen in ihren Verdauungsenzymen tragen. Indem die Forscher eine einzelne genetische Variante in einem schützenden Enzym genau betrachten, zeigen sie, wie eine subtile molekulare Änderung das Gleichgewicht von Schutz hin zu Selbstschädigung innerhalb der Bauchspeicheldrüse verschieben kann.
Ein eingebautes Sicherheitssystem der Verdauung
Unsere Bauchspeicheldrüse produziert potente proteolytische Enzyme, die normalerweise in einer inaktiven Form in den Darm freigesetzt werden. Einer dieser Vorläufer, das Trypsinogen, kann sich manchmal zu früh aktivieren, bereits innerhalb der Bauchspeicheldrüse. Wenn das geschieht, beginnt es, das Organ von innen heraus zu verdauen und eine Entzündung auszulösen. Zur Kontrolle nutzt der Körper Schutzmechanismen, darunter ein Inhibitorprotein (SPINK1) und ein weiteres Verdauungsenzym, Chymotrypsin C (CTRC). CTRC hat eine doppelte Aufgabe: Es unterstützt die Aktivierung von Verdauungsenzymen dort und dann, wo sie benötigt werden, und es baut überschüssiges Trypsinogen ab, bevor dieses zu aktivem Trypsin wird und Schaden anrichtet. Menschen, die abgeschwächte Formen von CTRC vererbt haben, tragen ein erhöhtes Risiko für chronische Pankreatitis.
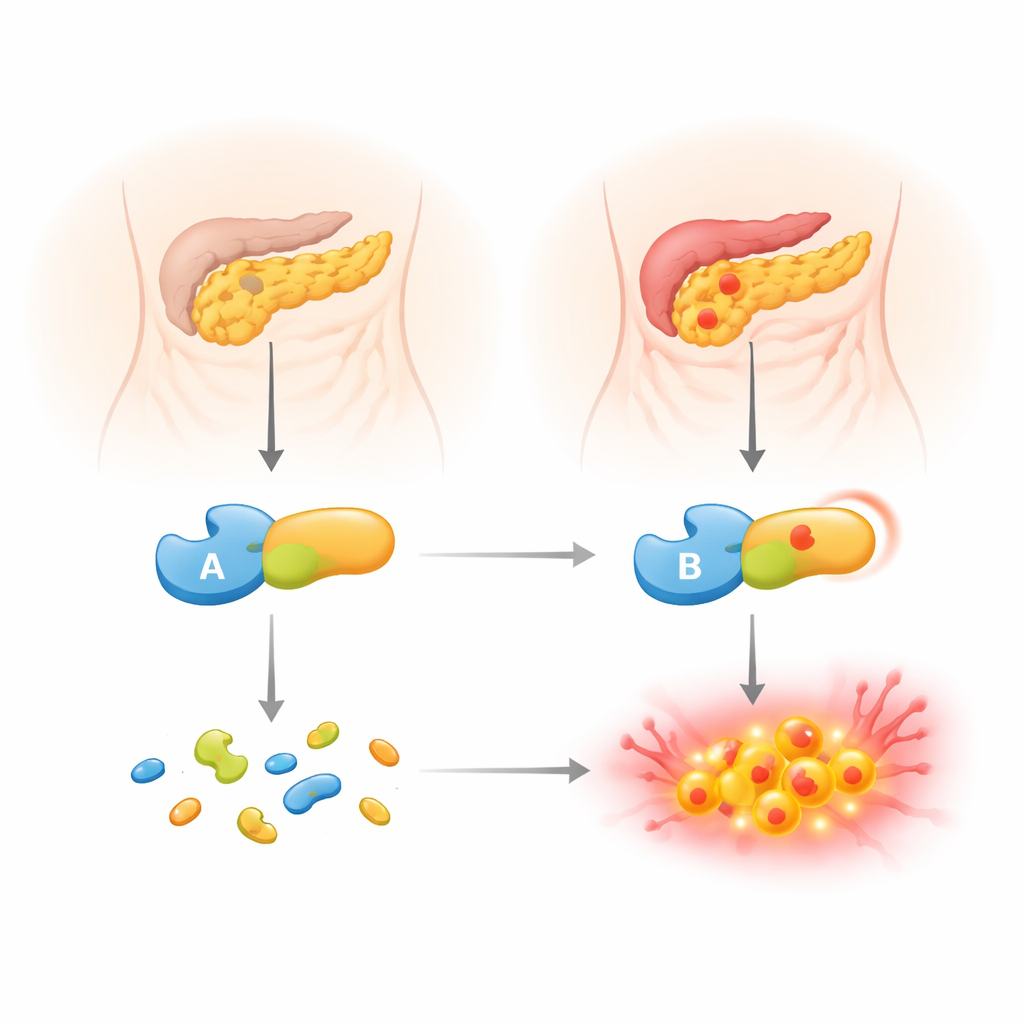
Eine seltene genetische Veränderung unter dem Mikroskop
Das Team konzentrierte sich auf eine ungewöhnliche CTRC-Variante namens p.R240Q, die bei einem Jungen aus der Slowakei mit frühkindlich beginnender chronischer Pankreatitis und bei seinem betroffenen Vater gefunden wurde. Diese Variante verändert einen einzigen Baustein an der Enzymoberfläche, indem eine positiv geladene Einheit durch eine neutrale ersetzt wird. Große genetische Datenbanken stufen sie als wahrscheinlich harmlos ein, dennoch ist sie bei mehreren jungen Patienten mit der Erkrankung aufgetreten. Um herauszufinden, was sie tatsächlich bewirkt, kombinierten die Autoren familiäre genetische Daten mit detaillierten Laborversuchen. Sie verglichen das Variantenenzym direkt mit normalem CTRC und untersuchten, wie gut es von Zellen produziert wird, wie aktiv es an standardisierten Testsubstanzen ist und wie es mit dem Trypsinogen interagiert, der Schlüsselsubstanz, die es kontrollieren soll.
Normale Kraft, aber fehlgeleitete Zielrichtung
Zunächst zeigten die Forscher, dass Zellen das p.R240Q-Enzym genauso gut herstellen und sekretieren wie die normale Version; die Variante führt demnach nicht zu Fehlfaltung oder Produktionsausfall. In Reagenzglas-Tests mit einem kleinen synthetischen Peptid und einem Milchprotein (Beta-Casein) arbeitete die Variante ebenso gut oder sogar leicht besser als normales CTRC. Das bedeutet, ihre Spaltkraft ist intakt. Die Überraschung kam bei der einen Reaktion, die für die Pankreatitis am wichtigsten ist: dem Abbau des menschlichen kationischen Trypsinogens. Hier war das Variantenenzym deutlich weniger effektiv — etwa vier- bis fünfmal langsamer beim Zerschneiden von Trypsinogen und deutlich schlechter darin, die Autoaktivierung von Trypsinogen zu aktivem Trypsin zu verhindern. In Autoaktivierungsexperimenten war deutlich mehr Varianten-CTRC nötig, um die Trypsinspiegel im Zaum zu halten als beim normalen Enzym.
Ein gestörter elektrostatischer „Traktorstrahl“
Um zu verstehen, warum das passiert, griffen die Autoren auf Strukturmodelle von CTRC zurück. Rund um die Rinne, in der CTRC seine Substrate greift, befindet sich ein Ring positiver elektrischer Ladung, gebildet von mehreren geladenen Aminosäuren, einschließlich der durch p.R240Q veränderten Stelle. Regionen des Trypsinogens, die CTRC schneiden muss, sind stark negativ geladen, sodass dieser positiv geladene Ring wie ein langreichweitiger „Traktorstrahl“ wirkt, der das Trypsinogen in die richtige Position zieht. Durch die Neutralisierung einer dieser positiven Stellen schwächt die p.R240Q-Variante diese entfernte Anziehungskraft. Das Enzym ist weiterhin scharf, aber das beschädigte Führungssystem bewirkt, dass Trypsinogen nicht mehr so effizient bindet und daher weniger davon sicher abgebaut wird. Andere Substrate, die nicht so stark von diesem Ladungsmuster abhängen, werden normal verarbeitet, was den hochselektiven Defekt erklärt, der in den Experimenten beobachtet wurde.
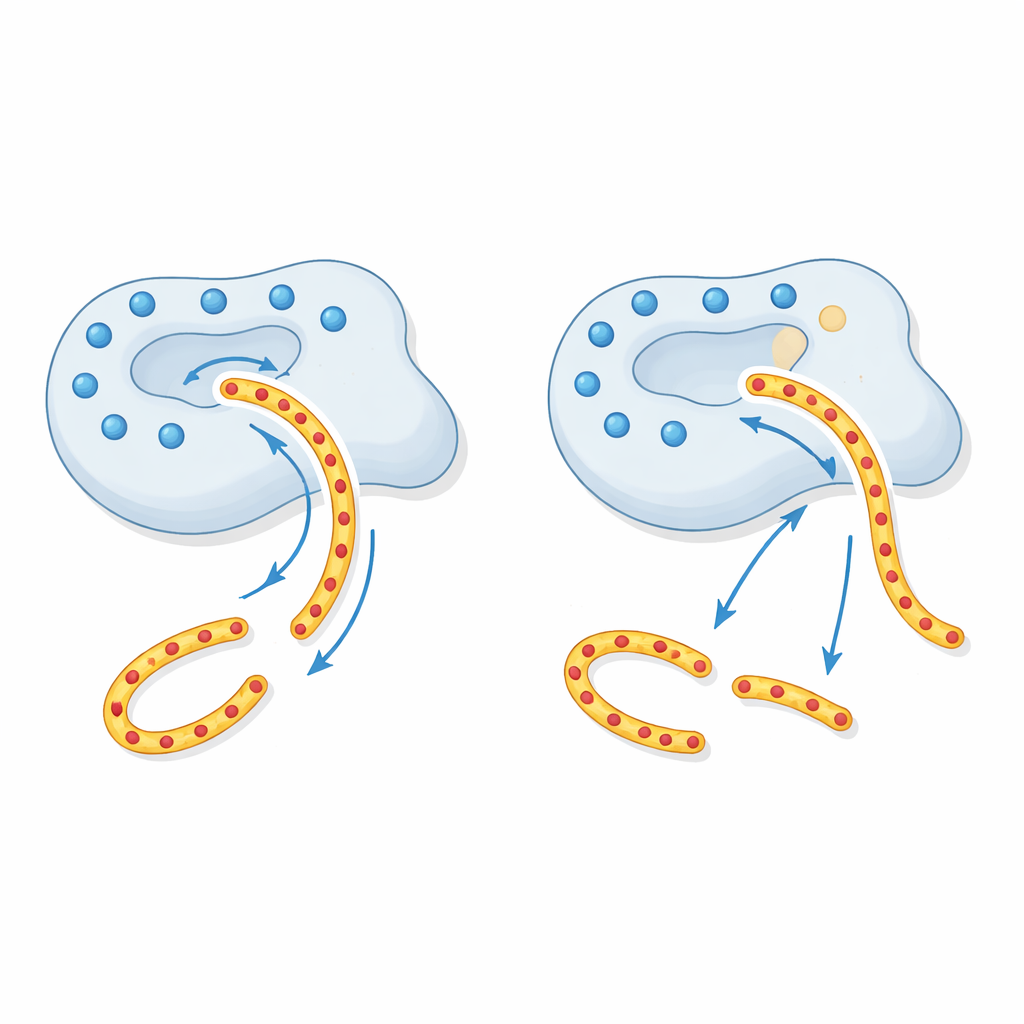
Was das für Patienten und Tests bedeutet
Klinisch trugen der betroffene Junge und sein Vater außerdem eine zweite schädliche CTRC-Variante, und der Vater wies zusätzliche Lebensstilrisiken wie starken Alkoholkonsum auf. Das passt zur Vorstellung, dass chronische Pankreatitis oft aus mehreren additiven genetischen und umweltbedingten Treffern entsteht. Die Arbeit zeigt, dass eine Variante, die in gängigen Vorhersagewerkzeugen harmlos erscheint, dennoch auf sehr spezifische Weise gefährlich sein kann. Für die genetische Diagnostik lautet die Botschaft klar: Wenn beurteilt werden soll, ob eine CTRC-Variante das Pankreatitisrisiko erhöht, müssen Wissenschaftler sie am realen Ziel Trypsinogen testen und nicht nur an generischen Labor-Substraten. Alltagsgerecht zeigt diese Studie, wie eine winzige Änderung an der „Führungsfläche“ des Enzyms eine der wichtigsten Sicherheitsverriegelungen der Bauchspeicheldrüse still und heimlich untergraben kann, wodurch anfällige Personen in Richtung chronischer Entzündung gedrängt werden.
Zitation: Nagy, Z.A., Sándor, M., Hegyi, E. et al. Pancreatitis-associated chymotrypsin C (CTRC) variant p.R240Q selectively impairs trypsinogen degradation through disruption of long-range electrostatic interactions. Sci Rep 16, 8937 (2026). https://doi.org/10.1038/s41598-026-40633-0
Schlüsselwörter: chronische Pankreatitis, Chymotrypsin C, Trypsinogen, genetische Variante, Verdauungsenzyme