Clear Sky Science · de
Niedrigaffine Bindung des Anti-B7-H3-Klons MJ18 an murines B7-H3 führt nicht zur Tumorrückbildung
Warum das für die Krebsforschung wichtig ist
Krebsimmuntherapie beruht häufig auf Antikörpern — laborgefertigten Proteinen, die an Tumorzellen binden und dem Immunsystem helfen, sie zu zerstören. Ein vielversprechendes Ziel ist das Molekül B7-H3, das in vielen menschlichen Tumoren reichlich vorkommt, in gesunden Geweben dagegen selten ist. Diese Arbeit nimmt einen weit verbreiteten Forschungsantikörper, MJ18, kritisch unter die Lupe, der in Mausstudien B7-H3 blockieren sollte. Die Autoren zeigen, dass MJ18 kaum an sein Ziel bindet und das Tumorwachstum nicht hemmt, was Zweifel daran weckt, wie frühere Tierversuche mit diesem Werkzeug zu interpretieren sind.
Das Versprechen einer Krebsmarkierung auf Tumorzellen
B7-H3 zieht großes Interesse auf sich, weil es wie ein molekularer Schild wirkt: Tumoren mit hoher B7-H3-Expression zeigen tendenziell weniger aggressive Immunzellen im Inneren und werden mit schlechteren Patientenergebnissen in Verbindung gebracht. In mehreren Mausmodellen führt das Entfernen des B7-H3-Gens in Tumorzellen zu einer stärkeren Immunantwort und kann dazu führen, dass Tumoren schrumpfen oder verschwinden. Diese Beobachtungen haben die Entwicklung von Medikamenten, gentechnisch veränderten Immunzellen und Antikörper-Wirkstoff-Konjugaten beflügelt, die gezielt B7-H3 auf menschlichen Tumoren anvisieren. Allerdings bleibt die genaue Art, wie B7-H3 die Immunantwort dämpft — und selbst welcher Rezeptor auf Immunzellen daran beteiligt ist — unsicher, zumal die Maus- und Humanversionen von B7-H3 strukturell voneinander abweichen.
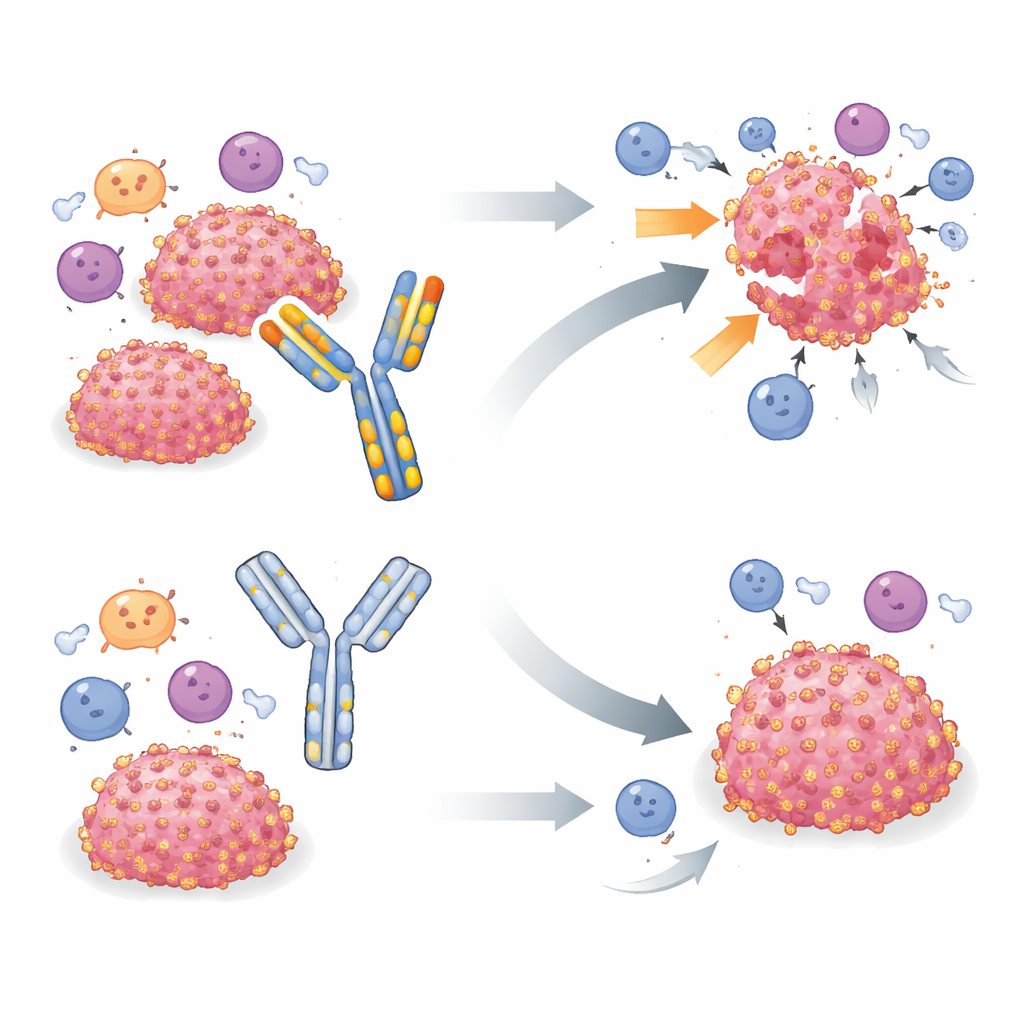
Ein vielgenutztes Werkzeug unter dem Mikroskop
Um B7-H3 in lebenden Mäusen zu untersuchen, haben viele Gruppen auf einen einzelnen rattenabgeleiteten Antikörper namens MJ18 gesetzt, dem nachgesagt wurde, Maus-B7-H3 zu erkennen und seine immunsuppressive Wirkung zu blockieren. Frühere Studien mit MJ18 in verschiedenen Krankheitsmodellen, darunter Krebs, berichteten häufig von verlangsamtem Tumorwachstum und verbessertem Überleben. Das aktuelle Team testete MJ18 zunächst in einem Mausmodell des Rhabdomyosarkoms, einem kindlichen Weichteiltumor, bei dem B7-H3 bereits als wichtiger Fluchtmechanismus identifiziert worden war. Als MJ18 die Tumorkontrolle nicht verbesserte, erweiterten die Forscher ihre Tests auf zwei weitere B7-H3-positive Tumortypen — Pankreas- und Mammakarzinome — die eindeutig auf eine Deletion von B7-H3 ansprechbar sind. In allen drei Modellen verzögerte oder eliminierte das Ausschalten von B7-H3 in Tumorzellen die Tumoren deutlich, während die Behandlung der Mäuse mit MJ18 in Dosen und Zeitplänen, die in der Literatur verwendet werden, keinen messbaren Einfluss auf Tumorwachstum oder Überleben zeigte.
Prüfung, ob MJ18 sein Ziel wirklich trifft
Die Autoren stellten dann eine grundlegende Frage, die überraschenderweise nie rigoros beantwortet worden war: Bindet MJ18 wirklich an murines B7-H3, und wie stark? Mit Durchflusszytometrie verglichen sie MJ18 mit einem anderen Antikörper, EPNCIR122, der bekannt war, B7-H3 zu detektieren. An mehreren Maus-Tumorzelllinien erzeugte EPNCIR122 ein deutliches Signal, das verschwand, wenn das B7-H3-Gen ausgeschaltet wurde, was seine Spezifität bestätigte. MJ18 hingegen zeigte selbst bei hohen Konzentrationen keine überzeugende Bindung. Bei der Untersuchung von Immunzellen aus der Milz band MJ18 zwar, aber das Muster stimmte nicht mit B7-H3 überein, und EPNCIR122 detektierte auf diesen Zellen überhaupt kein B7-H3, was darauf hindeutet, dass MJ18 an etwas anderes haftete.
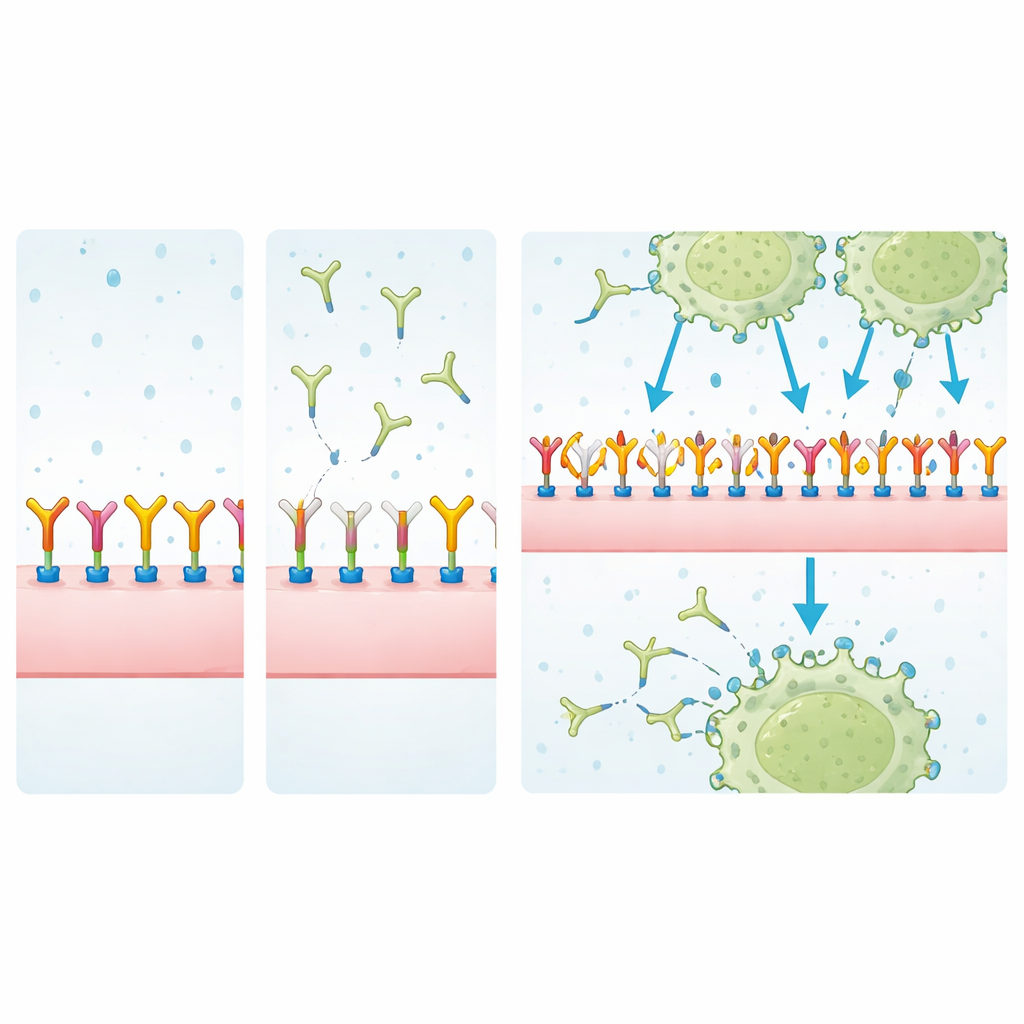
Untersuchung der Bindungspartner
Um herauszufinden, was MJ18 tatsächlich erkennen könnte, zogen die Forscher membranständige Proteine mit MJ18 oder EPNCIR122 heraus und analysierten sie mittels Massenspektrometrie, wobei sie häufige Hintergrundkontaminanten herausfilterten. In Tumorzellen reicherte EPNCIR122 B7-H3 deutlich über anderen Proteinen an und bestätigte damit seine hohe Spezifität. MJ18 hingegen zog ein Gemisch von Proteinen an, in dem B7-H3 nur schwach und auf ähnlichem Niveau wie unspezifische Binder erschien. Messungen mittels Oberflächenplasmonresonanz, einer empfindlichen Technik zur Quantifizierung molekularer Wechselwirkungen, unterstrichen den Befund: Die Affinität von MJ18 für murines B7-H3 war etwa 7.000-mal schwächer als die von EPNCIR122 — weit unter dem, was typisch für therapeutische Antikörper ist.
Wenn Antikörper von den falschen Zellen ergriffen werden
Die Geschichte endete nicht bei schwacher Bindung. In Milzzellen zeigten zusätzliche Tests, dass MJ18 und ähnliche Rattenantikörper von murinen Fc-Rezeptoren erkannt wurden — Molekülen auf Immunzellen, die natürlicherweise das Antikörper-Fc-Ende binden. Das Blockieren dieser Rezeptoren reduzierte das MJ18-Signal stark, was nahelegt, dass ein Großteil der scheinbaren Bindung darauf zurückging, dass Immunzellen den Antikörper selbst griffen, statt dass MJ18 ein spezifisches Oberflächenprotein anvisierte. Versuche, einen einzigartigen Proteinpartner für MJ18 auf Immunzellen zu identifizieren, förderten nur Kandidaten zutage, deren Vorkommen nicht von Hintergrundrauschen zu unterscheiden war. Insgesamt deuten die Daten darauf hin, dass MJ18 weitgehend als niedrigaffiner, unspezifischer Antikörper agiert, dessen Interaktionen von Fc-Rezeptorbindung dominiert werden statt von präziser Erkennung von B7-H3.
Was das für die Zukunft bedeutet
Für Nicht-Expertinnen und -Experten lautet die Quintessenz einfach: Während B7-H3 weiterhin ein überzeugendes Ziel bei vielen Krebsarten bleibt, ist der Antikörper MJ18 kein verlässlicher Pfeil. Er bindet B7-H3 bei Mäusen nur schwach und reproduziert nicht die starke Tumorkontrolle, die beim Entfernen des B7-H3-Gens beobachtet wird. Frühere Mausstudien, die dramatische Vorteile durch MJ18 berichteten, könnten daher andere Effekte widerspiegeln — etwa wie das Antikörper-Fc-Ende mit Rezeptoren auf Immunzellen interagiert — statt eine echte Blockade von B7-H3. Die Autoren plädieren dafür, dass das Feld dringend gut validierte, hochaffine Antikörper gegen murines B7-H3 benötigt und dass Forschende routinemäßig Spezifität und Bindungsstärke solcher Werkzeuge überprüfen. Nur mit verlässlichen Reagenzien können Erkenntnisse aus Tiermodellen vertrauenswürdig die Entwicklung nächster Generationen von B7-H3‑gerichteten Therapien für Patientinnen und Patienten leiten.
Zitation: Gulyás, D., Nammor, T., Frizzell, J. et al. Low-affinity binding of anti-B7-H3 clone MJ18 to murine B7-H3 fails to induce tumor regression. Sci Rep 16, 9519 (2026). https://doi.org/10.1038/s41598-026-40628-x
Schlüsselwörter: B7-H3, Krebsimmuntherapie, Antikörpervalidierung, Immun-Checkpoints, Tumormodelle