Clear Sky Science · de
Strukturelle Stabilität symmetrischer bispezifischer Antikörper: eine Fallstudie, die potenzielle Schwachstellen nahe Linker-Regionen aufzeigt
Warum winzige Verbindungsstücke in neuen Krebstherapien wichtig sind
Viele der derzeit spannendsten Krebstherapien sind Antikörper, die so konstruiert wurden, dass sie gleichzeitig zwei verschiedene Ziele binden und damit Immunzellen helfen, Tumore zu finden. Diese „bispezifischen“ Antikörper können leistungsfähiger sein als ältere Wirkstoffe mit nur einem Ziel, sind jedoch auch komplexere Moleküle. Diese Studie betrachtet einen solchen experimentellen Wirkstoff im Detail und stellt eine einfache, aber entscheidende Frage: Bleiben die winzigen Proteinverbindungsstücke, die seine Komponenten zusammenhalten, unter realen Herstellungs- und Lagerbedingungen intakt, oder werden sie zur Schwachstelle?
Aufbau eines zweitarmigen Antikörpers
Die Forscher konzentrierten sich auf einen symmetrischen bispezifischen Antikörper, der auf einen Tumormarker namens HER2 und einen Rezeptor auf Immunzellen namens CD3 abzielt. Symmetrisch bedeutet hier, dass das Molekül ausgeglichen und spiegelbildlich aufgebaut ist und vier Bindungsenden statt der üblichen zwei besitzt. Um dies zu erreichen, verband das Team bekannte Antikörperbausteine mit kurzen Abschnitten flexiblen Proteins, sogenannten Linkern. Diese Linker fungieren wie Scharniere oder Abstandshalter und ermöglichen es den Bindungsregionen, die richtigen Positionen einzunehmen, sodass das Medikament gleichzeitig die Krebszelle und die T‑Zelle greifen kann.
Die Schwachstellen bei Hitze und extremen Bedingungen
Um die Robustheit dieses Designs zu prüfen, setzten die Forscher den Antikörper gezielt Stress aus. Sie erhitzten ihn über Wochen und lagerten ihn in Lösungen mit unterschiedlicher Säure (pH) und Salzgehalt, um Bedingungen nachzuahmen, denen das Molekül während Reinigung, Formulierung oder Langzeitlagerung ausgesetzt sein könnte. Mithilfe einer Technik, die Moleküle nach Größe trennt, beobachteten sie, wie der Anteil intakter Antikörper allmählich abnahm und die Menge kleinerer Fragmente zunahm, besonders bei erhöhtem pH. Salz allein hatte nur einen bescheidenen Effekt, aber in Kombination von hohem pH und hohem Salz stieg die Fragmentierung stark an, was darauf hindeutet, dass bestimmte Bereiche des Moleküls auseinanderfielen.
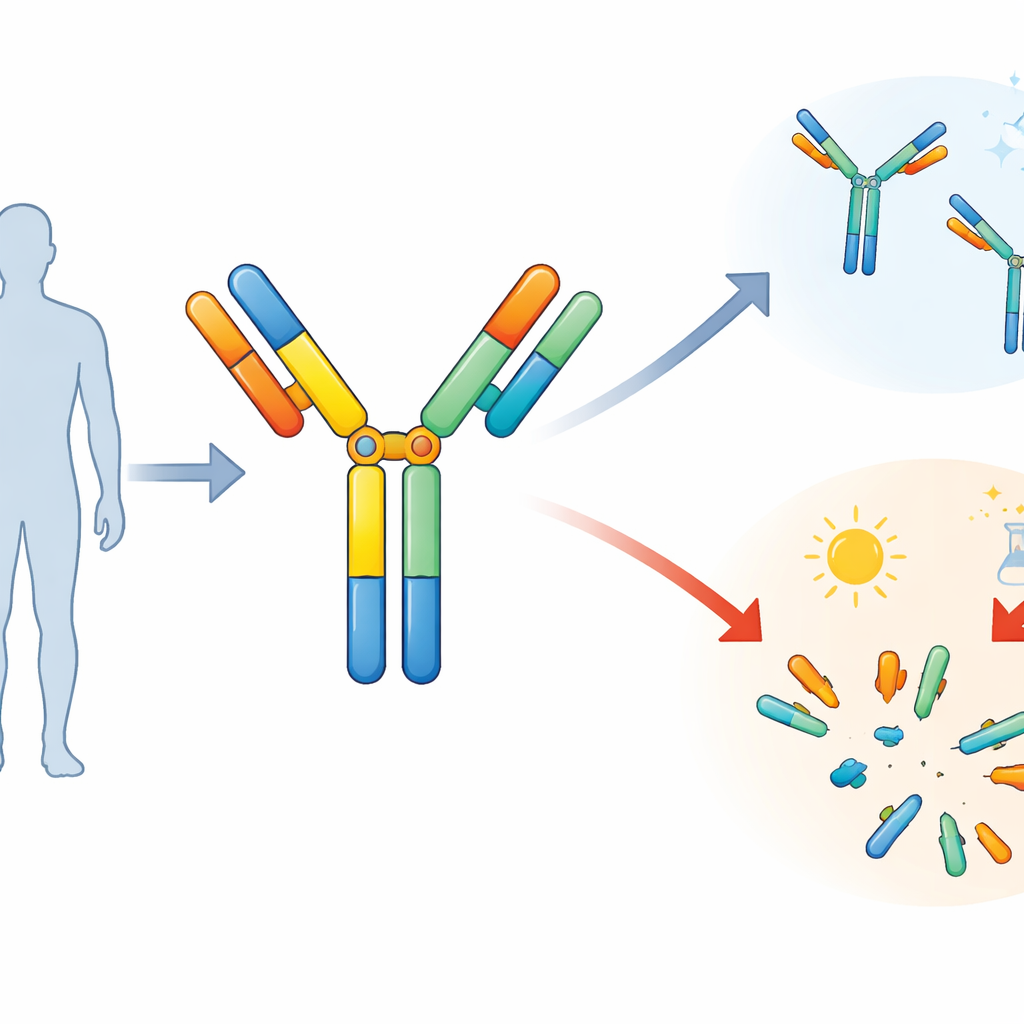
Fokussierung auf die Bruchstellen
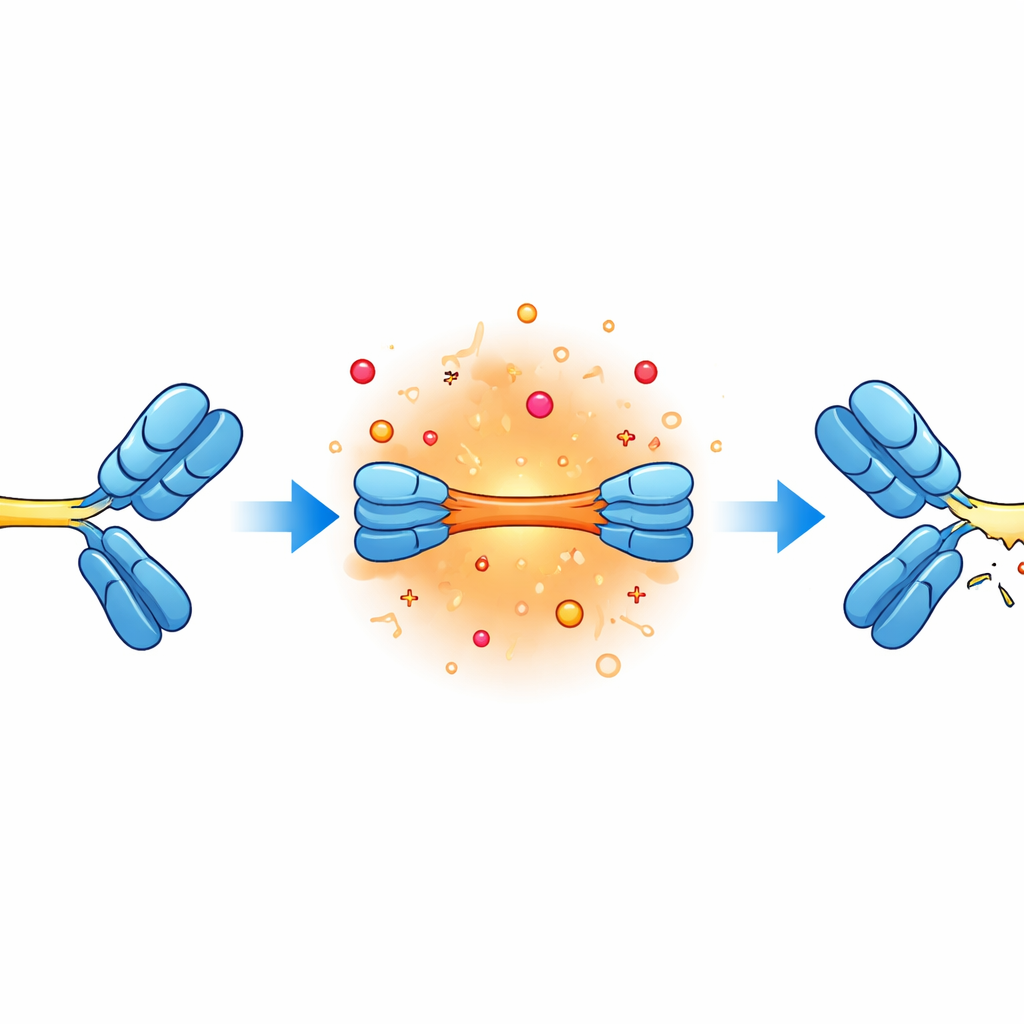
Im nächsten Schritt wollten die Forschenden genau herausfinden, wo die Brüche stattfanden. Sie isolierten die verschiedenen Fragmente und analysierten deren Massen mittels hochauflösender Massenspektrometrie, gewissermaßen indem sie die Teile wie ein molekulares Puzzle wogen und rekonstruirten. Dabei zeigte sich, dass zwei spezifische Linker—kurze Sequenzen, häufig als G4S und G4 bezeichnet—besonders anfällig für Schnitte waren. Diese flexiblen Verbindungsstücke sitzen zwischen den Hauptarmen des Antikörpers und den hinzugefügten Bindungssegmenten. Unter alkalischen, salzhaltigen und warmen Bedingungen wurden die Peptidbindungen in diesen Bereichen schrittweise gespalten, wodurch eine Reihe vorhersehbarer Fragmente entlang der Linkerketten entstanden.
Nicht nur die Verbindungen: weitere gefährdete Bindungen
Die Analyse zeigte außerdem Schäden an anderen empfindlichen Stellen. Einige Brüche traten in der Nähe bestimmter Asparagin-Bausteine auf, die dafür bekannt sind, bei hohem pH langsame chemische Veränderungen zu durchlaufen, die schließlich zur Kettenspaltung führen können. Zusätzlich wurden Bindungen betroffen, an denen schwefelhaltige Cysteinreste beteiligt sind, die normalerweise helfen, schwere und leichte Ketten von Antikörpern zusammenzuhalten. Dies führte zu losgelösten Leichtketten und verschiedenen chemisch modifizierten Varianten. Während diese Arten von Veränderungen aus Untersuchungen zu herkömmlichen monoklonalen Antikörpern vertraut sind, deutet ihr Auftreten in der Nähe der Linker-Regionen darauf hin, dass die zusätzliche Flexibilität des bispezifischen Designs benachbarte Bindungen einem erhöhten Stress aussetzen kann.
Gestaltungsprinzipien für sichere und stabilere Wirkstoffe
Für Nichtfachleute lautet die wichtigste Erkenntnis: Antikörper durch zusätzliche Bindungsarme vielseitiger zu machen, ist nicht nur eine Frage clevere genetischer Konstruktion; es erfordert auch sorgfältige Beachtung der kleinen Verbindungsregionen, die alles zusammenhalten. In diesem Fall erwiesen sich die häufig verwendeten flexiblen Linker, die die funktionalen Teile des bispezifischen Antikörpers verbinden, unter realistischen Stressbedingungen als strukturelle Schwachstellen. Die Schlussfolgerung der Studie ist nicht, dass bispezifische Antikörper unsicher seien, sondern dass ihre Stabilität stark davon abhängt, wie diese Linker zusammengesetzt und positioniert sind. Künftige Entwürfe müssen Linkerlänge, Sequenz und das lokale Umfeld optimieren, damit die nächste Generation von Antikörpertherapien ihr volles klinisches Potenzial entfalten kann, ohne während Herstellung, Lagerung oder Behandlung auseinanderzufallen.
Zitation: Ingavat, N., Kok, Y.J., Dzulkiflie, N. et al. Structural stability of symmetric bispecific antibodies: a case study showing potential compromise near linker regions. Sci Rep 16, 9715 (2026). https://doi.org/10.1038/s41598-026-40607-2
Schlüsselwörter: bispezifische Antikörper, Proteinstabilität, Linker-Design, Antikörper-Engineering, biopharmazeutische Entwicklung