Clear Sky Science · de
Theoretische Analyse der energiearmen optogenetischen Unterdrückung von Aktionspotenzialen in mittels kaliumselektiver Channelrhodopsine exprimierten menschlichen ventrikulären Kardiomyozyten
Ein sanfteres, lichtbasiertes Verfahren zur Beruhigung eines rasenden Herzens
Schnelle, chaotische Herzrhythmen können Ohnmacht, Schlaganfall oder plötzlichen Tod auslösen. Die heutigen Behandlungen — potente Medikamente, implantierbare Defibrillatoren oder Hochenergie‑Schocks — können Leben retten, sind jedoch oft schmerzhaft und unpräzise. Diese Studie untersucht eine ganz andere Idee: schwache Lichtblitze und speziell entwickelte Proteine zu verwenden, um Herzzellen leise zurück in einen sicheren, stabilen Rhythmus zu lenken — und das mit deutlich weniger Energie als bei heutigen Ansätzen.
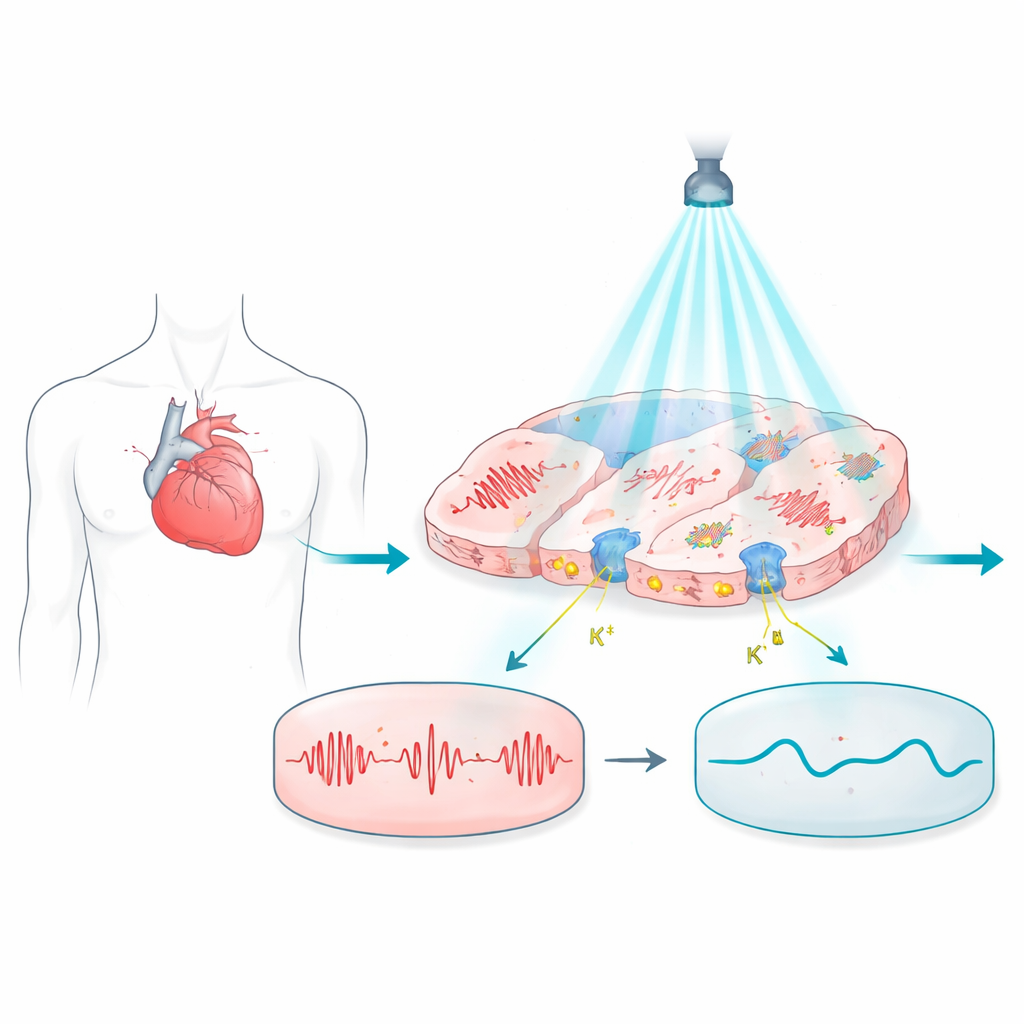
Den problematischen Herzschlag mit Licht beleuchten
Die Arbeit baut auf Optogenetik auf, einer Technik, bei der Zellen mit lichtempfindlichen Proteinen ausgestattet werden, sodass ihre elektrische Aktivität mittels Lichtblitzen gesteuert werden kann. Im Herzen können diese Proteine prinzipiell Metallelektroden ersetzen und eine kontaktfreie, schmerzfreie Steuerung ermöglichen. Die bislang verwendeten lichtgesteuerten Proteine neigen jedoch meist dazu, das Membranpotenzial in Richtung einer erregten, positiveren Spannung zu treiben, was es schwierig macht, die Zellen ruhig im Ruhezustand zu halten oder fein zu steuern, wie lange ein Herzschlag dauert. Das schränkt ihre Nützlichkeit für das sichere Abschalten gefährlicher Rhythmen oder die Korrektur zeitlich sensitiver elektrischer Störungen ein.
Neue Lichtschalter, abgestimmt auf die „Ruhe‑Einstellung“ des Herzens
Kürzlich entdeckte Proteine, sogenannte kaliumselektive Channelrhodopsine, darunter WiChR und HcKCR1, versprechen, dieses Missverhältnis zu beheben. Anders als ältere Proteine, die verschiedene geladene Ionen passieren lassen, bevorzugen diese Kanäle stark Kalium und ziehen das Membranpotenzial natürlich wieder auf das negative Niveau, das es im Ruhezustand annimmt. Die Autoren erstellten detaillierte Computermodelle menschlicher ventrikulärer Herzzellen, die diese neueren Kanäle exprimieren, und verglichen sie mit zwei bekannten, stärker erregenden Opsinen, ChR2(H134R) und ChRmine. Durch Simulationen, wie diese Zellen auf unterschiedliche Lichtfarben und -intensitäten reagieren, konnten sie sicher Situationen untersuchen, die in echten Herzen schwer oder zeitaufwendig zu testen wären.
Sanftes Licht, starke Kontrolle
Die Simulationen zeigen, dass kaliumselektive Kanäle deutlich wirtschaftlichere und stabilere Kontrolle ermöglichen. Insbesondere WiChR konnte Aktionspotenziale — die kurzen elektrischen Spitzen, die jeden Herzschlag auslösen — bei Lichtintensitäten vollständig unterdrücken, die hunderte bis tausende Male niedriger sind als die, die für viele frühere Werkzeuge erforderlich waren. Unter Dauerlicht hielten WiChR und HcKCR1 das Membranpotenzial nahe seinem normalen Ruhewert und hielten die Zelle damit effektiv in einem ruhigen, sicheren Zustand. Im Gegensatz dazu neigten ChR2 und ChRmine dazu, das Potenzial in Richtung positiver Werte zu treiben und manchmal die Aktivität zu blockieren, jedoch meist erst nachdem die Zelle in einen gestressten, übererregten Zustand gezwungen worden war. WiChR funktionierte auch gut mit kurzen Lichtpulsen und verhinderte verlässlich Herzzellenspikes Schlag für Schlag, was nahelegt, dass es mit schnellen Herzrhythmen mithalten kann, ohne Gewebe zu überhitzen oder Energie zu verschwenden.
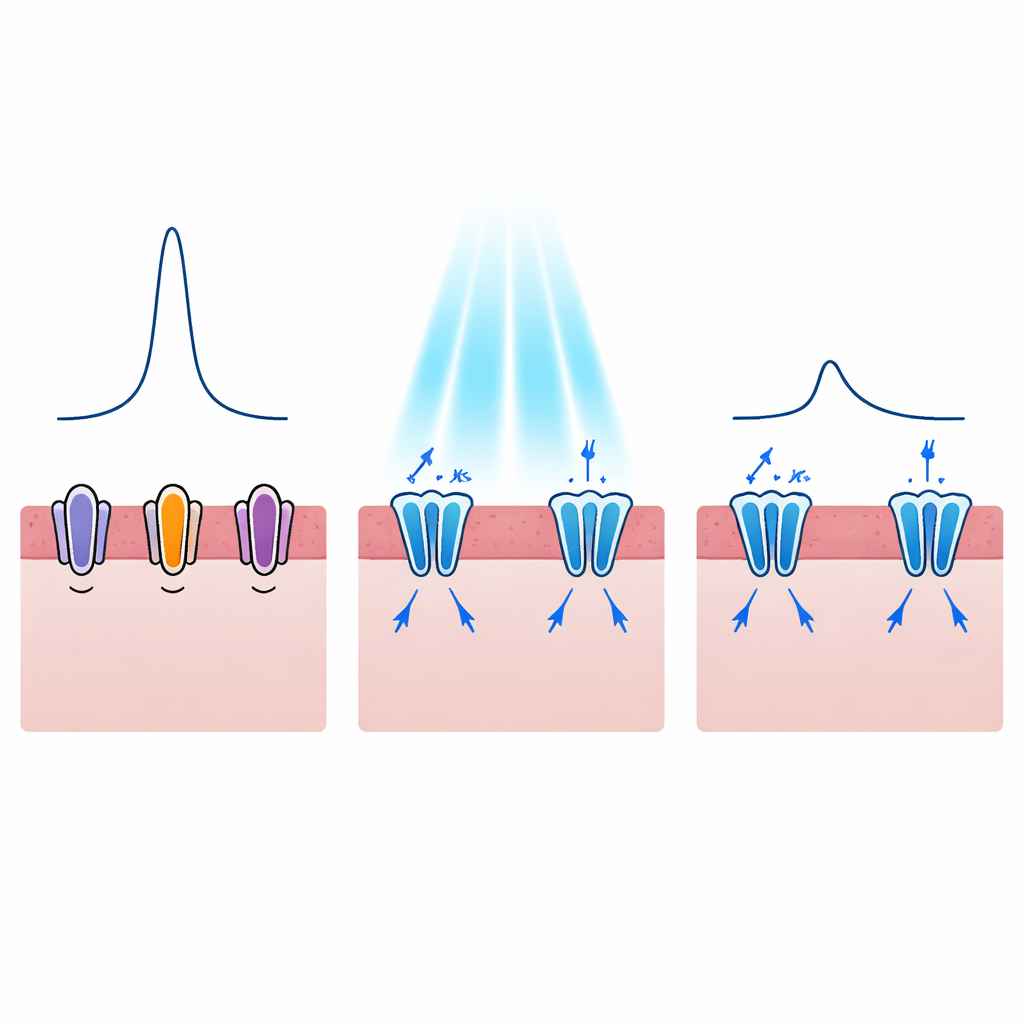
Den Herzschlag formen, nicht nur stoppen
Gefährliche Arrhythmien hängen oft nicht nur davon ab, ob eine Herzzelle feuert, sondern auch davon, wie lange sie erregt bleibt. Bei Erkrankungen wie dem Long‑QT‑Syndrom ist der elektrische Impuls jedes Schlages verlängert, wodurch die Wahrscheinlichkeit steigt, in lebensbedrohliche Rhythmen zu kippen. Die Autoren fragten daher, ob lichtaktivierte Kaliumkanäle diesen Impuls kontrolliert verkürzen könnten. Ihre Modelle zeigten, dass das Einschalten von WiChR oder HcKCR1 während der Plateauphase des Aktionspotenzials starke auswärts gerichtete Kaliumströme erzeugte, die das Potenzial früher wieder nach unten zogen. Mit zunehmender Lichtstärke verringerte sich die Dauer des elektrischen Impulses von etwa 300 Millisekunden auf ungefähr die Hälfte, und dieser Effekt war bereits mit sehr kurzen Lichtblitzen erreichbar. WiChR erzeugte tendenziell länger anhaltende Ruhephasen, während HcKCR1 ein schnelleres Wiederansteigen nach Abschalten des Lichts erlaubte, was auf unterschiedliche potenzielle klinische Anwendungen hindeutet.
Von Computermodellen zu künftigen Therapien
Insgesamt kommt die Studie zu dem Schluss, dass kaliumselektive lichtgesteuerte Kanäle, insbesondere WiChR, vielversprechende Werkzeuge für eine sanfte, energiearme Kontrolle des Herzens sind. Sie können sowohl ausufernde elektrische Aktivität zum Schweigen bringen als auch überlange Herzschläge kürzen, und das alles, während sie das Membranpotenzial nahe seinem natürlichen Ruhewert halten. Zwar stammen die Ergebnisse aus detaillierten Einzelzell‑Simulationen und nicht aus Ganzherz‑Experimenten, doch liefern sie quantitative Hinweise darauf, wie viel Licht erforderlich sein könnte, wann es appliziert werden sollte und welche Proteinvarianten sich für welche Ziele am besten eignen. Langfristig deutet diese Forschungsrichtung auf eine Zukunft hin, in der Kardiologen fein abgestimmte Lichtstrahlen anstelle schmerzhafter Schocks nutzen könnten, um lebensbedrohliche Arrhythmien zu verhindern oder zu beenden.
Zitation: Dixit, N., Pyari, G. & Roy, S. Theoretical analysis of low-power optogenetic suppression of action potentials in human ventricular cardiomyocytes expressed with potassium-selective channelrhodopsins. Sci Rep 16, 9765 (2026). https://doi.org/10.1038/s41598-026-40578-4
Schlüsselwörter: kardiale Optogenetik, Unterdrückung von Arrhythmien, kaliumselektive Channelrhodopsine, Dauer des Aktionspotenzials, Long-QT-Syndrom