Clear Sky Science · de
In-ovo-Geschlechtsbestimmung und Genotypisierung mittels PCR-Techniken: ein Beitrag zu den 3R-Prinzipien in der Geflügelzucht
Warum das, was im Ei passiert, wichtig ist
Jedes Jahr werden Millionen männlicher Küken kurz nach dem Schlüpfen getötet, weil sie für die Eierproduktion nicht brauchbar sind. Gleichzeitig schlüpfen Forschungslabore weltweit mehr Tiere als nötig, schlicht weil sie das Geschlecht oder den genetischen Aufbau eines Embryos nicht früh genug bestimmen können. Diese Studie stellt einen praxisnahen Weg vor, das Geschlecht und die Gene eines Kükens zu „lesen“, während es noch im Ei heranwächst, mithilfe standardisierter DNA‑Tests. Indem dies früh und schonend erfolgt, soll das Schlüpfen überzähliger Tiere vermieden und Leiden reduziert werden, ohne teure industrielle Ausrüstung zu benötigen.
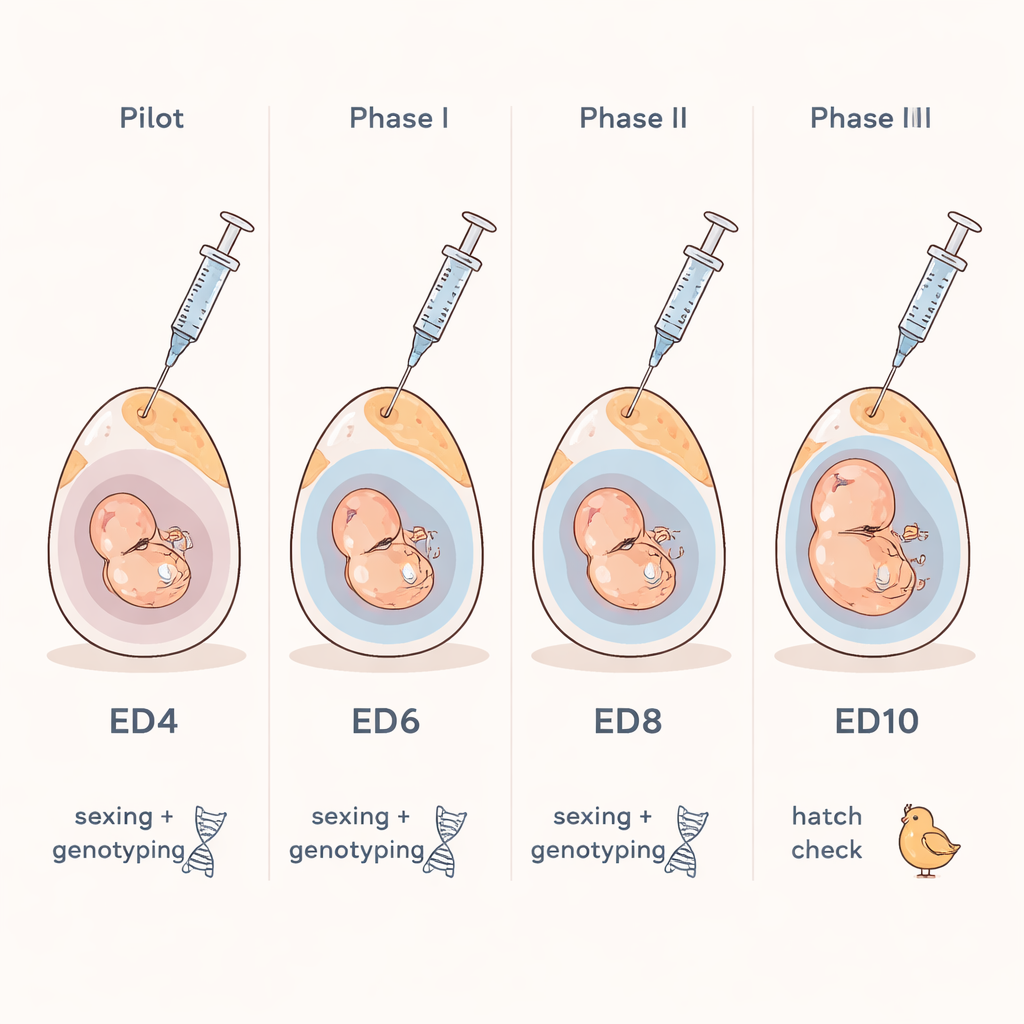
Ins Ei sehen, ohne es zu öffnen
Die Forschenden konzentrierten sich auf eine einfache Frage: Kann man sicher eine winzige Flüssigkeitsprobe aus einem befruchteten Hühnerei entnehmen und damit das Geschlecht und zentrale genetische Merkmale des Embryos bestimmen? Sie griffen auf ein aus der Humanmedizin bekanntes Konzept zurück, bei dem Flüssigkeit um einen Fötus auf genetische Erkrankungen untersucht wird. Beim Huhn bildet sich während des Wachstums eine dünne, mit Flüssigkeit gefüllte Membran, die Allantois. Bis zum siebten Tag der Brut enthält diese Membran genügend Flüssigkeit, dass eine feine Nadel sie erreichen kann, ohne den Embryo zu berühren. Das Team nutzte ein starkes Licht, um den Luftsack am stumpfen Ende des Eies zu lokalisieren, bohrte ein nadelgroßes Loch in die Schale und entnahm mit einer winzigen Spritze nur wenige Tropfen Flüssigkeit.
Von wenigen Tropfen zur genetischen Signatur
Die aus Eiern in frühen Entwicklungsstadien entnommene Flüssigkeit enthält nur winzige Mengen an DNA. Um dies zu kompensieren, vervielfältigten die Wissenschaftler*innen zunächst das gesamte genetische Material der Probe und erzeugten viele Kopien, ohne den Inhalt zu verändern. Anschließend wendeten sie zwei routinemäßige Labortests an: eine Standard‑Polymerase‑Kettenreaktion (PCR) und eine Variante namens Kompetitive Allelspezifische PCR (KASP). Beide Tests unterscheiden die Geschlechtschromosomen von männlichen und weiblichen Küken und können zudem spezifische genetische Marker nachweisen, etwa die Mutation für blaue Eierschalen oder das Vorhandensein eines im Labor eingeführten Gens in speziellen Forschungszuchtlinien. An über 800 Eiern mehrerer Rassen – darunter kommerzielle Legehybriden, bunte Araucana‑Kreuzungen und eine gentechnisch veränderte Versuchslinie – erzielten diese Methoden in etwa 92–100 % der Fälle korrekte Ergebnisse.
Das sicherste Zeitfenster für die Probenentnahme finden
Eine zu frühe Probennahme gefährdet fragile Strukturen, die für den Embryo lebenswichtig sind, während eine zu späte Entnahme wenig Zeit lässt, um auf die Ergebnisse zu reagieren. Um das ideale Zeitfenster zu bestimmen, kultivierte das Team Embryonen zunächst ohne Schale, um zu beobachten, wie sich Membranen und Flüssigkeitsräume im Zeitverlauf ausdehnen. Danach führten sie eine Reihe gestaffelter Versuche in intakten Eiern durch. Flüssigkeit konnte ab dem vierten Tag entnommen werden, allerdings waren die Erfolgsraten für DNA‑Tests in diesen frühen Stadien niedriger und die Prozedur technisch schwieriger. Beim Vergleich der Schlupfraten zwischen punktierten und unbehandelten Kontroll‑Eiern zeigte sich, dass Tag sieben die beste Balance darstellt: Es war ausreichend klare Allantoisflüssigkeit vorhanden, DNA‑Tests funktionierten zuverlässig und die meisten Embryonen überlebten bis zum Schlupf. Zu diesem Zeitpunkt liegen noch mehrere Tage vor dem wahrscheinlichen Einsetzen der Schmerzwahrnehmung beim Kükenembryo, was einen ethischen Puffer für Entscheidungen bietet.
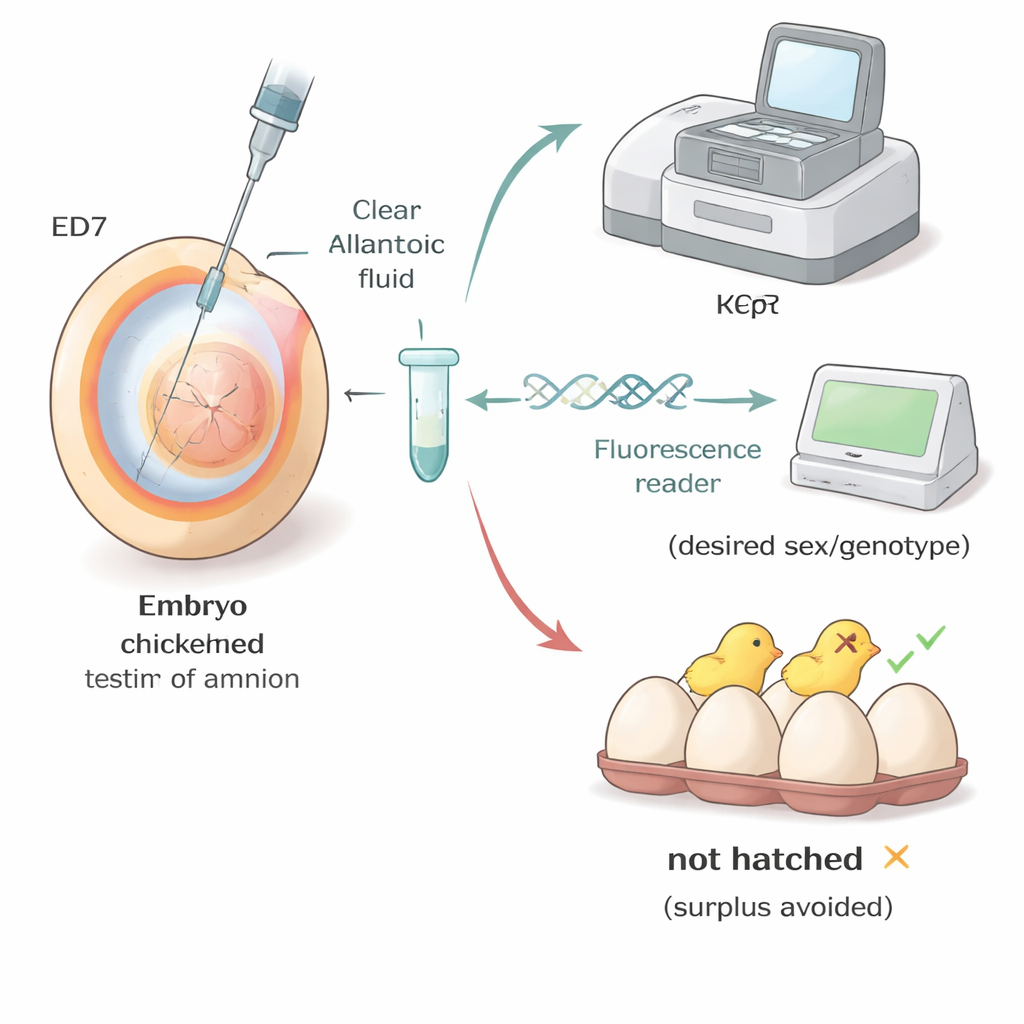
Die Methode in realen Herden anwenden
Die Forschenden testeten ihren Arbeitsablauf unter Bedingungen, die denen in Zuchtbetrieben und Universitätslaboren ähneln. In kommerziellen braunen und weißen Lege‑Linien zeigte sich bei Eiern, die zwischen Tag vier und sieben beprobt wurden, dass die Schlupfrate generell besser war, wenn die Probenahme später erfolgte, mit den besten Ergebnissen erneut an Tag sieben. In einer spezialisierten „Surrogat‑Host“‑Linie für erweiterte Genetik gingen sie noch einen Schritt weiter: Sie bestimmten an Tag sieben Geschlecht und Genotyp der Embryonen und ließen nur diejenigen mit der gewünschten Kombination weiterschlüpfen. Fast alle ausgewählten Embryonen schlüpften zu gesunden Küken und entwickelten sich wie erwartet, was zeigt, dass eine frühe Auswahl die Zahl unerwünschter Tiere stark reduzieren kann, ohne die Qualität der Küken zu beeinträchtigen.
Was das für Tierschutz und Forschung bedeutet
Für Nicht‑Spezialist*innen ist die Kernaussage klar: Mit einem Nadelstich und routinemäßigen Labormethoden ist es jetzt möglich, während das Küken noch sicher im Ei ist, sein Geschlecht und das Vorhandensein bestimmter genetischer Merkmale zu kennen. Die Studie zeigt, dass eine Untersuchung um den siebten Bruttag technisch zuverlässig und schonend genug ist, dass die Mehrheit der Embryonen überlebt. Indem unerwünschte Embryonen entfernt werden können, bevor sie vermutlich schmerzempfindungsfähig sind, unterstützt der Ansatz die weithin akzeptierten 3R‑Prinzipien: Replace (Ersetzen), Reduce (Vermindern) und Refine (Verfeinern) des Einsatzes von Tieren in der Forschung. Für Brütereien und Labore bietet diese Technik einen realistischen Weg zu weniger überzähligen Tieren, besserer Ressourcennutzung und höheren Tierschutzstandards – ohne den Bedarf an komplexen Industrieanlagen.
Zitation: Dierks, C., Förster, A., Meunier, D. et al. In ovo sexing and genotyping using PCR techniques: a contribution to the 3R principles in chicken breeding. Sci Rep 16, 7464 (2026). https://doi.org/10.1038/s41598-026-40562-y
Schlüsselwörter: Kükenembryo, In-ovo-Geschlechtsbestimmung, PCR-Genotypisierung, Tierschutz, 3R-Prinzipien