Clear Sky Science · de
Blutspiegel von MMP-7 und TNF-α als potenzielle prognostische Biomarker für pulmonale Langerhans-Zell-Histiozytose bei Erwachsenen
Warum das für Rauchende wichtig ist
Die pulmonale Langerhans-Zell-Histiozytose (PLCH) ist eine seltene Lungenerkrankung, die fast ausschließlich Raucher betrifft und häufig Menschen in der Lebensmitte trifft. Manche Patientinnen und Patienten kommen über Jahre hinweg recht gut zurecht, während andere schnell an Lungenfunktion verlieren und schwere Atemprobleme entwickeln. Ärztinnen und Ärzte haben derzeit keine einfache Möglichkeit, bereits bei der Diagnose zu unterscheiden, welchen Verlauf ein einzelner Patient nehmen wird. Die vorliegende Studie fragt, ob ein routinemäßiger Bluttest frühzeitig anzeigen könnte, bei welchen Personen die Lunge wahrscheinlich eher verschlechtert.
Eine seltene Lungenerkrankung mit zwei unterschiedlichen Verläufen
Charakteristisch für PLCH sind Ansammlungen abnormaler Immunzellen, die in die kleinen Atemwege eindringen und diese schädigen, wodurch Narben und Zysten in der Lunge entstehen. Frühere Untersuchungen an einer großen französischen Kohorte zeigten, dass die meisten Patientinnen und Patienten einen „stabilen“ Verlauf haben: Ihre Lungenkapazität, gemessen als forciertes exspiratorisches Volumen in einer Sekunde (FEV1), liegt zu Beginn nahe dem Normalwert und bleibt im Zeitverlauf relativ konstant. Eine kleinere Gruppe beginnt mit niedrigerem FEV1 und nimmt Jahr für Jahr weiter ab, mit erhöhtem Risiko für respiratorisches Versagen und Tod. Das Problem ist, dass bei der Diagnose die üblichen klinischen Merkmale diese beiden Gruppen nicht zuverlässig unterscheiden. Daher wandten sich die Autorinnen und Autoren Molekülen im Blut zu, die widerspiegeln könnten, was tief in der Lunge vor sich geht.
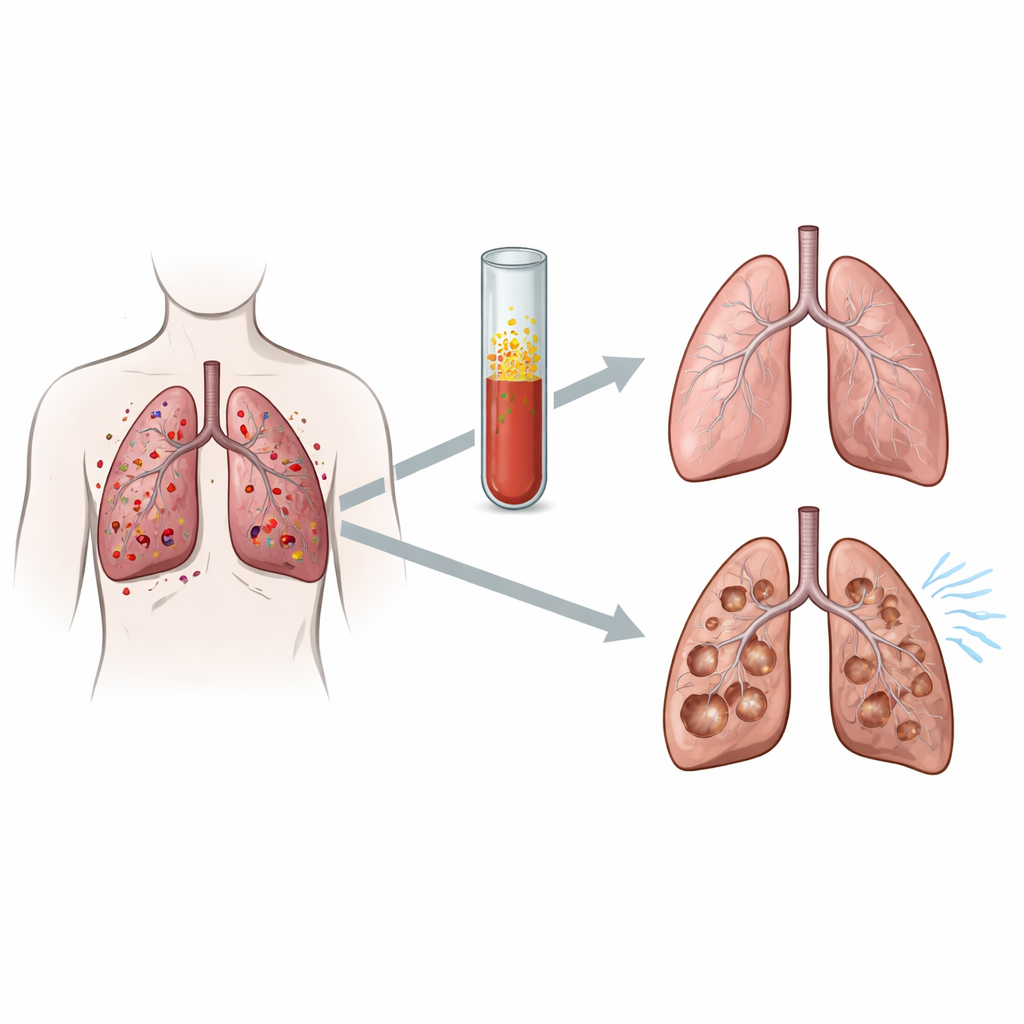
Ein genauerer Blick auf Blut-Signale
Die Forschenden nutzten ein nationales Register Erwachsener mit PLCH in Frankreich. Aus dieser größeren Kohorte konzentrierten sie sich auf 25 Patientinnen und Patienten, von denen zum Zeitpunkt der Erstdiagnose Blutproben konserviert waren und deren Tabakkonsum, Alter und Geschlecht abgeglichen werden konnten. Neun dieser Personen zeigten später über mehrere Jahre einen kontinuierlichen Abfall des FEV1, während 16 eine stabile Lungenfunktion behielten. Mit Multiplex-Immunoassays — Labortests, die viele Substanzen gleichzeitig messen können — bestimmten sie die Konzentrationen von 30 verschiedenen Immun- und Gewebsumbau-Molekülen in jeder Blutprobe. Dazu gehörten entzündliche Botenstoffe, chemotaktische Faktoren für Immunzellen, Wachstumsfaktoren und Enzyme, die das Gerüst des Lungengewebes abbauen können.
Zwei hervorstechende Moleküle, die mit schlechterer Lungenfunktion verbunden sind
Unter allen getesteten Mediatoren hoben sich zwei Moleküle deutlich ab: Tumornekrosefaktor alpha (TNF-α), ein starkes entzündliches Signal, und Matrix-Metalloproteinase-7 (MMP-7), ein Enzym, das strukturelle Gewebekomponenten abbauen kann. Bei der Diagnose waren sowohl TNF-α als auch MMP-7 in denjenigen Patienten signifikant erhöht, die später einen FEV1-Abfall erlitten, verglichen mit denen, deren Lungenfunktion stabil blieb — und das trotz Berücksichtigung von Alter, Geschlecht und Rauchintensität. Bedeutend war, dass höhere MMP-7-Werte bei der Diagnose stark mit schlechterem FEV1 und einer schlechteren Gasaustauschkapazität (DLCO) zum selben Zeitpunkt verknüpft waren, was darauf hindeutet, dass dieses Enzym das Ausmaß struktureller Lungenschädigung widerspiegelt. TNF-α war zwar ebenfalls in der abfallenden Gruppe erhöht, zeigte jedoch keine so enge Korrelation mit den numerischen Lungenfunktionswerten, was darauf hindeutet, dass es eher die allgemeinere Krankheitsaktivität als die direkte Zerstörung der Atemwegswände abbilden könnte.
Von Blutwerten zur Risikovorhersage
Um zu prüfen, ob diese Blutmarker helfen könnten, Patientinnen und Patienten mit Risiko für einen späteren Abfall zu identifizieren, verwendete das Team statistische Werkzeuge, sogenannte Receiver-Operating-Characteristic-(ROC)-Kurven. Sie bestimmten Schwellenwerte für MMP-7 und TNF-α, die die abfallende Gruppe am besten von der stabilen Gruppe trennten. Besonders für MMP-7 war ein hoher Wert bei der Diagnose mit einer guten Wahrscheinlichkeit verbunden, dass die Betroffenen später Lungenfunktion verlieren würden; noch aussagekräftiger war jedoch, dass Patienten unterhalb dieses Schwellenwerts mit hoher Wahrscheinlichkeit stabil blieben. Anders formuliert: Ein niedriger MMP-7-Wert könnte beruhigend wirken, während ein hoher Wert engmaschigere Nachsorge und frühzeitige therapeutische Überlegungen nahelegt. Einige weitere Immunbotenstoffe zeigten ebenfalls auffällige Unterschiede zwischen den Gruppen, doch war die Studie mit 25 Patienten zu klein, um deren Bedeutung sicher zu bestätigen.
Was das zukünftig für Patientinnen und Patienten bedeuten könnte
Diese Arbeit legt nahe, dass ein einfacher Bluttest zur Messung von TNF-α und insbesondere MMP-7 eines Tages Ärztinnen und Ärzten helfen könnte, PLCH-Patienten kurz nach der Diagnose in niedrig- und höher-riskante Gruppen einzuteilen. Ein solches Instrument könnte steuern, wie häufig Kontrollen stattfinden sollten, wie intensiv zur Rauchentwöhnung geraten wird und wann experimentelle oder zielgerichtete Therapien in Betracht gezogen werden sollten. Da die Studie nur 25 Patientinnen und Patienten umfasste, sind die Ergebnisse vorläufig und bedürfen der Bestätigung in größeren Kohorten. Dennoch stellen die Befunde einen vielversprechenden Schritt in Richtung einer personalisierteren Versorgung bei einer seltenen, raucherbedingten Lungenerkrankung dar, in der eine frühe Warnung vor Verschlechterung bislang fehlte.
Zitation: Benattia, A., Porcher, R., Terry, S. et al. Blood MMP-7 and TNF-α levels as potential prognostic biomarkers for adult pulmonary Langerhans cell histiocytosis. Sci Rep 16, 10059 (2026). https://doi.org/10.1038/s41598-026-40540-4
Schlüsselwörter: pulmonale Langerhans-Zell-Histiozytose, raucherbedingte Lungenerkrankung, Blut-Biomarker, MMP-7, Abnahme der Lungenfunktion