Clear Sky Science · de
Die MEOX1-PAX1-Achse reguliert koordiniert Tumormalignität und Treg-Differenzierung im Glioblastom
Warum diese Studie zum Gehirntumor wichtig ist
Glioblastom gehört zu den tödlichsten Hirntumoren, teilweise deshalb, weil der Tumor sich schnell vermehren kann und sich zugleich der Abwehr des Körpers entzieht. Diese Studie identifiziert eine molekulare „Befehlskette“ in Tumorzellen, die nicht nur ihr aggressives Verhalten antreibt, sondern auch benachbarte Immunzellen in einen Ruhemodus versetzt. Durch das Entschlüsseln dieser Kette zeigt die Forschung einen Ansatz auf, sowohl den Krebs als auch seinen immunologischen Schutz gleichzeitig anzugreifen.
Ein tödlicher Tumor, der die Abwehr entwaffnet
Das Glioblastom ist berüchtigt dafür, nach Operation, Bestrahlung und Chemotherapie zurückzukehren. Ein Grund dafür ist seine feindliche Nachbarschaft, die sogenannte Tumormikroumgebung. Anstatt von krebsbekämpfenden Zellen durchsetzt zu sein, enthält diese Umgebung oft Immunzellen, die den Tumor tatsächlich schützen. Zu den wichtigsten gehören regulatorische T-Zellen, oder Tregs, eine Art weißer Blutkörperchen, die normalerweise übermäßige Entzündungen verhindern. Beim Glioblastom sammeln sich jedoch Tregs rund um den Tumor und helfen ihm, einer Immunattacke zu entgehen.
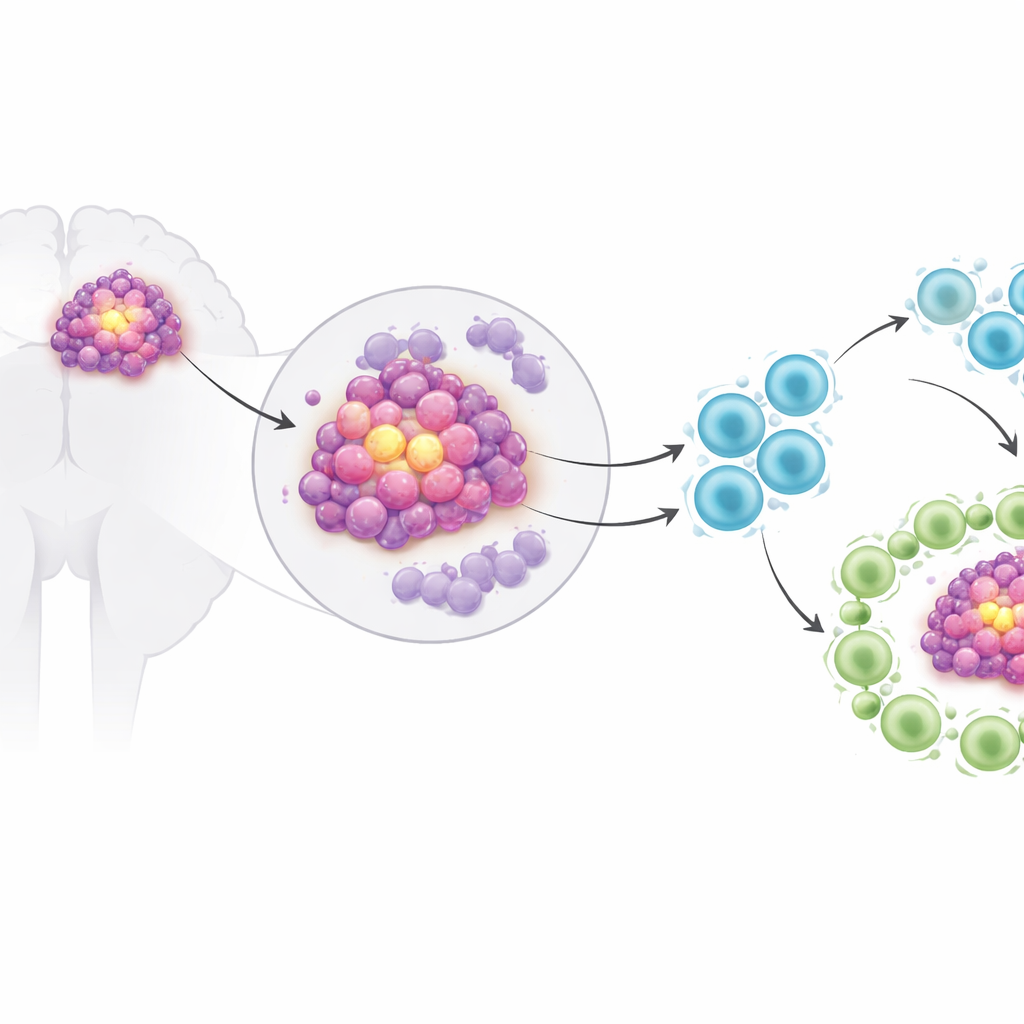
Zwei Schlüsselschalter in Tumorzellen
Die Forschenden konzentrierten sich auf zwei Proteine, die in Zellen wie genetische Schalter wirken: MEOX1 und PAX1. Frühere Arbeiten setzten MEOX1 mit Krebswachstum in Verbindung und deuteten an, dass es Immunzellen beeinflussen könnte, während PAX1 eher als Tumorsuppressor bekannt ist, der das Zellwachstum bremst. In im Labor gezüchteten Glioblastomzellen zeigte das Team, dass eine Erhöhung von MEOX1 die Tumorzellen schneller teilen, sich leichter bewegen und Barrieren durchdringen ließ, während zugleich ihre Neigung zum Zelltod sank. Eine Verringerung von MEOX1 hatte den gegenteiligen Effekt: verlangsamtes Wachstum und vermehrten Zelltod. Weiter zeigten sie, dass MEOX1 diese Effekte ausübt, indem es PAX1 abschaltet; werden die PAX1-Spiegel wiederhergestellt, verschwinden die schädlichen Wirkungen von MEOX1 weitgehend.
Von Tumorschaltern zur Immunumformung
Die Studie ging über das Tumorwachstum hinaus und untersuchte, wie dieses interne Schaltwerk Immunzellen beeinflusst. Die Wissenschaftler kultivierten menschliche Glioblastomzellen zusammen mit gereinigten CD4-T-Zellen, einer Gruppe von Immunzellen, die sich entweder zu angreifenden Helferzellen oder zu dämpfenden Tregs entwickeln können. Sie fanden heraus, dass bei reduziertem PAX1 in Tumorzellen mehr der benachbarten T-Zellen zu Tregs wurden. Bei erhöhtem PAX1 nahmen weniger T-Zellen diese unterdrückende Identität an. Gewebeproben eines Glioblastompatienten zeigten mehr Tregs im Tumorbereich als im angrenzenden, nicht tumorösen Hirngewebe, was mit den Laborbefunden übereinstimmt. Diese Ergebnisse deuten darauf hin, dass der PAX1-Spiegel in Tumorzellen ein entscheidender Faktor ist, der lokale Immunzellen in eine tumorprotektive Richtung lenkt.
Eine Achse, doppelter Vorteil für den Tumor
Insgesamt stützen die Daten ein Modell, wonach hohes MEOX1 in Glioblastomzellen PAX1 senkt und dem Tumor damit einen doppelten Vorteil verschafft. Innerhalb der Krebszellen fördert diese Verschiebung Wachstum, Bewegung und Widerstand gegen das Absterben. Außerhalb der Zellen trägt sie dazu bei, gewöhnliche T-Zellen in Tregs umzuwandeln, die sich in der Tumorumgebung ansiedeln und Immunangriffe dämpfen. Auf diese Weise verbindet die MEOX1–PAX1-Achse den inneren Motor der Tumoraggressivität mit der äußeren Schicht der Immunsuppression und schafft ein eng verknüpftes System, das dem Überleben des Tumors zuträglich ist.
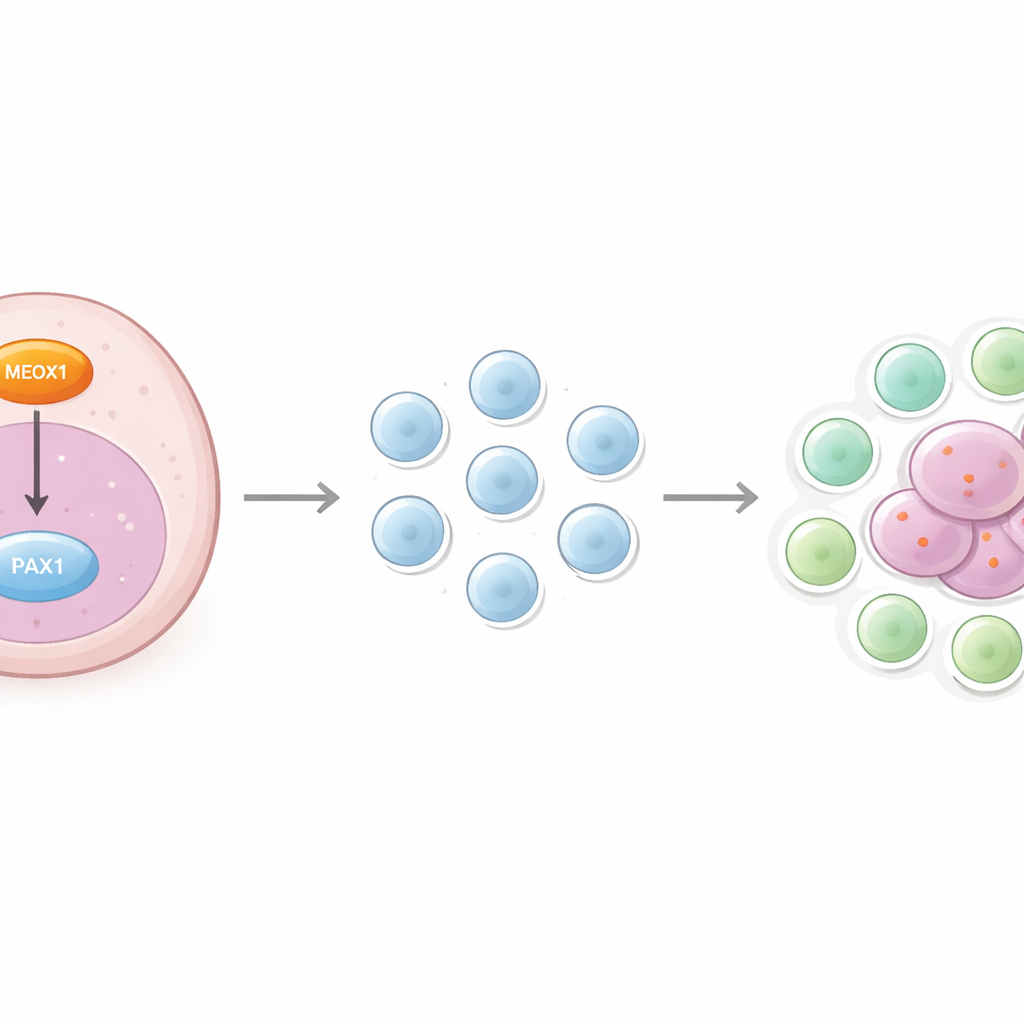
Was das für zukünftige Behandlungen bedeuten könnte
Für Menschen mit Glioblastom heben diese Befunde eine vielversprechende therapeutische Idee hervor: die MEOX1–PAX1-Achse anzugreifen, um gleichzeitig den Tumor und seinen immunologischen Schutz zu treffen. Wirkstoffe, die MEOX1 blockieren oder die PAX1-Aktivität wiederherstellen, könnten das Tumorwachstum verlangsamen und gleichzeitig die Zahl der Tregs in der Tumormikroumgebung verringern, wodurch bestehende Therapien, einschließlich Immuntherapien, wirksamer werden könnten. Obwohl diese Ergebnisse aus Zell- und Gewebeexperimenten stammen und noch in lebenden Organismen geprüft werden müssen, liefern sie eine klarere Karte dafür, wie das Glioblastom das Immunsystem überlistet — und weisen auf neue Wege hin, das Gleichgewicht zugunsten der Patientinnen und Patienten zu verschieben.
Zitation: Pan, P., Wang, R., Lv, P. et al. The MEOX1-PAX1 axis coordinately regulates tumor cell malignancy and Treg differentiation in glioblastoma. Sci Rep 16, 9136 (2026). https://doi.org/10.1038/s41598-026-40453-2
Schlüsselwörter: Glioblastom, Tumormikroumgebung, regulatorische T-Zellen, tumorinduzierte Immunsuppression, krebsbezogene Signalwege