Clear Sky Science · de
Stimuli-responsivere, chitosan-beschichtete Ferrit-Nanotransporter für gezielte Capsaicin-Freisetzung und kernabhängige, HepG2-selektive Bioaktivität
Gewürz mit verborgener Kraft
Chilis geben unserem Essen mehr als nur Schärfe: Das Brennen stammt von Capsaicin, einer natürlichen Verbindung, die auch Krebszellen abtöten kann. Die Nutzung von Capsaicin als Arzneimittel ist jedoch schwierig, weil es schlecht in Wasser löslich ist, im Körper schnell verschwindet und bei hohen Dosen gesundes Gewebe reizt. Diese Studie untersucht einen Weg, dieses feurige Molekül zu bändigen, indem es in winzige, intelligente Partikel verpackt wird, die Capsaicin sicher durch den Blutkreislauf transportieren und überwiegend im Inneren von Lebertumoren freisetzen können.
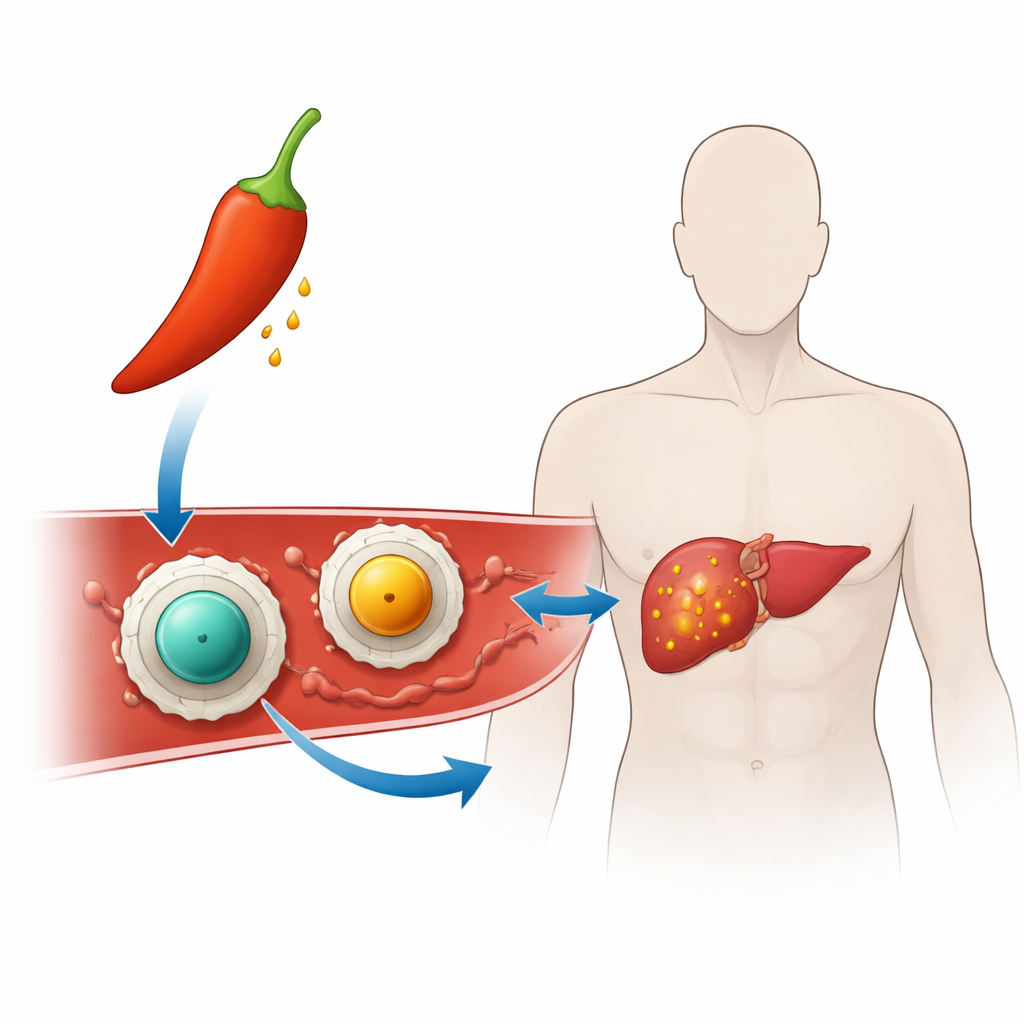
Vom Chili zur gezielten Therapie
Die Forschenden bauten „Nanotransporter“ – Partikel, die tausendfach kleiner sind als ein Sandkorn –, um Capsaicin zu Krebszellen zu bringen. Jeder Nanotransporter besitzt einen festen Kern aus einem magnetischen Mineral namens Ferrit (entweder Zinkferrit oder Manganferrit), umhüllt von einer dünnen Schicht Chitosan, einem zuckerähnlichen Stoff aus Schalentieren, der bereits in Medizin- und Lebensmittelprodukten verwendet wird. Diese Beschichtung erleichtert das Suspendieren in Wasser und fördert das Anhaften an Zelloberflächen und DNA, was für die Krebsbekämpfung wichtig ist. Indem Capsaicin in diese Chitosanhülle geladen wird, hoffte das Team, das Medikament stabil und verborgen zu halten, bis es die harsche Umgebung eines Tumors erreicht.
Intelligente Freisetzung unter Tumorbedingungen
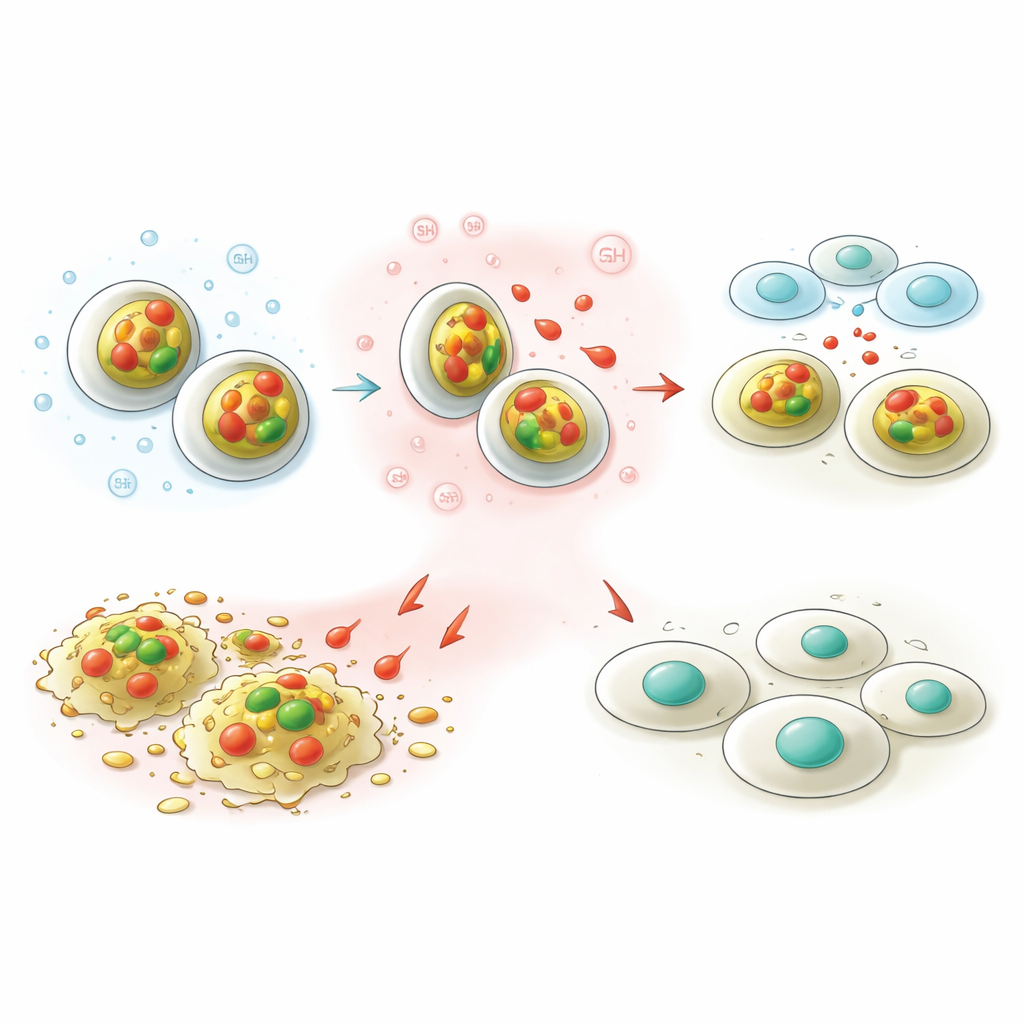
Ein Schlüsselmerkmal von Tumoren ist, dass sie tendenziell saurer sind und höhere Konzentrationen bestimmter Antioxidantien wie Glutathion aufweisen als gesundes Gewebe. Das Team entwarf seine Nanotransporter so, dass sie diese Bedingungen erkennen. In Labortests bei normalem Blut-pH traten in zwei Tagen weniger als zehn Prozent des gespeicherten Capsaicins aus, was darauf hindeutet, dass die Partikel ihre Fracht während der Zirkulation sicher transportieren würden. Unter tumorähnlichen Bedingungen – saurer und mit reichlich Glutathion – setzten die Partikel etwa ein Drittel ihres Capsaicins frei. Dieses „Ein–Aus“-Verhalten bedeutet, dass das Medikament eher in Krebszellen abgegeben wird als unterwegs, was den Nutzen erhöhen und Nebenwirkungen verringern könnte.
Wie Partikelbestandteile Sicherheit und Wirkung formen
Obwohl die beiden Nanotransporter aus der Ferne ähnlich wirkten, machte ihr innerer Kern einen entscheidenden Unterschied. Zinkbasierte Partikel waren tendenziell kleiner und banden Capsaicin fester, während manganbasierte Partikel poröser waren und das Medikament leichter freigaben. Beide Typen wiesen eine starke positive Oberflächenladung auf, die ihre Wechselwirkung mit den negativ geladenen Zell- und DNA-Oberflächen fördert. Tests mit menschlichem Blut zeigten nur sehr geringe Schädigungen der roten Blutkörperchen, und die leeren Partikel waren gegenüber normalen Lungenzellen schonend, was ihre grundlegende Sicherheit unterstützt. Mit Capsaicin beladen wurden beide Systeme gegen Leberkrebszellen wirksamer, doch die Manganvariante erzielte das beste Gleichgewicht: Sie schädigte Krebszellen stärker bei vergleichsweise geringerer Toxizität gegenüber normalen Zellen.
Mehr als Krebs: zusätzliche Schutzwirkungen
Die Nanotransporter leisteten mehr als nur die Lieferung von Capsaicin. In einigen Tests verlangsamten sie das Wachstum mehrerer pathogener Bakterien ebenso wirksam wie ein Standardantibiotikum und halfen, schädliche freie Radikale zu neutralisieren, die mit Entzündung und Gewebeschäden in Verbindung stehen. Sorgfältige lichtbasierte Messungen zeigten, dass Capsaicin, einmal in die Ferrit–Chitosan-Partikel gepackt, stärker und stabiler an DNA bindet. Schnellkinetische Experimente enthüllten einen zweistufigen Ablauf: Zuerst heftet sich die DNA an die positiv geladene Partikeloberfläche, danach ordnet sich der Komplex neu zu einer stärkeren, länger anhaltenden Verbindung. Diese verstärkten Wechselwirkungen erklären vermutlich, warum die beladenen Partikel stärkere antitumorale, antibakterielle und antioxidative Effekte zeigen als Capsaicin oder Ferritpartikel allein.
Was das für Patientinnen und Patienten bedeuten könnte
Bislang stammen diese Erkenntnisse aus Zellkulturversuchen, nicht aus Patientenstudien. Dennoch deuten sie darauf hin, dass sorgfältig konstruierte Nanotransporter ein scharfes Lebensmittelbestandteil in eine präzisere Krebswaffe verwandeln können. Durch die Wahl des richtigen Kernmaterials und einer passenden Hülle schufen die Forschenden winzige Pakete, die Capsaicin stabil halten, sicher im Blut transportieren und bevorzugt unter tumorähnlichen Bedingungen freisetzen, insbesondere in Leberkrebszellen. Unter den getesteten Designs boten manganbasierte Partikel die vielversprechendste Kombination aus gezielter Krebshemmung, geringer Schädigung normaler Zellen sowie zusätzlichen antibakteriellen und antioxidativen Vorteilen. Mit weiteren Tier- und Sicherheitsstudien könnten solche „intelligenten“ chili-inspirierten Partikel eines Tages zu schonenderen, fokussierteren Therapien gegen Leberkrebs und möglicherweise andere Erkrankungen beitragen.
Zitation: Bakr, E., Elshami, F.I., Okba, E.A. et al. Stimuli-responsive chitosan-coated ferrite nanocarriers for targeted capsaicin delivery and core-dependent HepG2-selective bioactivity. Sci Rep 16, 8957 (2026). https://doi.org/10.1038/s41598-026-40433-6
Schlüsselwörter: Capsaicin, Leberkrebs, Nanopartikel, gezielte Wirkstofffreisetzung, stimuli-responsive Träger