Clear Sky Science · de
Die Wirkung erhöhten Gewichtszufügens auf das Körpergewicht hängt teilweise von Piezo1 in osteoblastischen Zellen und TrkA-Signalgebung ab
Warum zusätzliches Gewicht bei der Bekämpfung von Fettleibigkeit helfen könnte
Die meisten von uns betrachten zusätzliches Gewicht als etwas, das es zu vermeiden gilt. Was aber, wenn wohl dosiertes Zusatzgewicht dem Körper tatsächlich helfen könnte, Fett zu verlieren? Diese Studie untersucht ein im Knochen verankertes Gewichtssensorsystem, das offenbar dem Gehirn signalisiert, wenn der Körper zu schwer ist, und es dazu veranlasst, Fett zu verbrennen. Durch das Aufschlüsseln dieses Systems auf zellulärer Ebene könnten sich Wege für Behandlungen eröffnen, die Fett reduzieren und gleichzeitig wertvolle Muskelmasse erhalten.
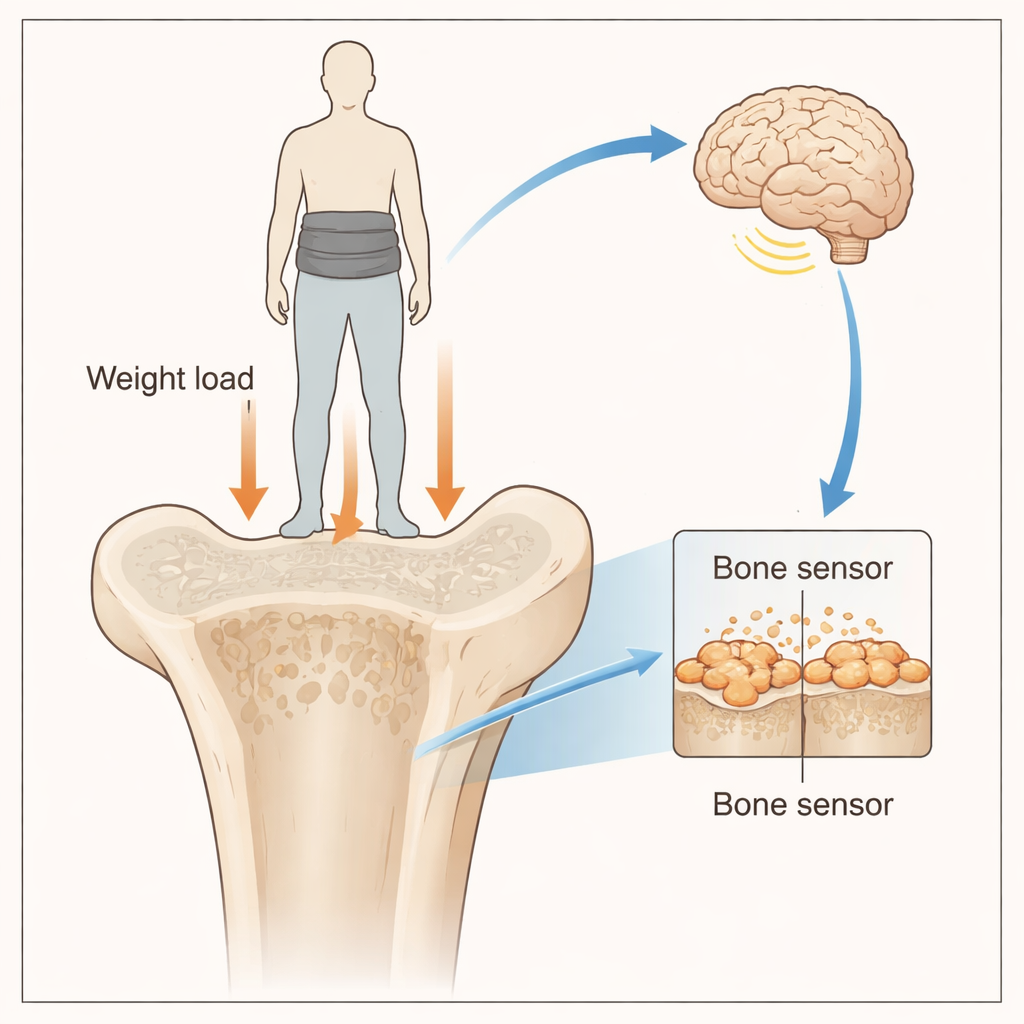
Eine versteckte Personenwaage in Ihren Knochen
Fettleibigkeit steht in Verbindung mit Diabetes, Herzkrankheiten und mehreren Krebsarten, und selbst die neuesten Gewichtsverlustmedikamente führen häufig zum Verlust von sowohl Fett als auch Muskel. Das ist ein ernstes Problem für Menschen mit „sarkopener Fettleibigkeit“, die bereits schwache Muskeln haben. Frühere Humanstudien zeigten, dass allein das Tragen einer Gewichtsweste über mehrere Wochen das Körperfett senken kann, ohne die Muskulatur zu reduzieren. Frühere Tierarbeiten veranlassten die Autoren zu der Hypothese, dass die Knochen der Beine eine Art interne „Gravitationswaage“ enthalten, die misst, wie schwer der Körper ist, und dazu beiträgt, Körperfett in Schach zu halten. Welche Moleküle dieses Sensoriksystem tatsächlich ausmachen, war jedoch unbekannt.
Prüfung des Knochen-Gewichtsensors bei adipösen Mäusen
Zur Untersuchung verwendeten die Forscher Mäuse, die durch eine fettreiche Ernährung adipös gemacht worden waren, und implantierten dann chirurgisch kleine Kapseln in den Bauchraum. In einer Gruppe war die Kapsel mit schwerem Material gefüllt, was das Körpergewicht um etwa 15 % erhöhte; in den Kontrollmäusen war die Kapsel nahezu gewichtslos. Nach der Operation zogen die Wissenschaftler das Gewicht der Kapsel von jeder Messung ab, um echte Änderungen des Körpergewichts verfolgen zu können. Am Ende des Experiments entnahmen sie außerdem ein spezifisches Fettdepot – retroperitoneales Weißfett – aus dem Bauchraum, um zu sehen, wie viel Fett die Mäuse verloren hatten.
Ein druckempfindlicher Kanal in Knochenzellen
Das Team konzentrierte sich zunächst auf Piezo1, einen Proteinkanals in Zellmembranen, der sich öffnet, wenn Zellen mechanisch gedehnt oder komprimiert werden. Mithilfe genetischer Manipulation löschten sie Piezo1 nur in frühen knochenbildenden Zellen (Osteoblasten-Linie), die einen Marker namens Runx2 exprimieren und hauptsächlich in den langen Knochen der Beine vorkommen. Sorgfältige mikroskopische Analysen bestätigten, dass Piezo1 in diesen Knochenzellen stark reduziert war, aber in der umgebenden Muskulatur weiterhin vorhanden blieb, was zeigt, dass die Deletion spezifisch war. Bei adipösen Mäusen mit normalem Piezo1 führte das zusätzliche Gewicht zu einem deutlichen Rückgang des Gesamtkörpergewichts und zu einer starken Verringerung des Bauchfetts. Im Gegensatz dazu zeigten Mäuse ohne Piezo1 in Knochenlinienzellen eine deutlich schwächere Reaktion: Ihr Körpergewicht und Bauchfett nahmen durch die zusätzliche Belastung kaum ab. Das deutet darauf hin, dass Piezo1 in Knochenzellen ein zentraler Bestandteil des Gewichtssensors ist.
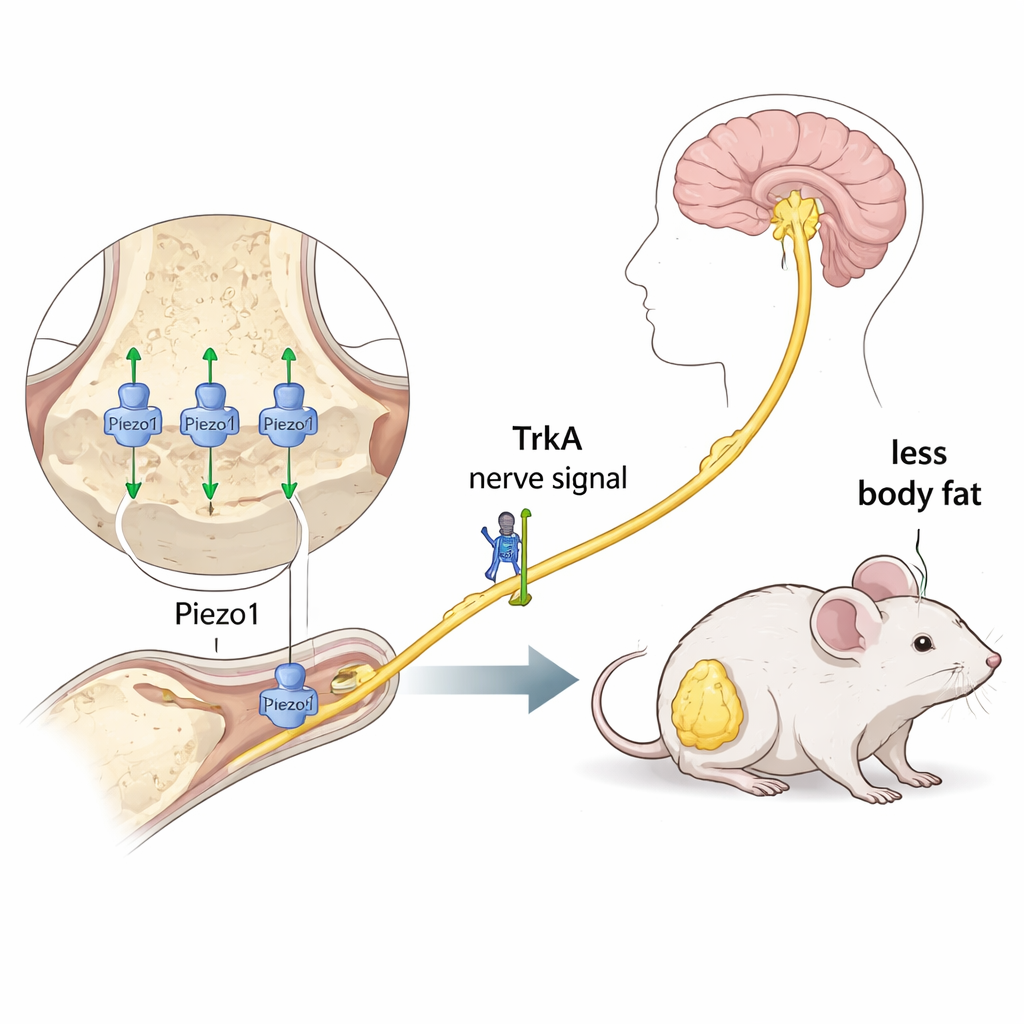
Nervensignale, die die Botschaft ans Gehirn tragen
Als Nächstes untersuchten die Wissenschaftler einen zweiten Akteur: TrkA, einen Rezeptor, der hauptsächlich auf bestimmten Nervenfasern vorkommt, die auf Nervenwachstumsfaktor (NGF) reagieren. TrkA unterstützt das Nervenwachstum und die Übertragung von Schmerz- und anderen Signalen. Mit einer speziellen Mauslinie konnte das Team die TrkA-Signalgebung im gesamten Körper durch Zugabe eines kleinen Moleküls, 1NM-PP1, ins Trinkwasser abschalten. Ein klassischer „Tail-Flick“-Schmerztest bestätigte, dass die TrkA-Signalgebung tatsächlich ausgeschaltet war: Behandelte Mäuse zeigten nach einem NGF-ähnlichen Medikament keine erhöhte Hitzeempfindlichkeit mehr. Als diese Mäuse einer erhöhten Gewichtslast ausgesetzt wurden, verloren Tiere mit normaler TrkA-Signalgebung signifikant an Körpergewicht und Bauchfett, während Mäuse mit blockierter TrkA-Signalgebung eine wesentlich kleinere und statistisch schwächere Reaktion zeigten. Interessanterweise löste das zusätzliche Gewicht kein offensichtliches Wachstum neuer Nervenfasern um den Knochen aus, was darauf hindeutet, dass vorhandene Nerven, eher als neu gesprossene, das Signal weiterleiten.
Was das für künftige Fettleibigkeitsbehandlungen bedeutet
In der Summe stützen die Ergebnisse ein Modell, wonach zusätzliches Körpergewicht – ob durch Fett oder eine hinzugefügte Last – die Bein Knochen komprimiert. Knochenlinienzellen erkennen diesen Druck über den Piezo1-Kanal und kommunizieren dann über TrkA-abhängige Nervenwege mit Gehirnzentren, die Appetit und Energieverbrauch regulieren. Das Gehirn hilft daraufhin, die Fettdepots zu reduzieren und gleichzeitig die Muskulatur zu schonen. Obwohl diese Arbeit an Mäusen durchgeführt wurde und chirurgische Implantate verwendet, trägt sie dazu bei zu erklären, warum etwas so Einfaches wie das Tragen einer Gewichtsweste beim Menschen Körperfett reduzieren kann. Langfristig könnte die gezielte Ansprache dieses Knochen–Nerv–Gehirn-Kreislaufs zu neuen Therapien führen, die bestehende Medikamente ergänzen, indem sie gezielt Fett reduzieren, ohne Muskelmasse zu opfern.
Zitation: Hägg, D., Li, L., Beeve, A.T. et al. The effect of increased weight loading on body weight is partly dependent on Piezo1 in osteoblast-lineage cells and TrkA signaling. Sci Rep 16, 7162 (2026). https://doi.org/10.1038/s41598-026-40431-8
Schlüsselwörter: Fettleibigkeit, Knochen-Mechanosensorik, Piezo1, TrkA-Signalgebung, Gewichtsbelastung