Clear Sky Science · de
MOV10, eine neuartige Immuntherapie und prognostischer Biomarker, trägt zur Gliomentwicklung bei, indem es die Autophagie reguliert
Warum diese Studie über Hirnkrebs wichtig ist
Das Glioblastom, eine besonders aggressive Form von Hirnkrebs, ist bekanntermaßen schwer zu behandeln. Die meisten Patienten überleben nur wenige Monate nach der Diagnose, selbst mit Operation, Strahlentherapie und Chemotherapie. Diese Studie richtet den Blick auf ein einzelnes Molekül namens MOV10, das in diesen Tumoren ungewöhnlich aktiv ist. Indem die Forschung zeigt, wie MOV10 Krebszellen beim Wachsen, bei der Umgehung des Immunsystems und beim Widerstehen des Zelltods unterstützt, identifizieren die Autoren ein neues potenzielles Ziel für effektivere Therapien — und einen möglichen Marker zur Vorhersage des Krankheitsverlaufs.
Ein verborgener Helfer tödlicher Hirntumoren
Das Team begann mit der Auswertung großer öffentlicher Krebsdatenbanken, die genetische und klinische Informationen von Hunderten von Menschen mit Gliom enthalten, einer übergeordneten Gruppe von Hirntumoren, zu der auch das Glioblastom gehört. Sie fanden heraus, dass MOV10, ein Protein, das an der Verarbeitung von RNA innerhalb der Zelle beteiligt ist, in Gliomgewebe stärker exprimiert wird als im normalen Gehirn. Patienten, deren Tumoren mehr MOV10 produzierten, lebten im Durchschnitt kürzer; dieser Zusammenhang blieb bestehen, selbst nachdem Alter, Tumorgrad und wichtige genetische Merkmale berücksichtigt wurden. Auf Basis dieser Faktoren entwickelten die Forscher ein mathematisches Modell, das zeigt, dass MOV10-Werte dazu beitragen können, die Überlebenschancen eines Patienten vorherzusagen, was darauf hindeutet, dass MOV10 als prognostischer Biomarker dienen könnte.
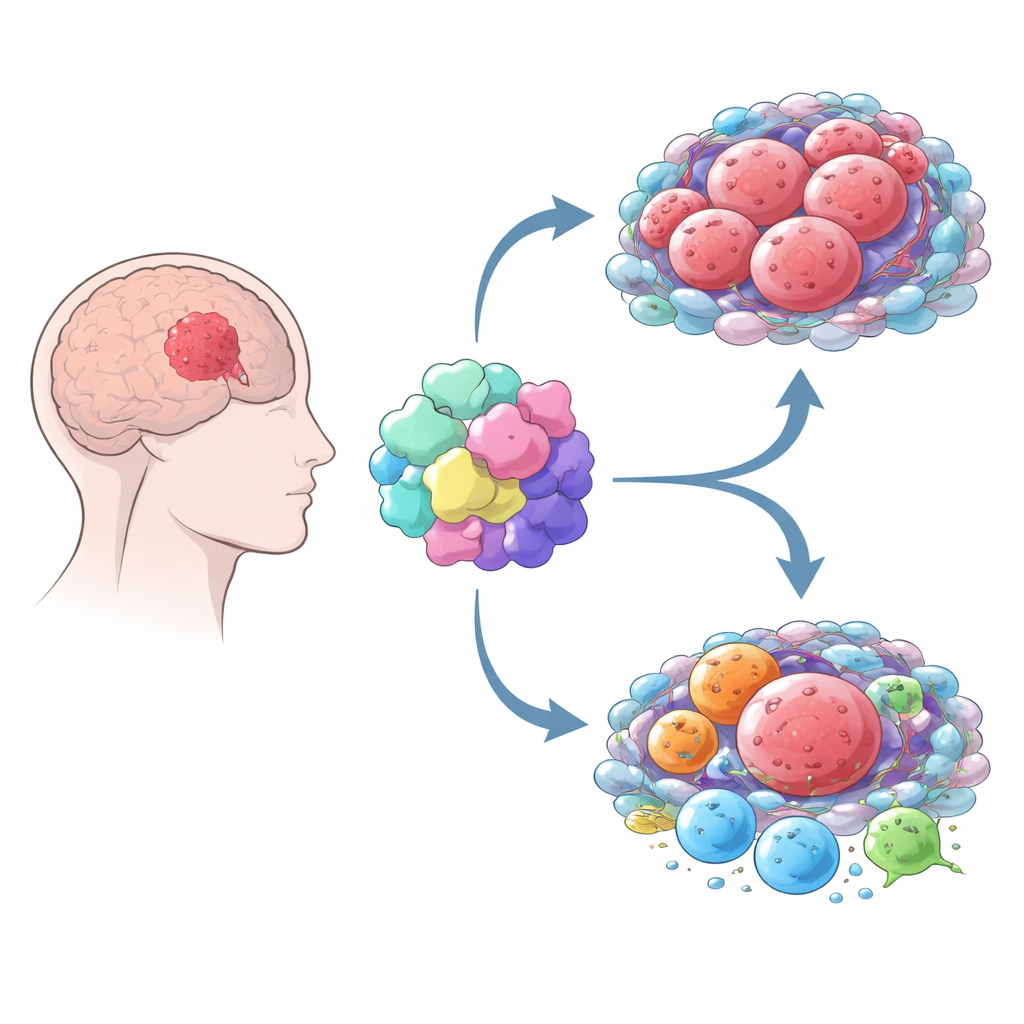
Wie MOV10 die Tumorumgebung umgestaltet
Krebs wächst nicht isoliert — er vereinnahmt die umgebende "Nachbarschaft" aus Immun- und Stütz-Zellen. Durch die Kombination mehrerer rechnerischer Methoden zeigten die Autoren, dass Gliome mit hoher MOV10-Expression von einer reicheren Mischung aus Immun- und Stromazellen umgeben sind als Tumoren mit niedriger MOV10-Expression. Das ist jedoch kein gesunder Immunangriff. Stattdessen enthalten Tumoren mit hoher MOV10-Konzentration mehr Makrophagen, insbesondere einen Subtyp, der häufig als M2 bezeichnet wird und das Tumorwachstum unterstützt sowie Immunantworten dämpft. Diese Tumoren zeigen außerdem stärkere Signaturen erschöpfter T‑Zellen und eine höhere Aktivität von Immunbremssystemen, die Ziele gängiger Immuntherapeutika wie PD-1 und CTLA-4 sind. Insgesamt deutet das Muster darauf hin, dass MOV10 mit einer immunsuppressiven Umgebung verbunden ist, in der die Abwehr des Körpers geschwächt ist.
Von Big Data zu Zellen im Labor
Um über Korrelationen hinauszugehen, untersuchten die Forscher MOV10 direkt in Patientenproben und kultivierten Zellen. Sie bestätigten, dass MOV10 in Gliomgewebe häufiger vorkommt als im normalen Gehirn und dass mehrere weitverbreitete Gliomzelllinien ebenfalls hohe Werte zeigen. Wenn sie kleine interferierende RNAs einsetzten, um MOV10 in im Labor gezüchteten Gliomzellen herunterzuregeln, teilten sich die Zellen langsamer, bildeten weniger Kolonien und verloren einen Teil ihrer Fähigkeit, sich zu bewegen und durch künstliche Membranen einzudringen. Proteine, die den Zellzyklus und die Invasion antreiben, gingen in ihrer Menge zurück, was die Idee stützt, dass MOV10 aktiv aggressives Verhalten fördert und kein bloßer Nebenfaktor ist.
Verknüpfung von MOV10 mit Immunzellen und Selbstreinigungswegen
Die Studie untersuchte außerdem, wie MOV10 mit zwei Schlüsselprozessen interagiert: dem Verhalten tumorassoziierter Makrophagen und dem zelleigenen "Selbstreinigungssystem" Autophagie. In menschlichen Tumorproben wurde MOV10 in denselben Bereichen wie M2‑ähnliche Makrophagen nachgewiesen. In einem Ko-Kultur-System wanderten weniger M2‑ähnliche Makrophagen durch eine Barriere auf Gliomzellen zu, die so verändert waren, dass sie weniger MOV10 produzierten; das deutet darauf hin, dass MOV10 in Tumorzellen diese pro-tumoralen Immunzellen anlockt oder unterstützt. Gleichzeitig verbanden genetische Analysen MOV10 mit mehreren Genen, die an der Autophagie beteiligt sind. Mit fluoreszenten Markern, die zelluläre Recycling-Strukturen sichtbar machen, zeigte das Team, dass das Herunterregeln von MOV10 die autophagische Aktivität in Gliomzellen erhöhte und mehr programmierten Zelltod auslöste. Veränderungen in charakteristischen Proteinen der Autophagie und Apoptose untermauerten diese Beobachtungen.
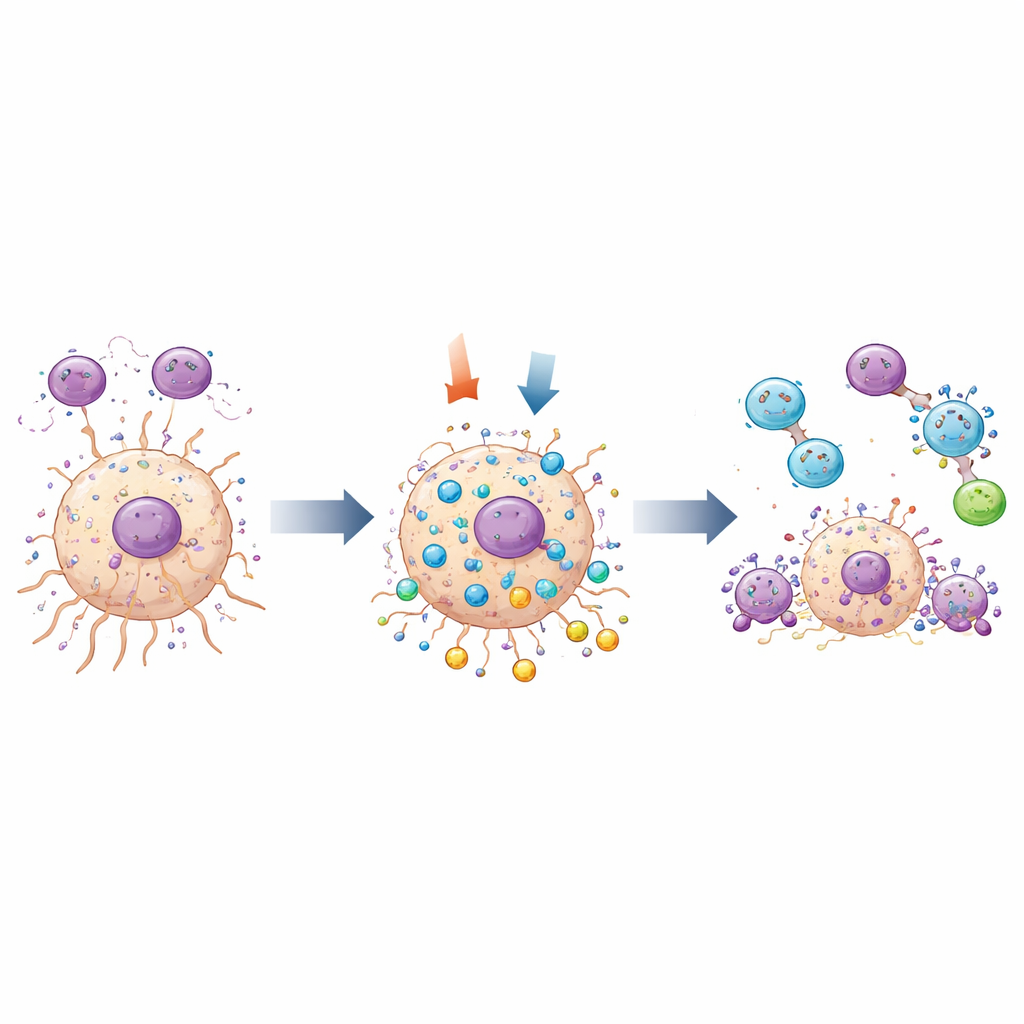
Was das für zukünftige Behandlungen bedeutet
In ihrer Gesamtsicht stellen die Ergebnisse MOV10 als vielseitigen Verbündeten des Glioms dar: Es fördert das Wachstum und die Invasion von Tumorzellen, trägt zur Bildung einer immunsuppressiven Mikroumgebung bei, die reich an tumorunterstützenden Makrophagen ist, und hält die zellinternen Selbstzerstörungs- und Recyclingmechanismen in Schach. Wird MOV10 ausgeschaltet, wachsen Gliomzellen weniger, sterben leichter und scheinen weniger in der Lage zu sein, schädliche Immunzelltypen anzuwerben. Für Nicht-Fachleute lautet die Kernbotschaft: MOV10 ist sowohl ein "Thermometer" als auch ein "Schalter": Sein Niveau im Tumor kann helfen, den Krankheitsverlauf vorherzusagen, und seine Hemmung könnte theoretisch Hirntumore anfälliger für Behandlungen machen. Obwohl weitere Tierstudien und letztlich klinische Studien nötig sind, sticht MOV10 nun als vielversprechendes Ziel im Kampf um bessere Therapien gegen einen der tödlichsten Hirntumoren hervor.
Zitation: Wang, F., Ruan, L., Yang, W. et al. MOV10, a novel immunotherapy and prognostic biomarker, contributes to glioma development by regulating autophagy. Sci Rep 16, 9501 (2026). https://doi.org/10.1038/s41598-026-40396-8
Schlüsselwörter: Glioblastom, Immuntherapie bei Hirntumoren, MOV10-Protein, Tumormikroumgebung, Autophagie und Apoptose