Clear Sky Science · de
Kupferkatalysierte Synthese von Thiazolderivaten aus Enaminonen, Aminen und CS₂
Warum diese neue Reaktion wichtig ist
Chemiker suchen ständig nach schnelleren, saubereren Wegen, um die komplexen Moleküle zu bauen, die moderne Arzneimittel und elektronische Materialien antreiben. Diese Studie stellt ein gestrafftes Rezept zur Herstellung einer Familie kleiner ringförmiger Verbindungen namens Thiazole vor, die in vielen Arzneimitteln und fortschrittlichen Materialien vorkommen. Indem drei einfache Zutaten in einem einzigen Reaktionsgefäß kombiniert werden und ein gebräuchliches Metall, Kupfer, die Umwandlung steuert, zeigen die Forschenden, wie sich grundlegende Bausteine mit minimalem Abfall und Aufwand in eine Vielzahl potenziell nützlicher Moleküle verwandeln lassen. 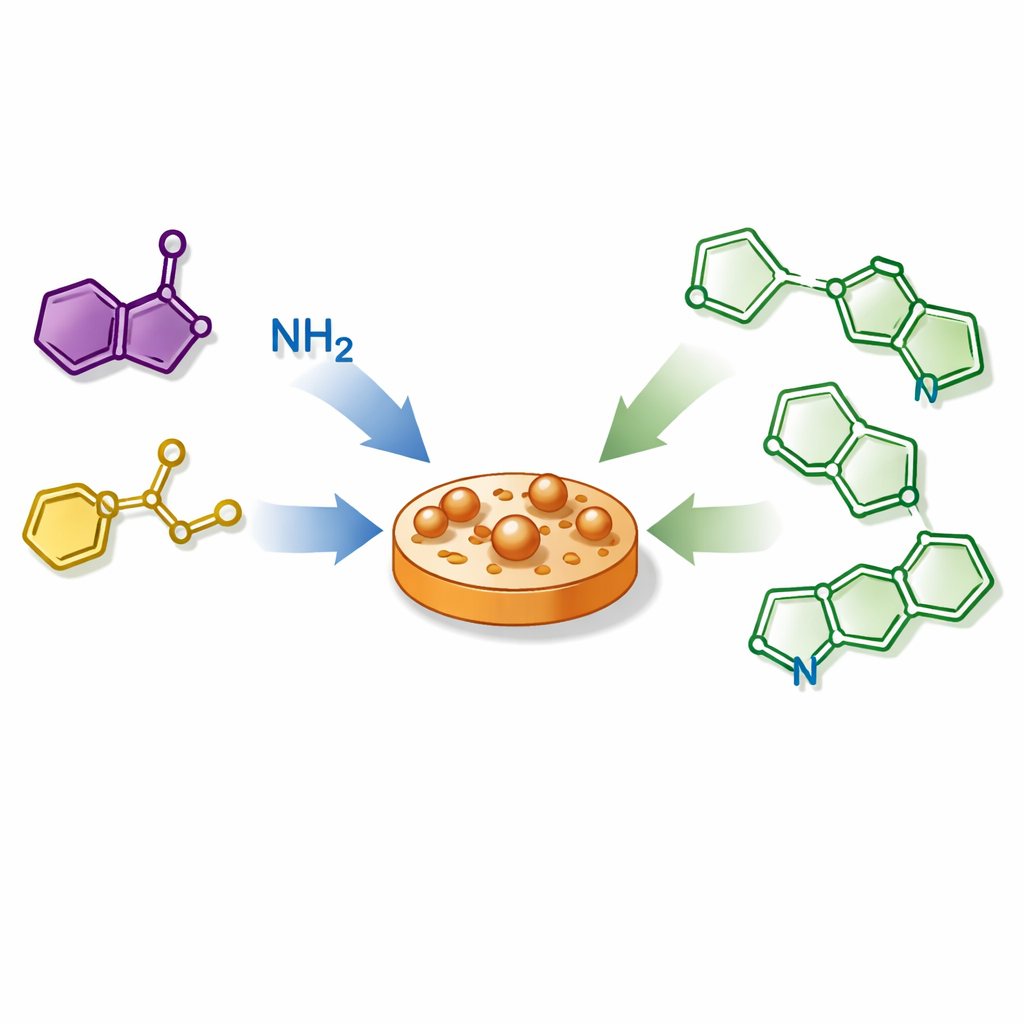
Kleine Ringe mit großer Wirkung
Thiazole sind kompakte Ringe, die sowohl Stickstoff- als auch Schwefelatome enthalten. Diese winzige Änderung in der Struktur verleiht ihnen ungewöhnliche elektrische und biologische Eigenschaften. Thiazol-basierte Verbindungen wurden als Antibiotika, entzündungshemmende Mittel, Wirkstoffkandidaten gegen Krebs und zur Behandlung von Erkrankungen von Diabetes bis hin zu neurologischen Störungen untersucht. Verwandte Strukturen treten auch in der organischen Elektronik auf, wo sie den Ladungstransport in Geräten wie Leuchtdioden und leitfähigen Polymeren unterstützen. Aufgrund dieser breiten Wirkung sind Chemiker daran interessiert, allgemeine, verlässliche Methoden zu haben, um verschiedene Thiazolstrukturen auf Abruf zu synthetisieren.
Grenzen älterer Syntheserouten
Traditionelle Methoden zum Aufbau von Thiazolen beginnen meist mit vorgefertigten schwefelreichen Bausteinen oder erfordern mehrere getrennte Schritte, spezialisierte Reagenzien oder harsche Bedingungen. Viele dieser Verfahren sind auf eine spezifische Unterklasse, die Benzothiazole, abgestimmt und weniger flexibel bei der Herstellung anderer Ringvarianten. Einige Ansätze benötigen zudem zusätzliche Additive, Liganden oder Oxidationsmittel, was Kosten erhöht und mehr chemischen Abfall erzeugt. Diese Einschränkungen erschweren es, schnell neue Thiazol-Designs für die Arzneimittelentwicklung oder Materialscreenings zu erkunden.
Ein-Etappen-Aufbau unter Kupferleitung
Die Autoren stellen eine andere Strategie vor, die auf drei leicht verfügbaren Bausteinen beruht: Enaminone (einfache kohlenstoffbasierte Fragmente mit eingebauter Reaktivität), gebräuchliche Amine und Kohlenstoffdisulfid, eine preiswerte Flüssigkeit, die hier sowohl Schwefel als auch Kohlenstoff liefert. Unter dem Einfluss eines Kupfersalzes und einer basischen Additive in einem einzigen Reaktionsgefäß verbinden sich diese Zutaten und falten sich zum gewünschten Thiazolring. Der Prozess benötigt keine speziellen Hilfsmoleküle und keinen Zusatzoxidator; gewöhnlicher Sauerstoff aus der Luft unterstützt die Regeneration des Kupferkatalysators. Durch systematische Tests von Lösungsmitteln, Temperaturen, Basen und Metallsalzen identifiziert das Team Bedingungen, die die Ausgangsmaterialien effizient in Thiazole überführen, oft in hoher Ausbeute. 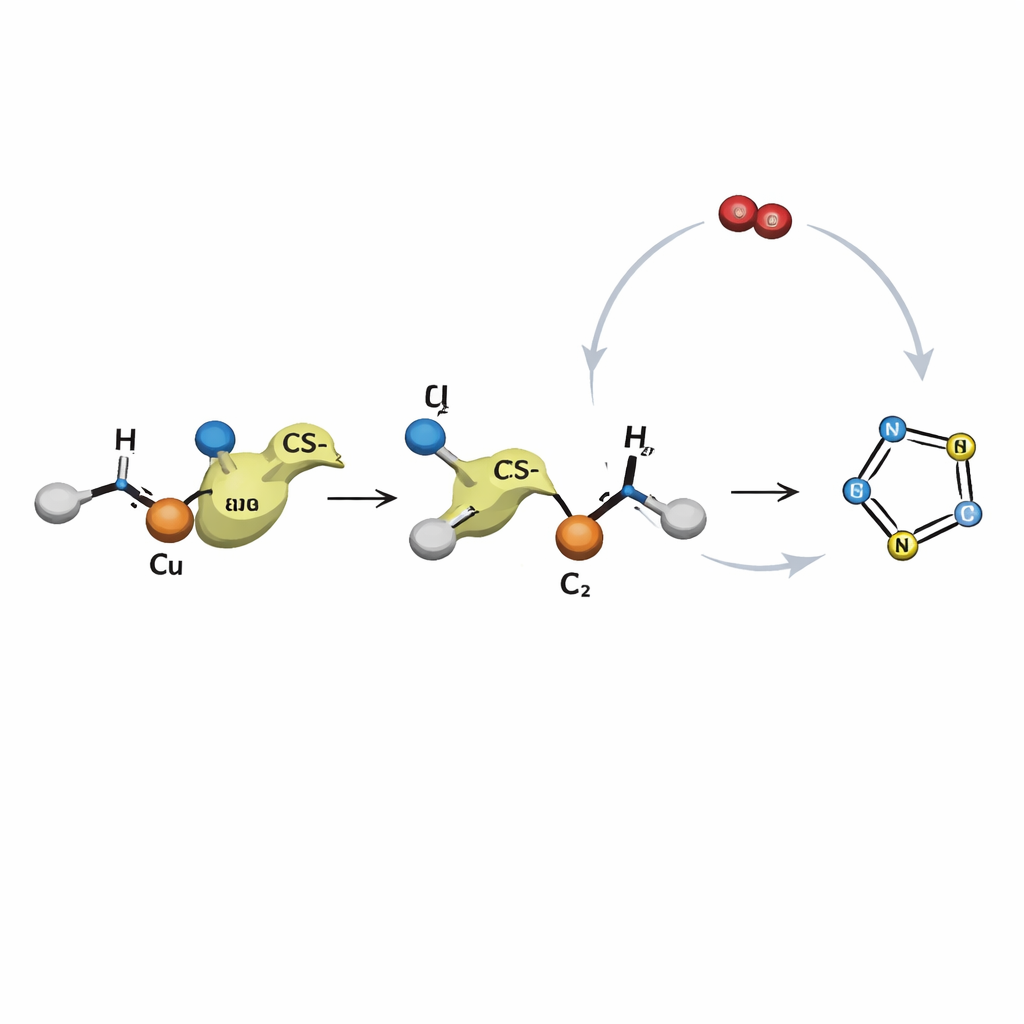
Große Vielfalt aus einfachen Bausteinen
Sobald die Bedingungen optimiert waren, untersuchten die Forschenden die Allgemeingültigkeit der Reaktion, indem sie viele verschiedene Amine und Enaminone einsetzten. Eine breite Palette sekundärer Amine, einschließlich flexibler kettenförmiger und starrer ringförmiger Beispiele, lieferte die gewünschten Thiazole in guten bis ausgezeichneten Ausbeuten. Primäre Amine funktionierten ebenfalls, wenn auch meist weniger effizient. Die Reaktion tolerierte verschiedene dekorative Gruppen an aromatischen Ringen, und selbst sperrigere „ortho“-Substituenten zeigten kaum negative Effekte, was darauf hindeutet, dass Platzmangel in der Nähe der reaktiven Stelle kein großes Hindernis darstellt. Einige stark elektronenziehende oder stickstoffreiche Amine reagierten jedoch nicht, vermutlich weil sie den entscheidenden schwefelhaltigen Partner für den Ringschluss abschwächten.
Wie der Kupferkatalysator seine Arbeit verrichtet
Um zu untersuchen, wie diese Umwandlung abläuft, führten die Autoren Kontrollversuche durch und schlugen einen schrittweisen Mechanismus vor. Zunächst verbinden sich das Amin und das Kohlenstoffdisulfid unter basischen Bedingungen zu einem schwefelreichen Fragment. Gleichzeitig bindet das Enaminon an Kupfer, das es für die Reaktion aktiviert. Das Schwefel–Stickstoff-Fragment greift dann diesen aktivierten Partner an und bildet neue Kohlenstoff–Schwefel- und Kohlenstoff–Stickstoff-Bindungen. Diese Verbindung reorganisiert sich zu einem teilgeschlossenen Ring, der sich schließt, wobei Schwefelwasserstoff ausgestoßen und der finale Thiazolkern gebildet wird. Kupfer wechselt während dieser Sequenz zwischen zwei Oxidationsstufen, und Sauerstoff aus der Luft hilft, es wieder in die aktive Form zu überführen, sodass der Katalysator im selben Reaktionsgemisch vielfach wiederverwendet werden kann.
Ein geradliniger Weg zu nützlichen Molekülen
Insgesamt liefert die Arbeit eine praktische und flexible Route zur Herstellung von Thiazolderivaten aus einfachen, leicht handhabbaren Ausgangsmaterialien. Da die Reaktion in einem Gefäß ohne zusätzliche Liganden oder Oxidantien abläuft, vereinfacht sie Laborabläufe und reduziert chemischen Abfall. Die Möglichkeit, viele verschiedene Thiazolstrukturen durch den Austausch unterschiedlicher Amine und Enaminone zu erzeugen, macht diese Methode zu einem wertvollen Werkzeug für Chemiker, die neue Arzneimittel oder funktionelle Materialien auf Basis dieses wichtigen Ringsystems entwerfen.
Zitation: Arman, A., Nowrouzi, N. & Abbasi, M. Copper catalyzed synthesis of thiazole derivatives from enaminones, amines and CS₂. Sci Rep 16, 9184 (2026). https://doi.org/10.1038/s41598-026-40393-x
Schlüsselwörter: Thiazol-Synthese, Kupferkatalyse, heterocyclische Chemie, Enaminone, Schwefeldisulfid