Clear Sky Science · de
Alternatives Spleißen und differentielle Genexpression während Veränderungen der Endometriumrezeptivität bei Patientinnen mit wiederholtem Implantationsversagen
Warum sich einige Embryonen nicht einnisten
Viele Paare, die eine In-vitro-Fertilisation durchlaufen, stehen vor einem frustrierenden Rätsel: Selbst wenn hochwertige Embryonen transferiert werden, kann es zu keiner Schwangerschaft kommen. Diese Studie untersucht die Gebärmutterschleimhaut — das Endometrium — genau, um zu verstehen, warum einige Frauen wiederholt fehlgeschlagene Einnistungsversuche erleben. Durch die Analyse, wie Gene ein- und ausgeschaltet werden, wie ihre Botschaften geschnitten und umgeordnet werden und wie sich Immunzellen während des kurzen Fensters verhalten, in dem die Gebärmutter bereit ist, einen Embryo aufzunehmen, deckt die Forschung neue molekulare Hinweise auf, die eines Tages präzisere Tests und Behandlungen ermöglichen könnten.
Das kurze Willkommensfenster der Gebärmutter
Die Einnistung kann nur in einem kurzen Abschnitt jedes Zyklus stattfinden, wenn die Gebärmutterschleimhaut "rezeptiv" wird. Die Forschenden verglichen Gewebeproben von 90 fruchtbaren Frauen und 73 Frauen mit wiederholtem Implantationsversagen, alle entnommen zu drei Schlüsselzeitpunkten: kurz bevor die Schleimhaut rezeptiv wird, während des rezeptiven Fensters und kurz nachdem es geschlossen ist. Mithilfe hochdurchsatzfähiger RNA-Sequenzierung maßen sie, welche Gene aktiv waren und wie ihre RNA-Botschaften verarbeitet wurden. Dieses Design ermöglichte es ihnen, nachzuverfolgen, wie sich eine gesunde Schleimhaut auf einen Embryo vorbereitet und wie diese Vorbereitung bei Frauen fehlgeht, die trotz guter Embryonen wiederholt nicht einnisten. 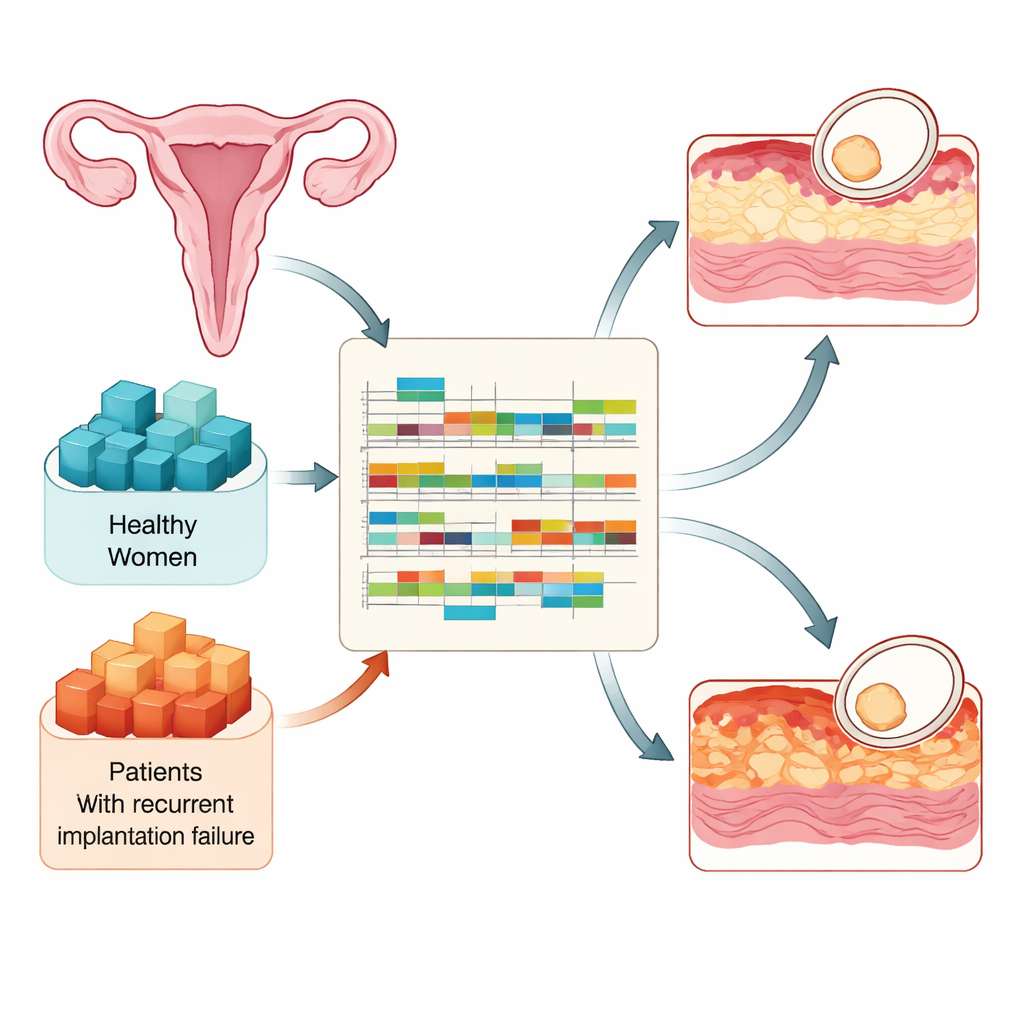
Genbotschaften werden geschnitten und umgeordnet
Über das reine Zählen der Genaktivität hinaus konzentrierte sich das Team auf alternatives Spleißen — den Prozess, bei dem ein einzelnes Gen in unterschiedliche Nachrichtenvarianten geschnitten werden kann, was zu verschiedenen Proteinformen führt. Sie fanden über eine Million Spleißereignisse in den Vergleichen, wobei zwei Typen — komplettes Überspringen von Segmenten und die Wahl zwischen sich gegenseitig ausschließenden Segmenten — besonders häufig waren. Betrachtete man nur Änderungen, die sowohl häufig als auch statistisch robust waren, zeigten sich Hunderte bis Tausende von Spleißverschiebungen, als die Schleimhaut von der nicht-rezeptiven zur rezeptiven Phase wechselte, insbesondere vom frühen (prärezeptiven) Stadium in das Einnistungsfenster. Viele dieser Veränderungen traten auf, obwohl die Gesamtmenge des jeweiligen Gens gleich blieb, was bedeutet, dass sich die Form des Proteins änderte, ohne dass sich die Gesamtgenaktivität veränderte.
Zellen haften, verändern Form und kommunizieren mit dem Immunsystem
Gene, die von verändertem Spleißen und von Aktivitätsänderungen betroffen waren, spielten starke Rollen bei Zellhaftung, bei der Umgestaltung des zellulären Gerüsts und bei der Übermittlung und dem Empfang von Immunbotenstoffen. Diese Funktionen sind entscheidend, wenn sich die Gebärmutterschleimhaut von einer einfachen Barriere in eine Oberfläche verwandelt, die einen Embryo willkommen heißen und verankern sowie Blutgefäße umgestalten kann. Sowohl bei fruchtbaren Frauen als auch bei denen mit Implantationsversagen war die rezeptive Phase durch ausgeprägte Umgestaltungen in diesen Signalwegen gekennzeichnet, doch Frauen mit wiederholtem Versagen zeigten tendenziell häufigere oder anders geformte Spleißänderungen. Einige der beteiligten Gene wurden bereits als Marker des idealen Einnistungsfensters vorgeschlagen, was die Vorstellung stützt, dass nicht nur die Genaktivität, sondern die genaue Form ihrer Produkte mitbestimmt, wann die Schleimhaut wirklich bereit ist.
Immunzellen und ein wichtiger Spleißregulator
Das Team schätzte außerdem die Arten der im Gewebe vorhandenen Immunzellen anhand derselben RNA-Daten. Bei Frauen mit Implantationsversagen zeigten sich in der rezeptiven Phase weniger zytotoxische T-Zellen und ruhende natürliche Killerzellen, jedoch mehr Monozyten und bestimmte Makrophagen im Vergleich zu früheren Phasen. Später, nachdem das Fenster geschlossen war, verschoben sich die Muster erneut, mit Veränderungen bei aktivierten natürlichen Killerzellen und Makrophagenuntertypen. Mehrere dieser Veränderungen von Immunzelltypen korrelierten eng mit bestimmten Spleißereignissen, was darauf hindeutet, dass die Umgestaltung von Genbotschaften und das immunologische Gleichgewicht miteinander verknüpft sind. Unter den Proteinen, die das Spleißen steuern, hob sich ein Faktor namens KHDRBS3 als zentrales Netzwerkglied hervor, das mit vielen der veränderten Ereignisse verbunden war und dessen Spiegel beim Übergang zur rezeptiven Phase sowohl bei fruchtbaren als auch betroffenen Frauen konsistent abnahm. Das spricht dafür, dass er am Anstoßen der Spleißmuster beteiligt sein könnte, die mit dem Öffnen des Einnistungsfensters einhergehen. 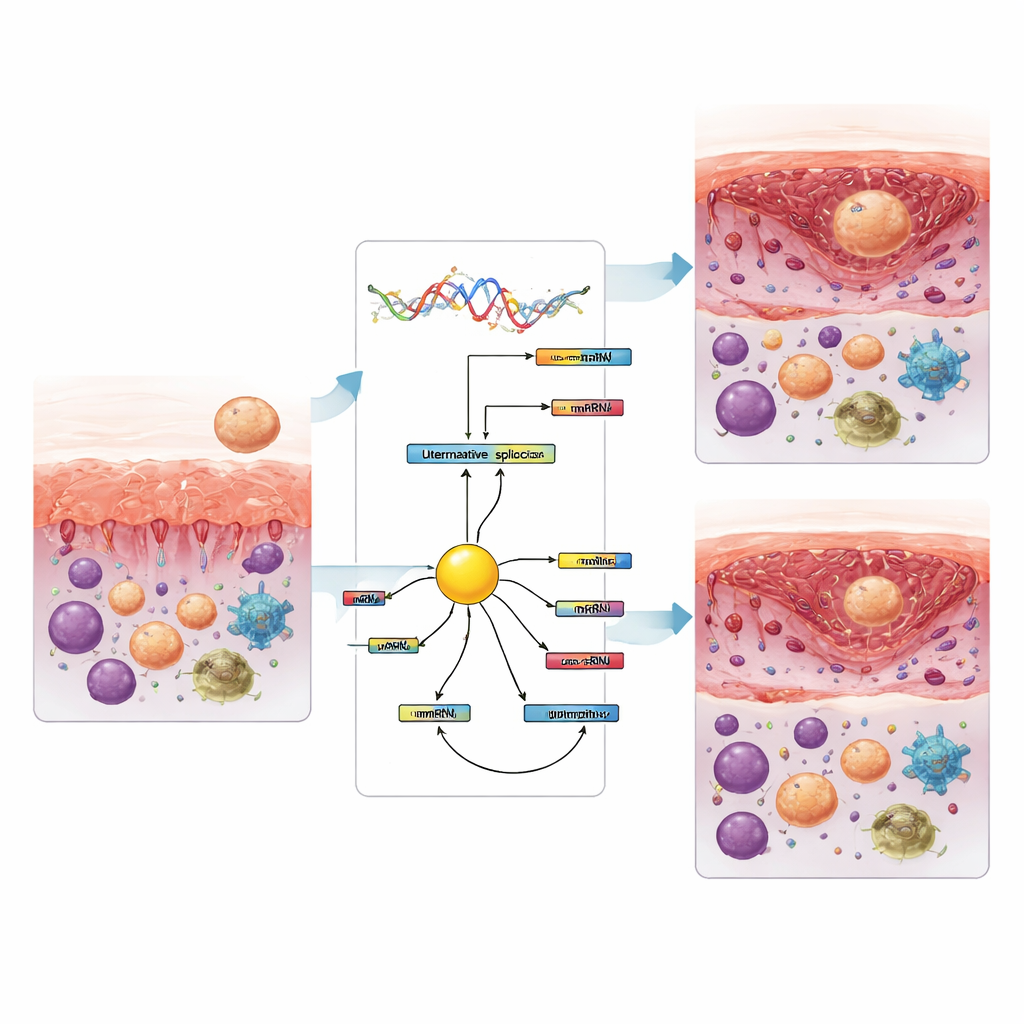
Hinweise auf künftige Tests und Behandlungen
Um diese molekularen Muster in mögliche Therapien zu überführen, prüften die Forschenden, ob bereits existierende Kleinmolekülmedikamente die abnormalen Spleißsignaturen, die sie beobachtet hatten, entgegenwirken könnten. Durch Abgleich ihrer Genlisten mit großen Datenbanken zu Arzneimittelantworten identifizierten sie mehrere zugelassene oder experimentelle Verbindungen, die Gene beeinflussen, die mit der Einnistung verbunden sind, darunter Wirkstoffe, die Immunreaktionen oder hormonbezogene Pfade modulieren. Zwar sind diese Verbindungen in diesem Kontext noch keineswegs klinisch einsetzbar, sie liefern jedoch eine Ausgangskarte für Laboruntersuchungen.
Was das für Patientinnen bedeutet
Insgesamt zeigt die Studie, dass Implantationsversagen nicht einfach eine Frage der „falschen“ Gene ist, sondern davon abhängt, wie diese Gene in unterschiedliche Botschaften geschnitten werden und wie das immunologische Umfeld der Gebärmutter im Zeitverlauf abgestimmt ist. Die Arbeit hebt KHDRBS3 und verwandte Faktoren als vielversprechende Regulatoren dieses Prozesses hervor und zeigt koordinierte Verschiebungen bei Immunzellen, die einen Embryo beim Einnisten unterstützen oder behindern können. Langfristig könnten solche Erkenntnisse zu präziseren Tests führen, die das tatsächliche Timing und die Qualität des rezeptiven Fensters einer Frau bestimmen, sowie zu gezielten Behandlungen, die die Genbotschaften oder das immunologische Gleichgewicht vorsichtig anpassen, um Embryonen bessere Chancen zur Einnistung zu geben.
Zitation: Wang, Ml., Lu, Bj., Lu, X. et al. Alternative splicing and differential gene expression during changes in endometrial receptivity in patients with recurrent implantation failure. Sci Rep 16, 9754 (2026). https://doi.org/10.1038/s41598-026-40386-w
Schlüsselwörter: Endometriumrezeptivität, wiederholtes Implantationsversagen, alternatives Spleißen, uterine Immunzellen, assistierte Reproduktion