Clear Sky Science · de
Trabectedin plus CD13-targetiertes Gewebefaktor-Protein tTF-NGR gegen fortgeschrittenes rezidivierendes oder refraktäres Weichteilsarkom: translationale Daten, klinische Sicherheit und Wirksamkeit
Warum diese Forschung wichtig ist
Menschen mit fortgeschrittenen Weichteilsarkomen – seltenen Krebserkrankungen, die in Muskeln, Fett oder anderem Stützgewebe entstehen – haben häufig nur begrenzte effektive Behandlungsoptionen. Diese Studie untersucht eine neue zweistufige Wirkstoffstrategie, die darauf abzielt, ein bereits eingesetztes Chemotherapeutikum im Tumor einzuschließen und gleichzeitig die Blutversorgung des Tumors zu unterbinden, in der Hoffnung, die Krankheitskontrolle zu verbessern und gleichzeitig die Nebenwirkungen beherrschbar zu halten.
Ein seltener Krebs, der bessere Optionen braucht
Weichteilsarkome machen nur etwa 1 % der Krebserkrankungen bei Erwachsenen aus, sind jedoch oft aggressiv, sobald sie metastasieren oder chirurgisch nicht mehr entfernt werden können. Standardchemotherapie kann ihr Wachstum verlangsamen, doch die Prognose bei fortgeschrittener Erkrankung bleibt schlecht. Trabectedin ist eines der wichtigsten Mittel, das nach Versagen der Erstlinientherapie eingesetzt wird. Es wirkt, indem es die DNA von Krebszellen schädigt und zudem Zellen im Tumormikromilieu beeinflusst. Dennoch wachsen viele Tumoren schließlich wieder, was die Suche nach Wegen befeuert, seine Wirkung zu verstärken, ohne die Belastung für die Patienten deutlich zu erhöhen.
Eine zweistufige „Falle“ für den Tumor
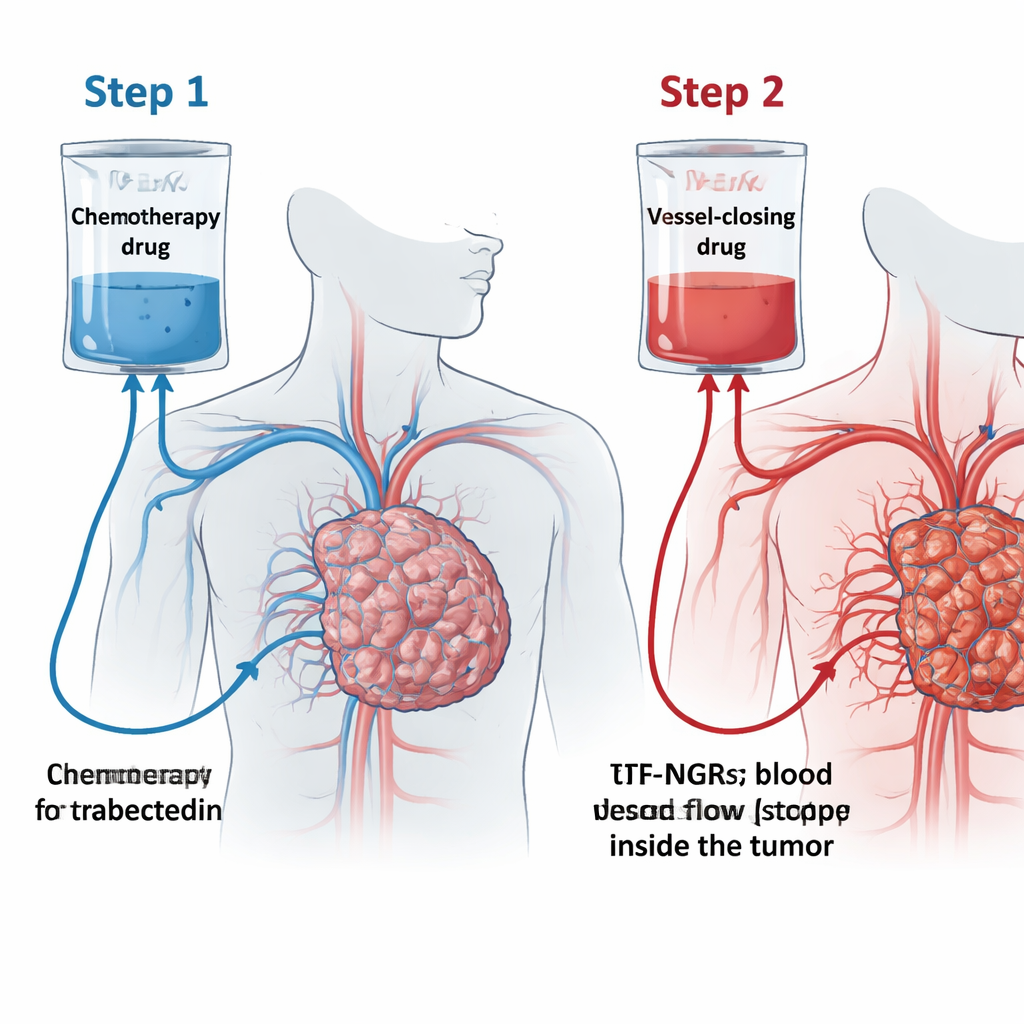
Das Team prüfte ein Konzept, das sie „trabectedin trap“ (TRABTRAP) nennen. Zuerst erhalten Patienten Trabectedin als 24‑stündige Infusion. An den ein bis zwei oder drei folgenden Tagen erhalten sie ein zweites Präparat, tTF‑NGR. Dieses gentechnisch veränderte Protein zielt auf einen Marker namens CD13, der vor allem an den Blutgefäßen liegt, die Tumore versorgen. Wenn tTF‑NGR an diese Gefäße bindet, löst es eine lokale Gerinnung aus und blockiert so den Blutfluss, wodurch Tumorbereiche absterben. Die Idee ist, dass Trabectedin zuerst in den Tumor eindringt und tTF‑NGR dann die Ausgänge versiegelt, indem es die feinen Gefäße verschließt, das Medikament dort einschließt, wo es am meisten wirkt, und die Effekte beider Therapien verstärkt.
Vom Labor zur frühen Patientenprüfung
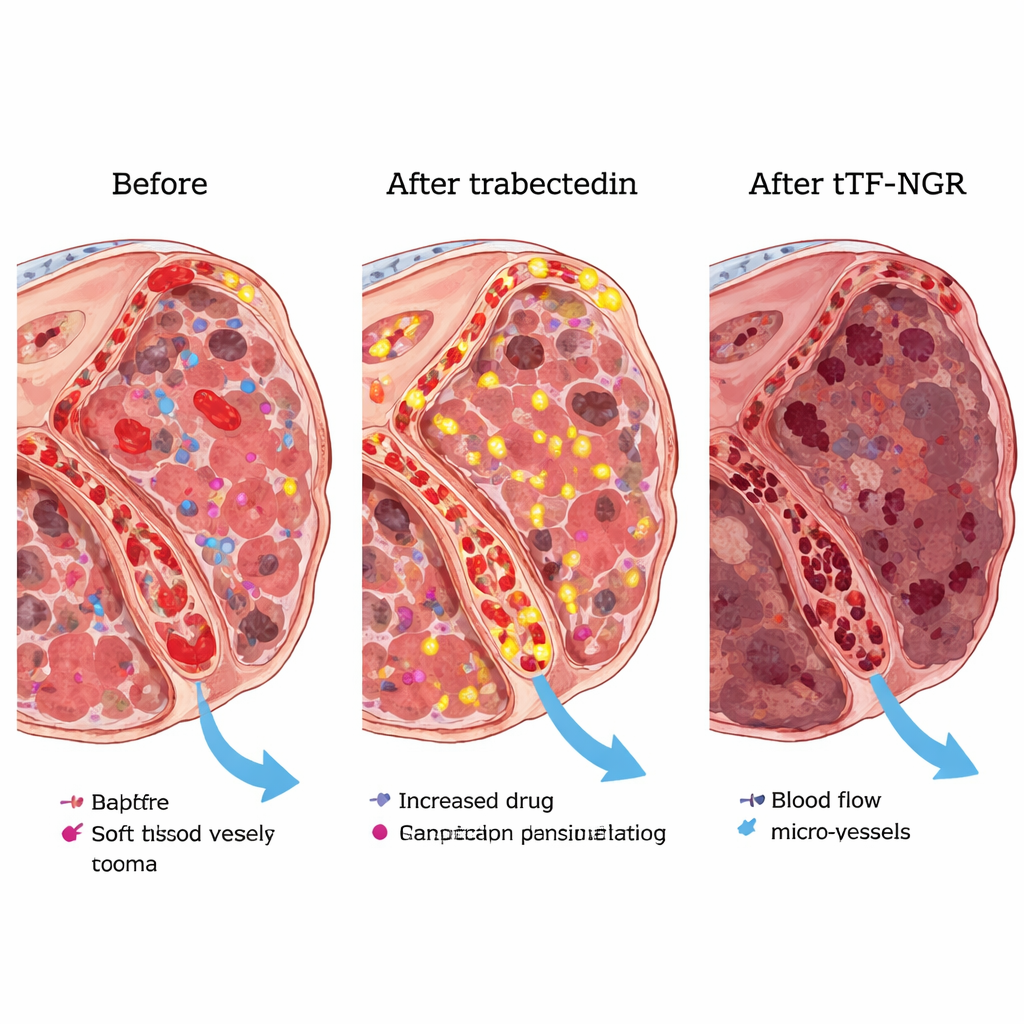
In Laborversuchen zeigten die Forschenden, dass Trabectedin dazu führt, dass Gefäßzellen und Sarkomzellen vermehrt ein bestimmtes Lipidmolekül auf ihrer Oberfläche präsentieren, das die Gerinnung begünstigt. Diese Veränderung machte tTF‑NGR wirksamer darin, auf diesen Zellen lokale Gerinnsel zu induzieren, genau das, was nötig ist, um Tumorgefäße zu verschließen. In Mäusen mit humanen Sarkomtransplantaten schrumpfte die Tumormasse nach der Abfolge von Trabectedin gefolgt von tTF‑NGR stärker als unter einer der Einzeltherapien. Da die Tumoren bei der Kombination so weitgehend zerstört wurden, ließ sich die zusätzlich eingeschlossene Menge an Trabectedin nicht zuverlässig messen, doch die stärkere Tumorkontrolle stützte das grundlegende Konzept der „Falle“.
Die sichere Dosis bei echten Patienten finden
Kern dieses Artikels ist die Sicherheits‑„Run‑in“-Phase der TRABTRAP‑Studie bei 19 Personen mit fortgeschrittenen, stark vorbehandelten Weichteilsarkomen. Alle Patienten erhielten die Standarddosis von Trabectedin. Das zweite Präparat, tTF‑NGR, wurde zunächst in der höchsten bisher als verträglich bekannten Monotherapie‑Dosis begonnen und bei Auftreten schwerer Nebenwirkungen schrittweise reduziert. Bei höheren Dosen traten bei einigen Patienten relevante kardiale oder thrombotische Komplikationen auf, wie stille Myokardschäden im Blutbild, kleine Lungenembolien oder tiefe Beinvenenthrombosen. Diese Ereignisse waren unter Behandlung und Absetzen oder Dosisreduktion von tTF‑NGR reversibel, wiesen jedoch auf die Notwendigkeit niedrigerer Dosen hin. Bei 0,5 mg/m² tTF‑NGR, gegeben an zwei Tagen nach Trabectedin, beendeten sechs Patienten mindestens zwei Zyklen ohne dosislimitierende Toxizitäten; einige setzten die Behandlung bis zu 14 Zyklen fort.
Frühe Hinweise auf Nutzen und Wirkstoffwechsel
Auch wenn dieser Studienabschnitt zu klein war, um Wirksamkeit zweifelsfrei zu belegen, waren die Ergebnisse vielversprechend. Unter den 19 Patienten hatten die meisten zumindest vorübergehend eine Krankheitskontrolle, und zwei zeigten klare partielle Tumorverkleinerungen. Bei Patientinnen und Patienten mit Liposarkom oder Leiomyosarkom – zwei für Trabectedin typische Subtypen – hatten bei der ersten größeren Kontrolluntersuchung fast zwei Drittel stabile Erkrankung oder partielle Anspreche. Detaillierte MRT‑Aufnahmen bei einem Patienten bestätigten, dass tTF‑NGR in der gewählten Dosis selektiv den Blutfluss innerhalb von Tumorherden reduzieren kann. Blutuntersuchungen zeigten außerdem, dass tTF‑NGR, wenn es nach Trabectedin gegeben wurde, länger im Kreislauf verbleibt und aktiver zu sein schien als als Monotherapie, was erklärt, warum die sichere Dosis in der Kombination niedriger ist als bei alleiniger Gabe.
Was das für Patienten bedeutet
Für Menschen mit fortgeschrittenem Weichteilsarkom stellt TRABTRAP einen sorgfältig konzipierten Versuch dar, mehr aus einem bestehenden Chemotherapeutikum herauszuholen, indem es mit einem gefäßverengenden Wirkstoff kombiniert wird, der die Blutversorgung des Tumors gezielt angreift. Die Sicherheits‑Run‑in‑Phase zeigt, dass diese Kombination in angepassten Dosen wiederholt verabreicht werden kann, mit Nebenwirkungen, die zwar bedeutend, aber unter engmaschiger Überwachung in der Regel beherrschbar und reversibel sind. Ob die Kombination das Leben verlängert oder Tumoren zuverlässig verkleinert, lässt sich derzeit noch nicht sagen; die vielversprechende frühe Krankheitskontrolle und die deutlichen Effekte auf den Tumorblutfluss rechtfertigen jedoch die Fortführung in eine größere, randomisierte Studie. Sollten künftige Ergebnisse positiv ausfallen, könnte dieser zweistufige Ansatz einen neuen Weg in der Behandlung von Sarkomen eröffnen und ähnliche Strategien für andere schwer behandelbare Krebsarten anregen.
Zitation: Hessling, K., Brand, C., Schwöppe, C. et al. Trabectedin plus CD13-targeted tissue factor tTF-NGR against advanced relapsed or refractory soft tissue sarcoma: translational data, clinical safety and efficacy. Sci Rep 16, 7389 (2026). https://doi.org/10.1038/s41598-026-40362-4
Schlüsselwörter: Weichteilsarkom, Trabectedin, Tumorblutgefäße, zielgerichtete Koagulationstherapie, Kombinationschemotherapie