Clear Sky Science · de
Vergleich angeborener und adaptiver Immunreaktionen auf Gelenkverletzungen während des Beginns und der Progression der posttraumatischen Arthrose in gängigen Mausmodellen
Warum Gelenkverletzungen nicht immer gleich enden
Viele Menschen, die ein Knieband reißen oder ihren Meniskus schädigen, entwickeln eine schmerzhafte, lang anhaltende Arthrose – andere mit sehr ähnlichen Verletzungen hingegen nicht. Diese Studie an Mäusen stellt eine einfache, aber wichtige Frage: Über die mechanische Schädigung hinaus: Was geschieht im Gelenk, das einige Verletzungen in eine chronische Arthritis kippen lässt, während andere verheilen? Indem die Forschenden Immunzellen über die Zeit nach verschiedenen Knieverletzungen verfolgen, zeigen sie, dass die körpereigenen Entzündungsabwehrkräfte vorhersagen können — und möglicherweise antreiben, — ob sich eine posttraumatische Arthrose entwickelt.
Verschiedene Knieverletzungen, verschiedene Langzeitverläufe
Das Team verwendete mehrere etablierte Mausmodelle, die gängige menschliche Knieverletzungen nachahmen. Einige Eingriffe beschädigten das vordere Kreuzband (ACL), das das Knie stabilisiert, entweder chirurgisch oder durch gezielte mechanische Ruptur. Ein anderer Eingriff destabilisierte den medialen Meniskus, die Pufferstruktur an der Innenseite des Gelenks. Zwei Vergleichsgruppen erhielten entweder eine Scheingesellschaftsoperation (Sham), bei der das Gelenk geöffnet, wichtige Strukturen jedoch intakt gelassen wurden, oder eine leichte ACL‑Verdrehung, die das Band belastete, aber nicht riss. Über zehn Wochen untersuchten die Forschenden wiederholt das Gelenkgewebe mikroskopisch, um Knorpelabnutzung, Knochenveränderungen und Entzündungen der Gelenkinnenhaut zu bewerten.
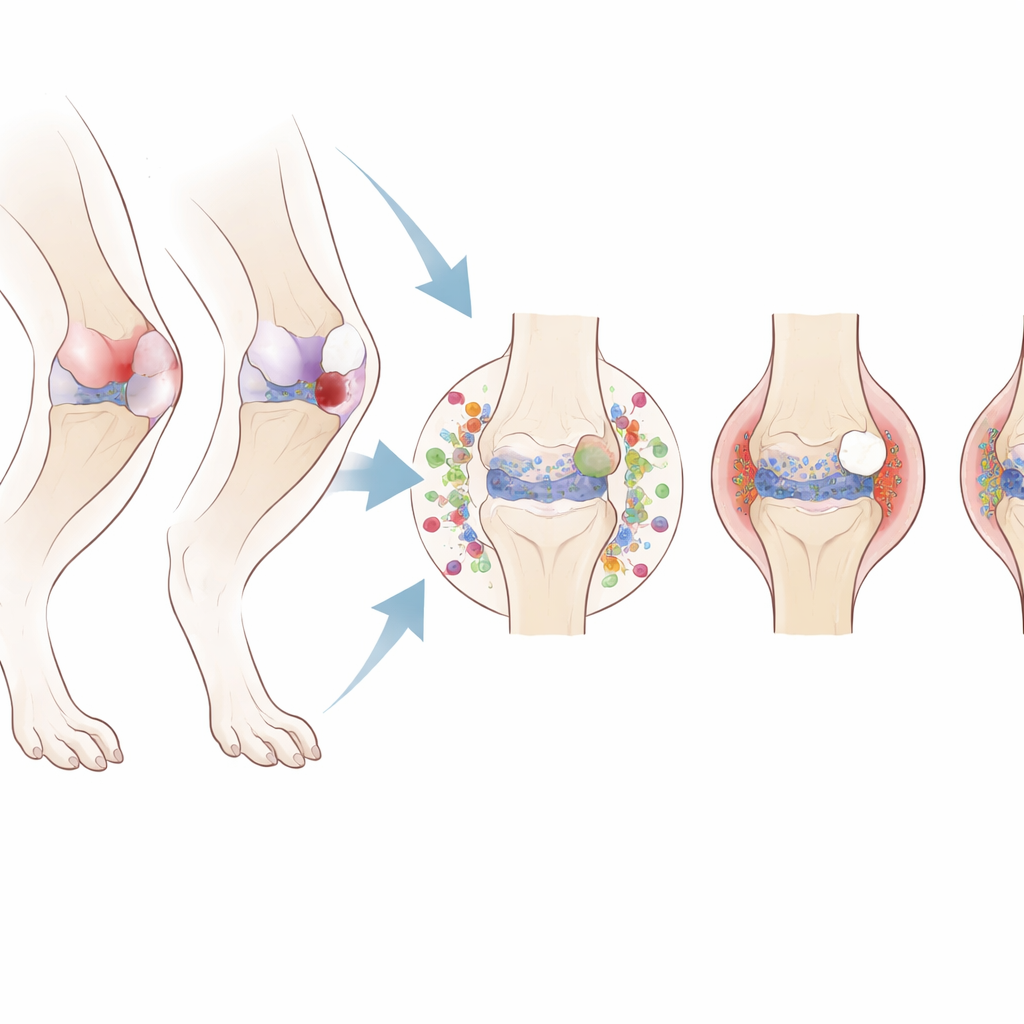
Wie das Gelenk sich langsam abbaut
Die strukturellen Veränderungen im Knie folgten je nach geschädigtem Gewebe unterschiedlichen Mustern. Sowohl chirurgische als auch nicht‑chirurgische ACL‑Rupturen führten zu schnellen und schweren Knorpelschäden, knöchernen Auswüchsen am Gelenkrand und Erosion der Knochen‑Knorpel‑Grenzfläche. Im Gegensatz dazu verursachte eine Meniskusverletzung langsameren, milden Knorpelverschleiß, aber stärkere Verdickung und Verhärtung des darunterliegenden Knochens. Sham‑Operationen und die nicht‑reißende ACL‑Distorsion führten nur zu geringen, spät auftretenden Veränderungen. Diese Befunde zeigen, dass das bloße Öffnen des Gelenks oder eine kurzzeitige Überlastung nicht ausreicht, um eine ausgeprägte posttraumatische Arthrose auszulösen; erheblicher Schaden am ACL oder Meniskus ist erforderlich.
Das Immunsystem rückt ins Gelenk
Um die zugrunde liegende Biologie dieser unterschiedlichen Ergebnisse zu verstehen, nutzten die Forschenden Durchflusszytometrie — eine fortgeschrittene Zählmethode für Zellen — um Immunzellen in der Gelenkinnenhaut, in nahegelegenen Lymphknoten, in der Milz und im Knochenmark zu verfolgen. Alle Verletzungen riefen frühe Entzündungen hervor, doch Gelenke, die zur Arthrose führten, zeigten eine deutlich stärkere und anhaltendere Reaktion. Unmittelbar nach ACL‑ oder Meniskusschaden verließen große Mengen zirkulierender Monozyten — Vorläuferzellen, die sich zu entzündungsfördernden Makrophagen differenzieren können — das Knochenmark und die Milz und tauchten in der Synovialhaut des verletzten Knies auf. Dort nahmen sie einen proinflammatorischen Zustand an, bekannt als M1‑ähnlich, und blieben wochenlang erhöht. Gleichzeitig akkumulierten bestimmte Helfer‑T‑Zell‑Untergruppen, die mit einem aggressiveren Immunprofil assoziiert sind (häufig Th1 und Th17 genannt), im Gelenk, insbesondere nach ACL‑Ruptur.
Lokaler Brand, begrenzte Ausbreitung
Man könnte erwarten, dass eine so starke Reaktion den ganzen Körper erfasst, doch die Studie fand, dass sich das Geschehen größtenteils in der Nähe des verletzten Gelenks abspielte. Veränderungen der Immunzellen in Milz und fernem Knochenmark waren allgemein kurzlebig, während Synovium und der abfließende Lymphknoten neben dem verletzten Bein die deutlichsten und beständigsten Verschiebungen zeigten. Interessanterweise spielte die Art und Weise, wie das ACL geschädigt wurde — chirurgisch oder durch mechanische Belastung — eine deutlich geringere Rolle als das betroffene Gewebe. Modelle mit ACL‑Riss verhielten sich ähnlich zueinander und deutlich anders als das Meniskusmodell. Das unterstreicht, dass „was man verletzt“ wichtiger ist als „wie man es verletzt“, wenn es darum geht, die Immunantwort und das spätere Muster der Gelenkschädigung zu formen.
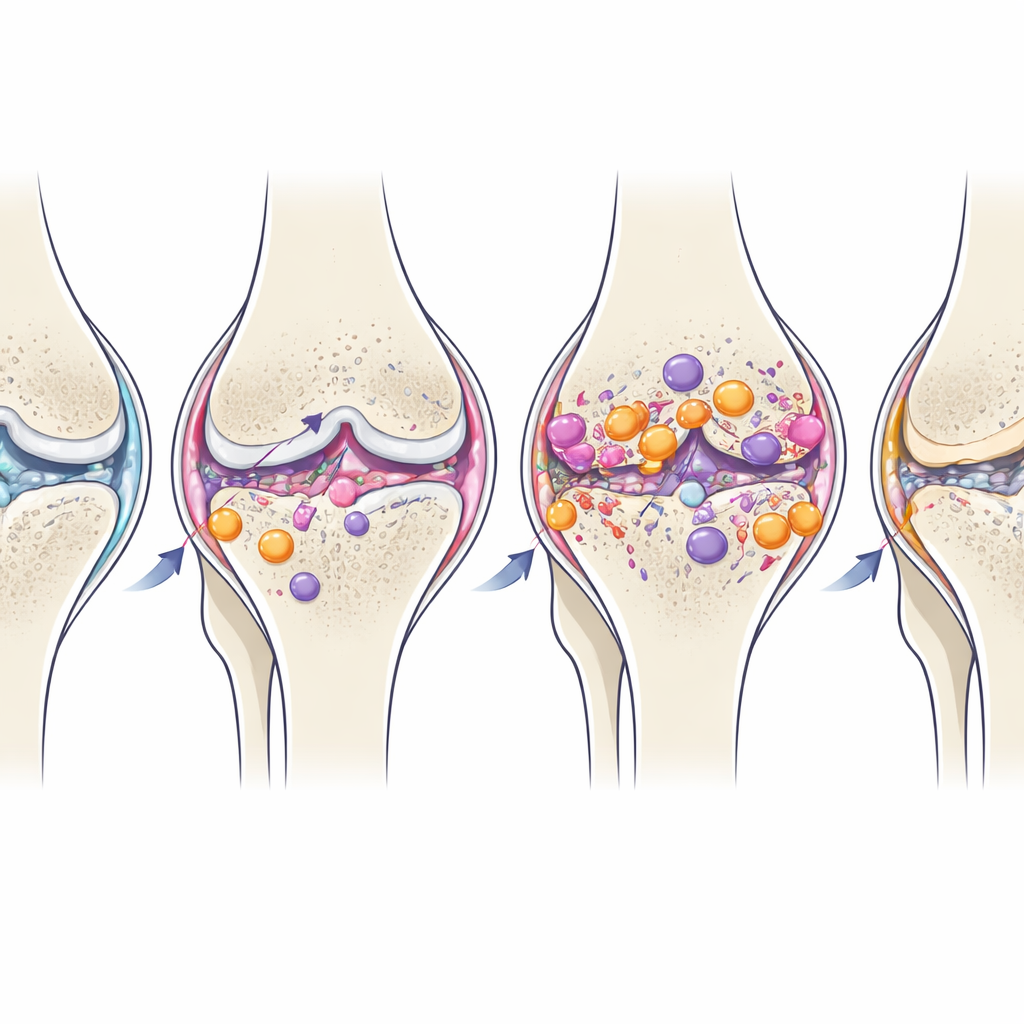
Wenn Entzündung vom Helfer zum Schaden wird
Im Laufe der Zeit verschoben sich einige der im Gelenk ansässigen Makrophagen allmählich in Richtung eines beruhigenderen, M2‑ähnlichen Profils, obwohl sich die strukturellen Schäden weiter verschlechterten. Dieser natürliche späte Umschwung deutet darauf hin, dass das Gelenk versucht, die Entzündung zu beenden; bei posttraumatischer Arthrose kommt dieser Wechsel jedoch zu spät oder ist zu schwach, um den fortschreitenden Knorpelverlust und die Knochenumlagerung zu verhindern. Die anhaltende Erhöhung von Th17‑artigen T‑Zellen im Gelenk, lange nach der Erstverletzung, legt nahe, dass diese Zellen dazu beitragen könnten, das entzündliche Milieu weiter zum Lodern zu bringen.
Was das für verletzte Knie bedeutet
Für eine allgemeine Leserin oder einen allgemeinen Leser, der sich fragt, warum die Sportverletzung der einen Person heilt, während die einer anderen zum lebenslangen Problem wird, bietet diese Arbeit eine wichtige Erkenntnis: Die frühe, lokale Reaktion des Immunsystems auf eine Verletzung kann über das Schicksal des Gelenks mitentscheiden. In diesen Mausmodellen waren Verletzungen, die schließlich eine posttraumatische Arthrose verursachten, gekennzeichnet durch einen starken, lang andauernden Zustrom entzündlicher Monozyten und Makrophagen und eine verschobene Helfer‑T‑Zell‑Antwort in und um das verletzte Knie, bei insgesamt nur moderater Systembeteiligung. Diese Befunde weisen auf neue Behandlungsstrategien hin, die über Operation und Rehabilitation hinausgehen — etwa rechtzeitig eingesetzte Medikamente, die die im Gelenk residenten Immunzellen in den Tagen und Wochen nach der Verletzung wieder ins Gleichgewicht bringen und so das Risiko verringern könnten, dass eine schwere Verstauchung oder ein Riss in eine chronische Arthrose übergeht.
Zitation: Haubruck, P., Colbath, A.C., Blaker, C.L. et al. Comparison of innate and adaptive immune responses to joint injury during the onset and progression of post-traumatic osteoarthritis in common murine models. Sci Rep 16, 9767 (2026). https://doi.org/10.1038/s41598-026-40338-4
Schlüsselwörter: posttraumatische Arthrose, Knieverletzung, Gelenkentzündung, Immunzellen, Mausmodell