Clear Sky Science · de
Adaptive Beispielauswahl für prototypbasierte erklärbare Mitoseerkennung in der digitalen Pathologie
Warum das für die Krebsversorgung wichtig ist
Wenn Pathologinnen und Pathologen Krebsproben unter dem Mikroskop betrachten, hilft das Zählen aktiv teilender Tumorzellen dabei, die Aggressivität eines Tumors einzuschätzen und geeignete Behandlungen zu wählen. Künstliche Intelligenz kann diese teilenden Zellen in digitalen Schnitten inzwischen schnell erkennen, doch ihre Entscheidungen bleiben selbst für Expertinnen und Experten oft undurchsichtig. Diese Arbeit stellt eine Methode namens Adaptive Example Selection (AES) vor, die einem KI-System erlaubt, seine Entscheidungen zu "begründen", indem es auf reale frühere Fälle verweist, die eine Entscheidung stützen oder ihr widersprechen, und macht so die automatisierte Mitoseerkennung transparenter und klinisch vertrauenswürdiger.
Die Herausforderung, teilende Zellen zu finden
Teilende Tumorzellen, sogenannte Mitosefiguren, sind winzig, selten und visuell vielfältig. Unter der üblichen rosa-violetten Färbung können sie sehr ähnlich aussehen wie harmlose Strukturen, etwa absterbende Zellen oder bestimmte Immunzellen. Menschliche Expertinnen und Experten müssen große digitale Schnitte durchsuchen, was langsam, ermüdend und konfliktanfällig ist. Moderne Deep-Learning-Systeme erreichen bei dieser Aufgabe eine gleichwertige oder bessere Leistung als Menschen, verhalten sich aber wie Black Boxes: Sie liefern für jede verdächtige Zelle einen Score, ohne klar zu erklären, warum. In der Medizin, wo Therapieentscheidungen lebensverändernde Folgen haben können, ist diese Unklarheit ein ernsthaftes Hindernis für den Einsatz von KI im Alltag.
Entwicklung eines leistungsstarken, aber undurchsichtigen Detektors
Die Autorinnen und Autoren trainieren zunächst ein hochmodernes Objekterkennungsnetzwerk, basierend auf der Faster R-CNN-Architektur, um Mitosefiguren in einem großen, heterogenen Datensatz namens MIDOG++ zu finden. Diese Bilder stammen sowohl von menschlichen als auch von kaninen Tumoren, über verschiedene Tumortypen und Labore hinweg, und enthalten mehr als elftausend sorgfältig gelabelte teilende Zellen. Um feine Details zu erhalten, werden die Schnitte in kleine Patches zerteilt und stark augmentiert, um reale Variationen in Färbung und Bildgebung nachzuahmen. Der resultierende Detektor erzielt solide Leistungen über Tumortypen hinweg, mit F1-Werten bis zu 0,84, was bestätigt, dass er genau, aber komplex ist—genau die Art von System, das vor klinischem Einsatz bessere Erklärungen benötigt.
Der KI beibringen, sich mit Beispielen zu erklären
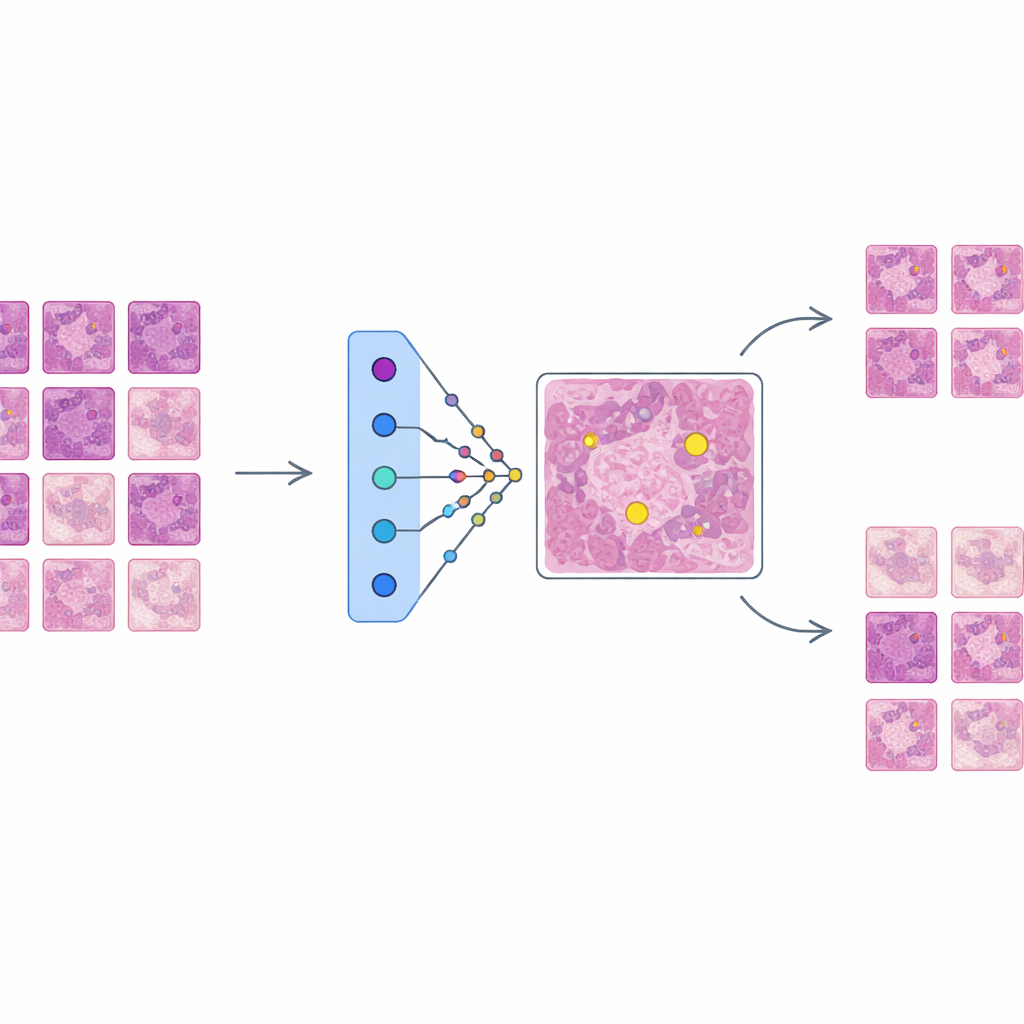
AES sitzt als Interpretationsschicht auf dem trainierten Detektor, ohne dessen Funktionsweise zu verändern. Für jede vom Detektor markierte Kandidatenregion durchsucht AES eine Bibliothek realer Gewebe-Patches aus den Trainingsdaten. Aus dieser Bibliothek wählt es eine kleine Menge "unterstützender" Beispiele aus, die echten Mitosen ähneln, und eine Menge "widersprechender" Beispiele, die eher wie nicht-mitotische Zellen aussehen. Im Hintergrund behandelt AES die Konfidenzwerte des Detektors als glatte Landschaft und verwendet ein mathematisches Werkzeug, radiale Basisfunktionen, um zu approximieren, wie sich diese Konfidenz in der Nähe jedes Falls ändert. Es werden nur Prototypen behalten, die den lokalen Konfidenzwert sinnvoll beeinflussen, sodass die Erklärung für eine einzelne Entscheidung typischerweise aus etwa zehn sorgfältig ausgewählten Beispielen besteht statt aus Hunderten kaum relevanter.
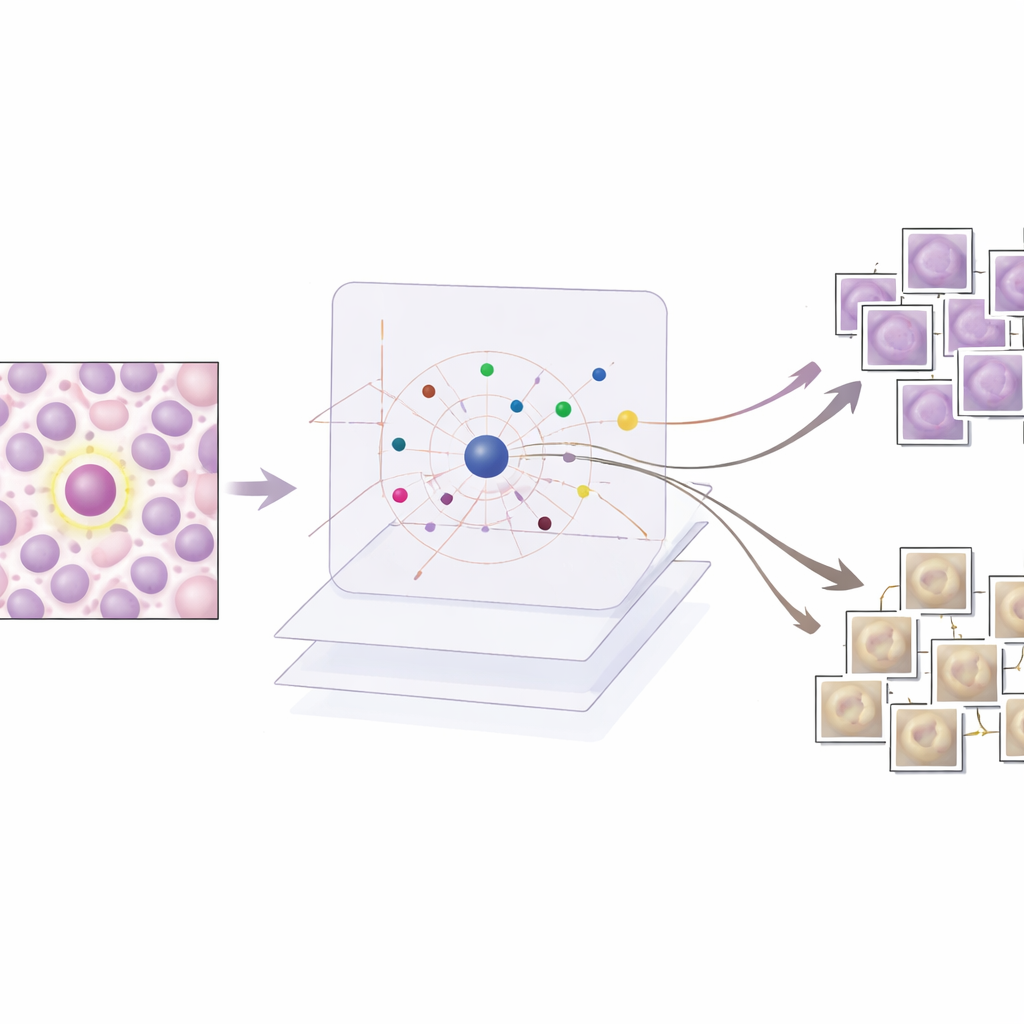
Was die Beispiele über KI-Entscheidungen offenbaren
Die Forschenden bewerten AES sowohl quantitativ als auch qualitativ. Quantitativ zeigen sie, dass ein kompakter Katalog von etwa 190 Prototyp-Bildern die Konfidenzwerte des Detektors mit sehr hoher Genauigkeit nachbilden kann, während die Zahl der pro Fall gezeigten Beispiele niedrig genug bleibt, dass ein Mensch sie prüfen kann. Qualitativ untersuchen sie drei typische Szenarien. Wenn der Detektor eindeutig richtig liegt, liefert AES nur mitotische Prototypen, die die Entscheidung stark stützen, was für Klinikerinnen und Kliniker beruhigend ist. Bei Fehlalarmen zeigt die Methode ähnliche mitotische Beispiele, die erklären, warum der Detektor durch ähnliche Texturen oder Chromatinmuster in die Irre geführt wurde, oft zusammen mit schwächeren nicht-mitotischen Prototypen, die auf Unsicherheit hinweisen. Bei übersehenen Mitosen gibt AES meist vorwiegend nicht-mitotische oder ambivalente Beispiele zurück, was auf blinde Flecken in den Trainingsdaten hinweist und Bereiche markiert, in denen neue oder besser gelabelte Beispiele nötig sind.
Vom Black Box-System zum kollaborativen Werkzeug
Indem jede Vorhersage auf einer Handvoll realer, gelabelter Gewebe-Patches begründet wird, lässt AES einen komplexen KI-Detektor eher wie eine menschliche Kollegin oder einen Kollegen erscheinen, die Entscheidungen durch Rückgriff auf frühere Fälle rechtfertigen. Das System meldet nicht nur, ob eine Zelle wahrscheinlich teilt, sondern zeigt auch, warum und wie sicher es ist, anhand der Zusammensetzung und des Einflusses unterstützender und widersprechender Prototypen. Dieses Design erlaubt Pathologinnen und Pathologen, klare Vorhersagen schnell zu bestätigen, die Aufmerksamkeit auf Grenzfälle oder verwirrende Regionen zu lenken und systematische Fehlerprofile zu identifizieren, die weiteres Training leiten können. Obwohl für die Mitoseerkennung entwickelt, könnte derselbe Ansatz auf weitere Aufgaben in der digitalen Pathologie ausgeweitet werden und so helfen, KI von einer undurchsichtigen Automatisierung zu einem interpretierbaren, fallbasierten Assistenten zu machen, den Klinikerinnen und Kliniker hinterfragen, vertrauen und weiterentwickeln können.
Zitation: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
Schlüsselwörter: erklärbare KI, digitale Pathologie, Mitoseerkennung, prototypbasierte Modelle, Krebsdiagnostik