Clear Sky Science · de
Ultraintensive gepulste Quelle ionisierender Strahlung basierend auf direkter Laserbeschleunigung von Elektronen zur Untersuchung des FLASH-Effekts
Warum ultraschnelle Strahlungspulse wichtig sind
Die Strahlentherapie gegen Krebs balanciert auf einem schmalen Grat: genug Strahlung verabreichen, um Tumore zu zerstören, ohne gesundes Gewebe dauerhaft zu schädigen. Eine jüngste, vielversprechende Idee, der sogenannte FLASH-Effekt, legt nahe, dass eine ultrakurze, ultrastarke Dosisabgabe normales Gewebe schont, während der Tumor weiter angegriffen wird. Diese Studie stellt eine neue experimentelle Strahlungsquelle vor, die auf einem leistungsstarken Laser basiert und extrem kurze Pulse hochenergetischer Elektronen erzeugt. Damit beobachten die Forschenden, wie Sauerstoff in Wasser und biologischen Flüssigkeiten während der Bestrahlung plötzlich verbraucht wird – ein Prozess, der als zentral für den FLASH-Effekt gilt. 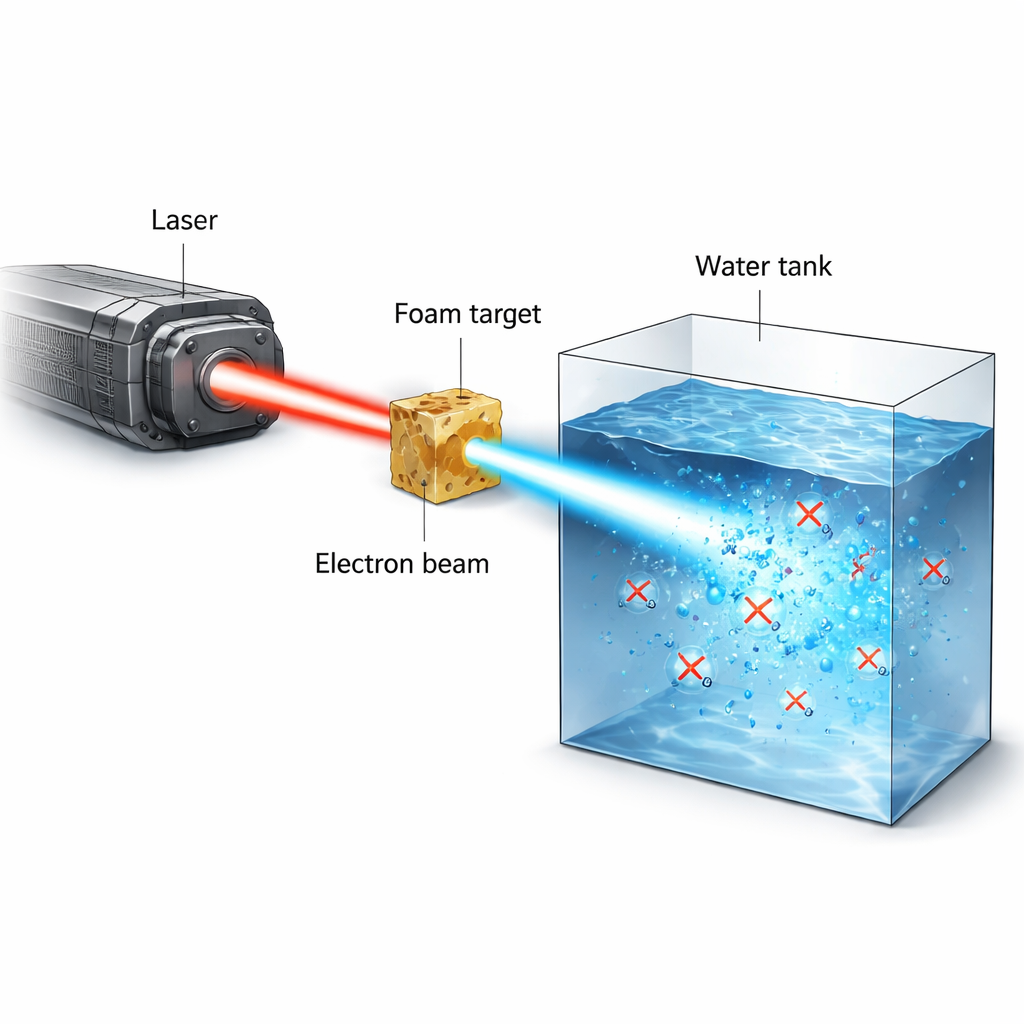
Von Krankenhausgeräten zu lasergetriebenen Strahlen
Konventionelle Radiotherapie nutzt Röntgenstrahlen, Elektronen oder Protonen aus großen Beschleunigern. Diese Geräte liefern Dosen typischerweise über Millisekunden bis Sekunden; obwohl sie sehr präzise sind, schädigen sie dennoch gesundes Gewebe, weil Strahlung indirekt DNA zerstört, indem sie Wassermoleküle spaltet und reaktive Sauerstoffspezies erzeugt. Sauerstoff in gesundem, gut durchblutetem Gewebe verschärft diese Schäden – der sogenannte Sauerstoffeffekt. Die FLASH-Radiotherapie versucht, dieses Problem umzukehren, indem die gesamte therapeutische Dosis in einem Bruchteil einer Sekunde bei ultrahoher Dosisrate verabreicht wird, was in Tierstudien offenbar normales Gewebe vorübergehend schützt, ohne Tumore zu schonen. Standardmedizinische Beschleuniger können diese extremen Dosisraten jedoch schwer erreichen, weshalb nach alternativen Quellen wie Hochleistungslasern gesucht wird.
Schaum und Licht zu einem leistungsstarken Elektronenpuls machen
Die Forschenden nutzten den Hochleistungslaser PHELIX, um schmale, hochstromige Elektronenstrahlen mit Energien von mehreren Millionen Elektronenvolt (MeV) zu erzeugen. Zuerst ionisiert der Laser einen niederdichten Polymerschaum zu einem nahezu kritischen Plasma. In einem zweiten, ultrakurzen Puls von unter einer Billionstel Sekunde drückt und fängt der Laser Elektronen in einem Plasmakanal ein und beschleunigt sie direkt auf hohe Energien. Dieser Prozess, direkte Laserbeschleunigung genannt, erzeugt einen stark kollimierten Strahl, der Zehner von Nanocoulomb Ladung in einem Pikosekunden-Puls transportieren kann. Trifft dieser Strahl auf Wasser oder wasserähnliches Material, kann er in einem einzigen Schuss 20–50 Gray Dosis abgeben, mit momentanen Dosisraten über 10¹³ Gray pro Sekunde – weit über dem, was konventionelle Geräte erreichen.
Beobachtung, wie Sauerstoff im Blitz verschwindet
Um zu untersuchen, wie solche intensiven Pulse die Chemie unter gewebsähnlichen Bedingungen beeinflussen, bauten die Forschenden verschlossene Wassertanks, die im Vakuum betrieben und mit reinem Wasser, Zellkulturmedium oder lysierten Zellen gefüllt werden konnten, jeweils zuvor vollständig mit Sauerstoff gesättigt. Der Elektronenstrahl wurde geformt und gefiltert, sodass hochenergetische Elektronen die Dosis im Tank dominierten, während Protonen und Röntgenstrahlung größtenteils unterdrückt oder durch Abschirmungen und radiochrome Filme genau berücksichtigt wurden. Ein optischer Sensor an der Innenwand des Tanks überwachte gelösten Sauerstoff, indem er misst, wie Sauerstoff die Lumineszenz eines Farbstoffs dämpft. Nach jedem Einzelpulsschuss zeichnete der Sensor einen plötzlichen Abfall der Sauerstoffkonzentration auf, der sich dann langsam wieder entspannte, als Sauerstoff in der Sensorregion diffundierte. Durch Kombination von Filmdaten, Simulationen und bekanntem Bremsvermögen (stopping power) der Elektronen rekonstruierten die Autorinnen und Autoren die in das bestrahlte Volumen eingebrachte Dosis und verknüpften sie direkt mit dem gemessenen Sauerstoffverlust. 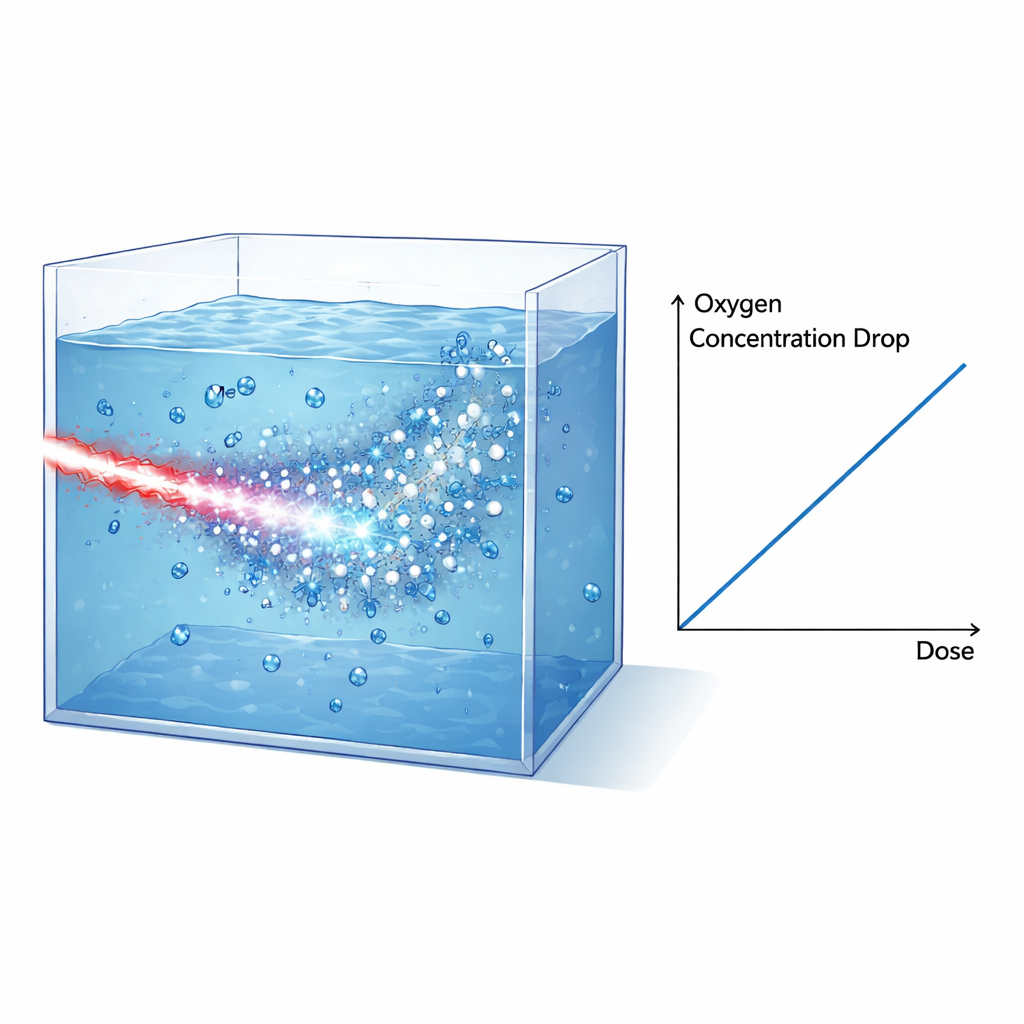
Experiment und Theorie verknüpfen
Die zentrale Erkenntnis ist, dass der Abfall des gelösten Sauerstoffs proportional zur verabreichten Dosis ist, sowohl in Wasser als auch im Kulturmedium, mit sehr ähnlichen Steigungen. Nach Korrektur um eine kleine zusätzliche Dosis durch Röntgenstrahlung liegt der gemessene Sauerstoffverbrauch in Wasser bei etwa 0,32 Mikromol pro Liter und Gray. Dieser Wert stimmt bemerkenswert gut mit Vorhersagen detaillierter Monte-Carlo-Track-Struktur-Simulationen (TRAX-CHEM) überein, die die Bahnen von Elektronen in Wasser verfolgen und die rasche Chemie modellieren, die sich innerhalb von Mikrosekunden nach der Bestrahlung abspielt. Entscheidend ist, dass in diesem lasergetriebenen Aufbau nahezu die gesamte Dosis in etwa einer Pikosekunde geliefert wird – viel kürzer als die charakteristischen Zeiten der folgenden chemischen Reaktionen. Das bedeutet, dass das Experiment die idealen Bedingungen dieser Simulationen eng nachbildet und so ein strenges Testfeld für die zugrundeliegenden Modelle bietet.
Ein besseres Testfeld für FLASH-Forschung bauen
Über die Validierung der Theorie hinaus nutzen die Autorinnen und Autoren ihre Ergebnisse, um ein verbessertes experimentelles Layout zu entwerfen. Durch Vereinfachung der Geometrie, Wegfall von Magneten und symmetrische Platzierung von Wasser und dosismessenden Filmen um den Strahl könnten künftige Setups die Dosis direkt im Tank messen, ohne komplexe Rekonstruktion, und gleichzeitig unerwünschte Protonen- und Röntgenanteile weiter unterdrücken. Simulationen zeigen, dass die Modifikation des Targets – etwa das Hinzufügen dünner Kunststoff- oder Goldschichten – die Dosis pro Schuss zwischen etwa 40 und 80 Gray einstellbar macht und so eine flexible Plattform bietet, um ein breites Spektrum für FLASH-relevante Bedingungen zu erkunden.
Was das für zukünftige Krebstherapien bedeutet
Für Nicht-Fachleute lautet die Kernbotschaft: Diese laserbasierte Quelle erzeugt extrem intensive, ultrakurze Elektronenpulse, die die Bedingungen simulieren – und in mancher Hinsicht übertreffen –, die für die FLASH-Radiotherapie angedacht sind. Die Studie zeigt, dass diese Pulse gelösten Sauerstoff in Wasser und biologischen Medien schnell verbrauchen, und zwar in einer Weise, die mit fortgeschrittenen theoretischen Vorhersagen übereinstimmt. Da Sauerstoffverbrauch und damit verbundene Radikalchemie führende Erklärungsansätze dafür sind, warum FLASH gesundes Gewebe schonen könnte, ist eine kontrollierbare, gut verstandene Quelle wie diese ein großer Fortschritt. Sie bietet ein leistungsfähiges Testfeld zur Verfeinerung von Modellen und letztlich zur Orientierung beim Design künftiger klinischer Geräte, die Krebs effektiver behandeln und Nebenwirkungen reduzieren könnten.
Zitation: Gyrdymov, M., Bukharskii, N., Fabian, V. et al. Ultra-intense pulsed source of ionizing radiation based on direct laser acceleration of electrons for studying the FLASH effect. Sci Rep 16, 7164 (2026). https://doi.org/10.1038/s41598-026-40281-4
Schlüsselwörter: FLASH-Radiotherapie, lasergetriebene Elektronen, ultrahohe Dosisrate, Sauerstoffverbrauch, Wasserradiolyse