Clear Sky Science · de
Selektive Eliminierung monoklonaler Antikörper über den Mannose-Rezeptor hängt von der Glykankopplung ab
Warum Zuckermuster bei Arzneimitteln wichtig sind
Viele der heutigen Blockbuster-Medikamente sind monoklonale Antikörper — gentechnisch hergestellte Proteine, die wochenlang im Blutkreislauf verbleiben können und gezielt Krankheiten wie Krebs und Autoimmunerkrankungen ansteuern. Doch nicht alle Antikörper verhalten sich nach der Injektion gleich. Diese Studie stellt eine täuschend einfache Frage mit weitreichenden Konsequenzen: Wie bestimmt das feine „Zuckermuster“, das an einen Antikörper gebunden ist, wie schnell der Körper ihn entfernt, und könnte das Muster auch Nebenwirkungen wie Immunreaktionen beeinflussen?
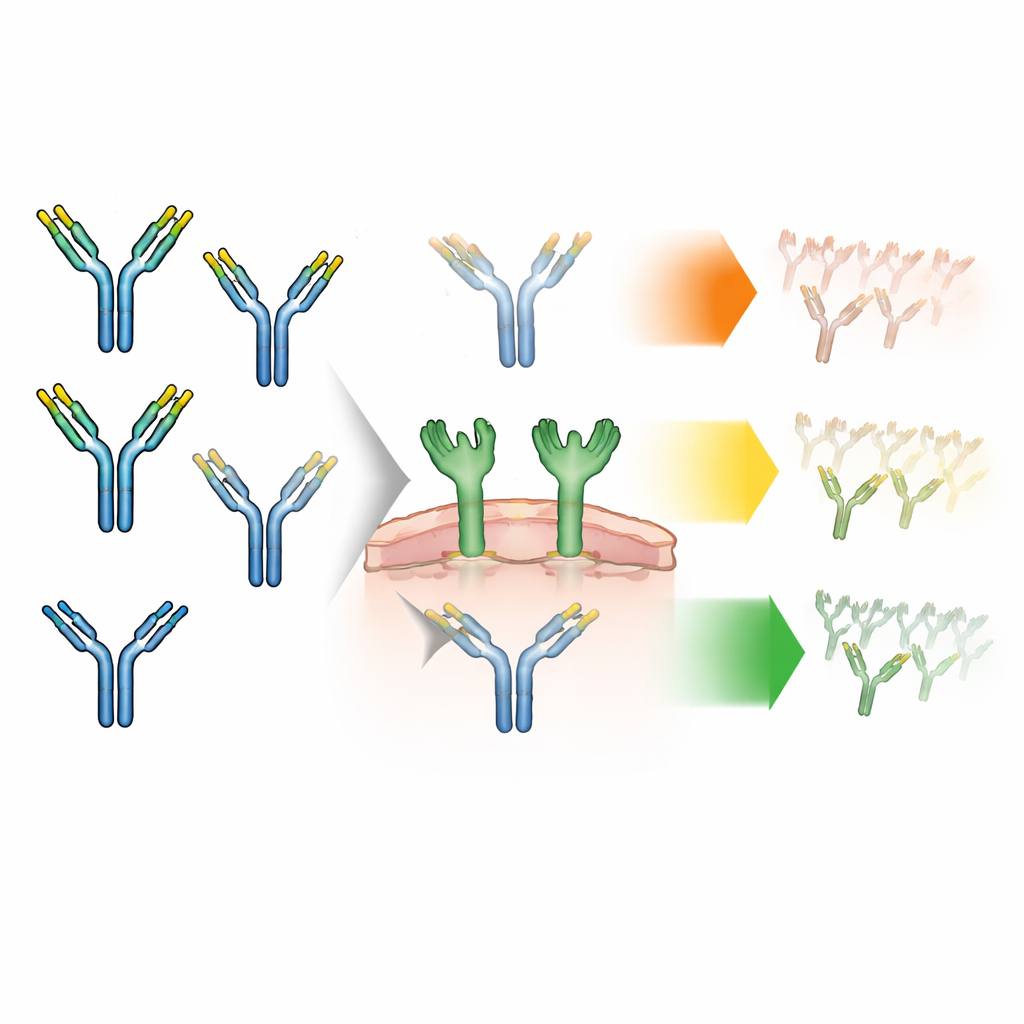
Kleine Zucker als Verkehrsschilder
Antikörper tragen natürlicherweise kurze Zuckerketten — sogenannte Glykanen — an ihrem Gerüst. Diese Glycane treten in unterschiedlichen Ausprägungen auf. Die meisten sind „komplexe“ Strukturen, ein kleinerer Anteil sind „High-Mannose“-Glycane, einfachere Formen, die in früheren Arbeiten mit einer schnelleren Eliminierung aus dem Blut in Verbindung gebracht wurden. Jeder Antikörper hat zwei Zuckerstellen, die ein Paar bilden und entweder gleich (symmetrische Paare) oder verschieden (asymmetrische Paare) sein können. Bisher haben Hersteller meist nur gezählt, wie viele der jeweiligen Zuckerart insgesamt vorhanden sind, ohne zu prüfen, wie die beiden Zucker desselben Antikörpers gepaart sind. Die Autor:innen vermuteten, dass dieses Paarungsmuster verändern könnte, wie stark Antikörper mit einem speziellen Zucker-erkennenden Protein auf Immunzellen, dem Mannose-Rezeptor, interagieren — und damit wie schnell der Körper das Arzneimittel eliminiert.
Antikörper nach ihren Zuckerpaaren sortieren
Um das zu untersuchen, erzeugte das Team Antikörper, die vermehrt High-Mannose-Glycane tragen, und trennte sie dann physikalisch in drei Hauptgruppen: Antikörper mit zwei komplexen Glykanen, mit einem komplexen und einem High-Mannose-Glykan (asymmetrisch) oder mit zwei High-Mannose-Glykanen (symmetrisch). Sie überprüften sorgfältig, dass sich diese Gruppen in allen anderen Eigenschaften nahezu nicht unterscheiden: gleiche Größe, Form, Ladung und Stabilität sowie ähnliche Bindung an den Recycling-Rezeptor, der Antikörper normalerweise vor Abbau schützt. Damit konnten Unterschiede, die sie später in Zellexperimenten oder im Tiermodell beobachteten, eindeutig auf die Glykanpaarung zurückgeführt werden, nicht auf versteckte Schädigungen oder Verunreinigungen.
Zusehen, wie Zellen Antikörper aufnehmen
Als Nächstes fragten die Forscher:innen, wie schnell jedes Zuckermuster Antikörper in Zellen ziehen lässt, die den Mannose-Rezeptor tragen. Sie markierten die verschiedenen Antikörperfraktionen mit einem fluoreszenten Marker und inkubierten sie mit menschlichen Zellen, die so verändert waren, dass sie diesen Rezeptor zeigten. Über nahezu drei Tage verfolgten sie das Fluoreszenzsignal in den Zellen als Maß für die Aufnahme. Alle Antikörper wurden bis zu einem gewissen Grad aufgenommen, doch die Raten unterschieden sich: Antikörper mit zwei High-Mannose-Glykanen wurden am schnellsten internalisiert, solche mit einem High-Mannose-Glykan zeigten eine mittlere Aufnahme, und Antikörper mit nur komplexen Glykanen wurden am langsamsten aufgenommen. Als das Team Mannan — einen natürlichen Zucker, der mit dem Mannose-Rezeptor konkurriert — hinzufügte, sank die Aufnahme der High-Mannose-Antikörper deutlich, was bestätigte, dass dieser Rezeptor für einen Großteil der schnellen Internalisierung verantwortlich war.
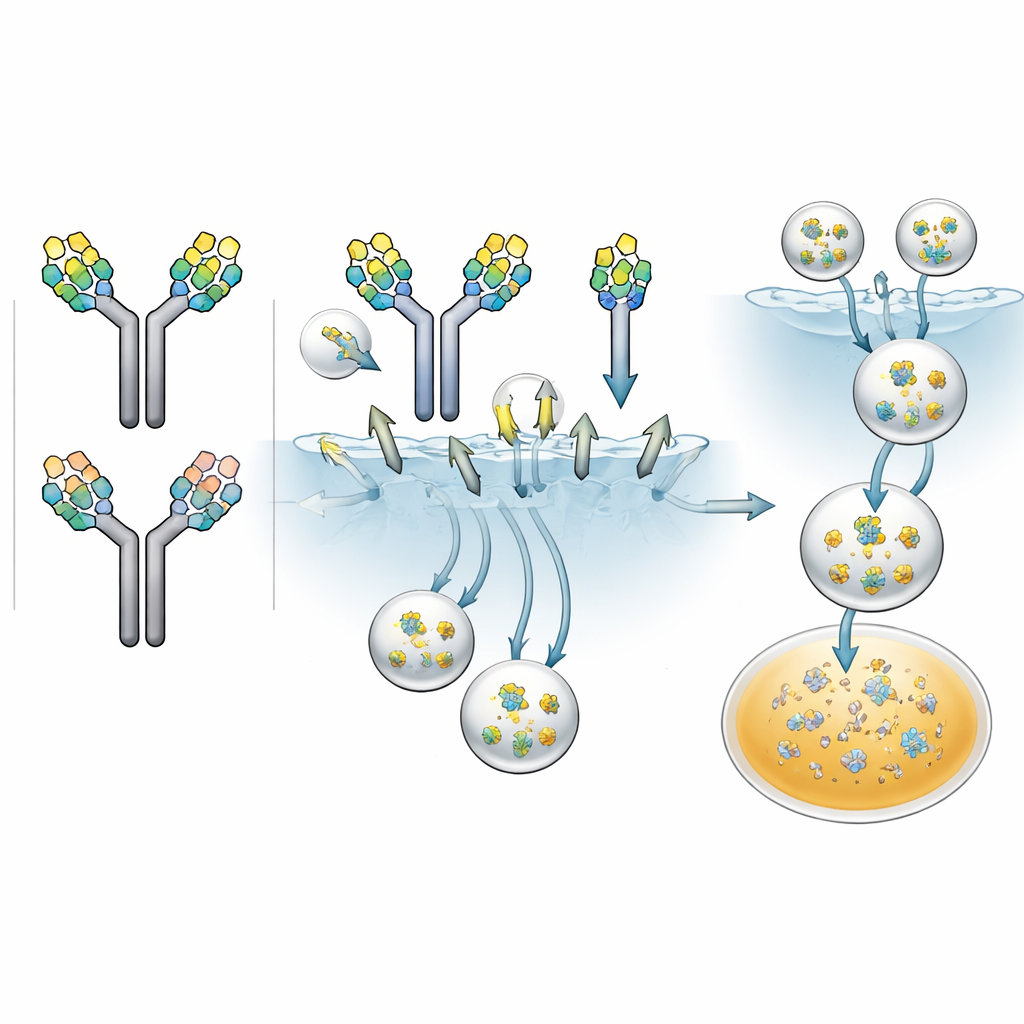
Zuckermarkierte Antikörper in lebenden Tieren verfolgen
Der entscheidende Test war, ob sich diese zellulären Unterschiede in realem Arzneimittelverhalten niederschlagen. Die Wissenschaftler:innen stellten ein Arzneimittelpräparat her, das reiche Anteile von symmetrischen und asymmetrischen High-Mannose-Paaren sowie ausschließlich komplexe Paare enthielt, und injizierten es Ratten. Mit sensiblen Massenspektrometriemethoden konnten sie nicht nur die Gesamtantikörperkonzentration über zwei Wochen verfolgen, sondern auch, wie jede Glykanpaarung im Zeitverlauf abnahm. Das Muster war deutlich: Antikörper mit zwei High-Mannose-Glykanen verschwanden am schnellsten, mit einer Halbwertszeit von etwa 2,4 Tagen; solche mit einem High-Mannose-Glykan hielten länger, etwa 7,2 Tage; und Antikörper mit nur komplexen Glykanen blieben ungefähr 17,4 Tage. Die Exposition über die Zeit — die Fläche unter der Konzentrationskurve — fiel im Vergleich zum reinen komplexen Paar auf 38 % für das doppelte High-Mannose-Paar und auf 73 % für das gemischte Paar. Im Grunde wirkte jedes zusätzliche High-Mannose-Glykan wie eine zusätzliche „klare mich“‑Markierung für den Mannose-Rezeptor.
Was das für sichere, länger wirkende Medikamente bedeutet
Für Patient:innen machen diese Ergebnisse verständlich, warum zwei Antikörperpräparate, die auf dem Papier ähnlich aussehen, sich im Körper unterschiedlich verhalten können. Die Studie zeigt, dass nicht nur das Vorhandensein, sondern die Paarung von High-Mannose-Glykanen maßgeblich beeinflusst, wie schnell Antikörper entfernt werden — vermutlich über mannose-rezeptorvermittelte Aufnahme und Abbau in Immunzellen. Da derselbe Weg auch Antigene in die Maschinerie einspeisen kann, die Immunantworten auslöst, könnten diese Zuckermuster auch das Risiko für Anti‑Drug‑Antikörper und allergische Reaktionen beeinflussen. Die Autor:innen plädieren dafür, dass Hersteller die Glykanpaarung — nicht nur die Gesamtzuckerzusammensetzung — überwachen und steuern, wenn sie Antikörpertherapeutika entwickeln und testen. So ließen sich vorhersehbarere Dosierungen, länger anhaltende Wirkungen und ein geringeres Risiko unerwünschter Immunreaktionen erreichen.
Zitation: Baumeister, J., Meudt, M., Wei, W. et al. Selective clearance of monoclonal antibodies via the mannose receptor is dependent on glycan pairing. Sci Rep 16, 8489 (2026). https://doi.org/10.1038/s41598-026-40268-1
Schlüsselwörter: monoklonale Antikörper, Glykosylierung, Mannose-Rezeptor, Pharmakokinetik, Immunogenität